摘要:2.加热分解: Cu(OH)2 △==CuO+H2O
网址:http://m.1010jiajiao.com/timu_id_3731507[举报]
工业上制备氯化铜时,是将浓盐酸用蒸气加热至80℃左右,慢慢加入粗制氧化铜粉末(含杂质氧化亚铁),充分搅拌,使之溶解,反应如下:CuO+2HCl═CuCl2+H2O FeO+2HCl═FeCl2+H2O; 已知:pH≥9.6时,Fe2+以Fe(OH)2形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀.除去溶液中的Fe2+,可以采用的方法是( )
查看习题详情和答案>>
工业上制备氯化铜时,是将浓盐酸用蒸气加热至80℃左右,慢慢加入粗制氧化铜粉末(含杂质氧化亚铁),充分搅拌,使之溶解,反应如下:CuO+2HCl═CuCl2+H2O FeO+2HCl═FeCl2+H2O; 已知:pH≥9.6时,Fe2+以Fe(OH)2形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀.除去溶液中的Fe2+,可以采用的方法是( )
查看习题详情和答案>>
| A.直接加碱,调整溶液pH≥9.6 |
| B.加纯铜粉,将Fe2+还原出来 |
| C.先将Fe2+氧化成Fe3+,再调整pH在3~4 |
| D.通入硫化氢,使Fe2+直接沉淀 |
工业上制备氯化铜时,是将浓盐酸用蒸气加热至80℃左右,慢慢加入粗制氧化铜粉末(含杂质氧化亚铁),充分搅拌,使之溶解,反应如下:CuO+2HCl═CuCl2+H2O FeO+2HCl═FeCl2+H2O; 已知:pH≥9.6时,Fe2+以Fe(OH)2形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀.除去溶液中的Fe2+,可以采用的方法是( )
A.直接加碱,调整溶液pH≥9.6
B.加纯铜粉,将Fe2+还原出来
C.先将Fe2+氧化成Fe3+,再调整pH在3~4
D.通入硫化氢,使Fe2+直接沉淀
查看习题详情和答案>>
A.直接加碱,调整溶液pH≥9.6
B.加纯铜粉,将Fe2+还原出来
C.先将Fe2+氧化成Fe3+,再调整pH在3~4
D.通入硫化氢,使Fe2+直接沉淀
查看习题详情和答案>>
如图所示装置是用于气体制备、干燥、性质验证、尾气处理的部分仪器装置(加热及夹持固定装置均已略去).请根据下列要求回答问题.
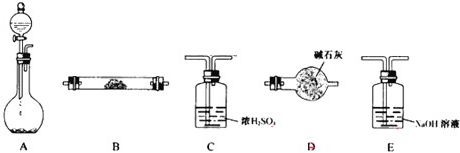
(1)若烧瓶中盛装Na2O2,分液漏斗中盛装浓氨水,则:
①烧瓶内除了能产生O2外,还能产生大量NH3.能产生大量NH3的原因是:
a.Na2O2与水反应,使溶剂减少,降低NH3的溶解量,使氨气逸出;
b.Na2O2与水反应,放热,使氨气逸出;
c.
②用产生的气体做氨的催化氧化实验,各仪器装置按气流方向(从左到右)连接顺序是:A→
(2)若烧瓶中盛装X g Zn片,分液漏斗中盛装稀H2SO4,则:
①当制备H2、验证H2还原性并检验H2的氧化产物,仪器连接顺序A→C→B→B→D时,两次使用B装置,第一个B装置中反应的化学方程式为
②上述实验中如果使用的是纯锌,反应速度往往较慢,为了加快H2产生的速率可采取的方法有
a、将烧瓶放入热水中.b、将稀H2SO4改为浓H2SO4.c、在稀H2SO4溶液中滴入少量CuSO4.d、在稀H2SO4中加入少量固体NaCl.
③若锌片不纯(杂质不与稀H2SO4反应),稀H2SO4及B装置中固体足量,反应后测得第一个B装置质量的变化Y g,则锌片纯度为
.
查看习题详情和答案>>

(1)若烧瓶中盛装Na2O2,分液漏斗中盛装浓氨水,则:
①烧瓶内除了能产生O2外,还能产生大量NH3.能产生大量NH3的原因是:
a.Na2O2与水反应,使溶剂减少,降低NH3的溶解量,使氨气逸出;
b.Na2O2与水反应,放热,使氨气逸出;
c.
Na2O2与水反应生成OH-,c(OH-)增大,抑制NH3?H2O的电离,有利于NH3的逸出
Na2O2与水反应生成OH-,c(OH-)增大,抑制NH3?H2O的电离,有利于NH3的逸出
;②用产生的气体做氨的催化氧化实验,各仪器装置按气流方向(从左到右)连接顺序是:A→
D
D
→B
B
→E
E
.(2)若烧瓶中盛装X g Zn片,分液漏斗中盛装稀H2SO4,则:
①当制备H2、验证H2还原性并检验H2的氧化产物,仪器连接顺序A→C→B→B→D时,两次使用B装置,第一个B装置中反应的化学方程式为
H2+CuO
H2O+Cu
| ||
H2+CuO
H2O+Cu
、第二个B装置中所盛的药品是
| ||
无水CuSO4
无水CuSO4
;D装置的作用是防止空气中的水进入装置,干扰H2氧化产物的检验
防止空气中的水进入装置,干扰H2氧化产物的检验
.②上述实验中如果使用的是纯锌,反应速度往往较慢,为了加快H2产生的速率可采取的方法有
a、c
a、c
a、将烧瓶放入热水中.b、将稀H2SO4改为浓H2SO4.c、在稀H2SO4溶液中滴入少量CuSO4.d、在稀H2SO4中加入少量固体NaCl.
③若锌片不纯(杂质不与稀H2SO4反应),稀H2SO4及B装置中固体足量,反应后测得第一个B装置质量的变化Y g,则锌片纯度为
| 65Y |
| 16X |
| 65Y |
| 16X |
(2013?浙江)氢能源是一种重要清洁能源.现有两种可产生H2的化合物甲和乙.将6.00g甲加热至完全分解,只得到一种短周期元素的金属单质和6.72L的H2(已折算成标准状况).甲与水反应也能放出H2,同时还产生一种白色沉淀物,该白色沉淀可溶于NaOH溶液.化合物乙在催化剂存在下可分解得到H2和另一种单质气体丙,丙在标准状况下的密度为1.25g?L-1.请回答下列问题:
(1)甲的化学式是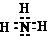
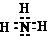 .
.
(2)甲与水反应的化学方程式是
(3)气体丙与金属镁反应的产物是
(4)乙在加热条件下与CuO反应可生成Cu和气体丙,写出该反应的化学方程式
(5)甲与乙之间
查看习题详情和答案>>
(1)甲的化学式是
AlH3
AlH3
;乙的电子式是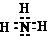
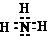
(2)甲与水反应的化学方程式是
AlH3+3H2O=Al(OH)3↓+3H2↑
AlH3+3H2O=Al(OH)3↓+3H2↑
.(3)气体丙与金属镁反应的产物是
Mg3N2
Mg3N2
(用化学式表示).(4)乙在加热条件下与CuO反应可生成Cu和气体丙,写出该反应的化学方程式
3CuO+2NH3
N2+3Cu+3H2O
| ||
3CuO+2NH3
N2+3Cu+3H2O
.有人提出产物Cu中可能还混有Cu2O,请设计实验方案验证之
| ||
取样后加H2SO4,如果溶液变蓝,说明产物中含有Cu2O,反之则无Cu2O
取样后加H2SO4,如果溶液变蓝,说明产物中含有Cu2O,反之则无Cu2O
.(已知:Cu2O+2H+═Cu+Cu2++H2O)(5)甲与乙之间
可能
可能
(填“可能”或“不可能”)发生反应产生H2,判断理由是AlH3中的H为-1价,NH3中的H为+1价,有可能发生氧化还原反应生成氢气
AlH3中的H为-1价,NH3中的H为+1价,有可能发生氧化还原反应生成氢气
.