摘要:4.铜的冶炼 (1)高温冶炼黄铜矿(CuFeS2)2CuFeS2+O2=Cu2S+2FeS+SO2↑ 2Cu2S+3O2=2Cu2O+2SO2↑ 2Cu2O+Cu2S=6Cu+SO2↑ (2)生物炼铜:浸出黄铜矿
网址:http://m.1010jiajiao.com/timu_id_3731502[举报]
(2013?肇庆一模)铜是一种重要的金属元素,位于元素周期表第ⅠB族,+1价的铜与氯离子结合的生成的CuCl是一种难溶物质,但它可与过量的Cl-形成可溶于水的络离子[CuCl2]-.含铜最丰富的天然资源是黄铜矿(CuFeS2).
(1)目前有一种湿法冶炼技术,以黄铜矿为主要原料来生产铜、铁红颜料和可用于橡胶硫化的硫单质,原料的综合利用率较高.其主要流程如下:
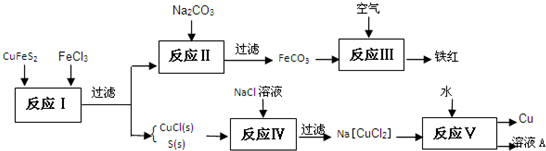
①请完成反应Ⅰ中FeCl3与CuFeS2反应的化学方程式:
CuFeS2+
②写出反应Ⅳ中发生反应的离子方程式:
③反应Ⅲ是FeCO3在空气中煅烧,其化学方程式是
④已知Cu+ 在反应V中发生自身氧化还原反应,歧化为Cu2+和Cu.则反应Ⅴ所得溶液A中含有的溶质有
(2)传统工艺从黄铜矿冶炼粗铜的技术,是将精选后的富铜矿砂与空气在高温下煅烧,使其转变为铜.与上面湿法冶炼技术方法比较,新方法的优点是
查看习题详情和答案>>
(1)目前有一种湿法冶炼技术,以黄铜矿为主要原料来生产铜、铁红颜料和可用于橡胶硫化的硫单质,原料的综合利用率较高.其主要流程如下:

①请完成反应Ⅰ中FeCl3与CuFeS2反应的化学方程式:
CuFeS2+
3
3
FeCl3=CuCl
CuCl
+4FeCl2
FeCl2
+2S.②写出反应Ⅳ中发生反应的离子方程式:
Cl-+CuCl=[CuCl2]-
Cl-+CuCl=[CuCl2]-
.③反应Ⅲ是FeCO3在空气中煅烧,其化学方程式是
4FeCO3+O2
+2Fe2O3
| ||
4FeCO3+O2
+2Fe2O3
.
| ||
④已知Cu+ 在反应V中发生自身氧化还原反应,歧化为Cu2+和Cu.则反应Ⅴ所得溶液A中含有的溶质有
CuCl2、NaCl
CuCl2、NaCl
.(2)传统工艺从黄铜矿冶炼粗铜的技术,是将精选后的富铜矿砂与空气在高温下煅烧,使其转变为铜.与上面湿法冶炼技术方法比较,新方法的优点是
不会产生SO2污染大气
不会产生SO2污染大气
、不用煅烧黄铜矿从而节约热能
不用煅烧黄铜矿从而节约热能
.辉铜矿(主成份为Cu2S)通适量的空气可冶炼金属铜,经过一系列反应可得到B和D、E.G为砖红色沉淀.

请回答下列问题:
(1)辉铜矿(Cu2S)通适量的空气冶炼金属铜的化学方程式
(2)E的浓溶液与Cu发生反应②的化学方程式是
(3)利用电解可提纯粗,在该电解反应中阳极物质是
(4)自然界中当胆矾矿与黄铁矿(FeS2二硫化亚铁)相遇时会缓慢发生下列反应产生辉铜矿.对反应:14CuSO4+5FeS2+12H2O═7Cu2S+5FeSO4+12H2SO4,被氧化的硫和被还原的硫的质量比为
查看习题详情和答案>>

请回答下列问题:
(1)辉铜矿(Cu2S)通适量的空气冶炼金属铜的化学方程式
Cu2S+O2(适量)
2Cu+SO2
| ||
Cu2S+O2(适量)
2Cu+SO2
其中氧化剂为
| ||
O2和Cu2S
O2和Cu2S
.(2)E的浓溶液与Cu发生反应②的化学方程式是
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
| ||
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
.
| ||
(3)利用电解可提纯粗,在该电解反应中阳极物质是
粗铜
粗铜
,电解质溶液是硫酸铜或含Cu2+的盐溶液
硫酸铜或含Cu2+的盐溶液
;(4)自然界中当胆矾矿与黄铁矿(FeS2二硫化亚铁)相遇时会缓慢发生下列反应产生辉铜矿.对反应:14CuSO4+5FeS2+12H2O═7Cu2S+5FeSO4+12H2SO4,被氧化的硫和被还原的硫的质量比为
3:7
3:7
.铜是一种重要的金属元素,铜元素与银元素同处第ⅠB族,+1价的铜和+1价的银都可形成二配位的络离子,如Ag(NH3)2+、AgCl2-等,含铜最丰富的天然资源是黄铜矿(CuFeS2).
(1)从黄铜矿冶炼粗铜的传统工艺是将精选后的富铜矿砂与空气在高温下煅烧,使其转变为铜.这种方法的缺点是、.
(2)现有一种湿法冶炼技术,以黄铜矿为主要原料来生产铜、铁红颜料和可用于橡胶硫化的硫单质,原料的综合利用率较高.其主要流程如下:

①写出反应Ⅰ中FeCl3与CuFeS2所发生反应的化学方程式:
②写出反应Ⅳ中发生反应的离子方程式:
③反应Ⅲ是FeCO3在空气中煅烧,写出化学方程式:
④反应Ⅴ所得溶液A中含有的溶质有
查看习题详情和答案>>
(1)从黄铜矿冶炼粗铜的传统工艺是将精选后的富铜矿砂与空气在高温下煅烧,使其转变为铜.这种方法的缺点是、.
(2)现有一种湿法冶炼技术,以黄铜矿为主要原料来生产铜、铁红颜料和可用于橡胶硫化的硫单质,原料的综合利用率较高.其主要流程如下:

①写出反应Ⅰ中FeCl3与CuFeS2所发生反应的化学方程式:
CuFeS2+3FeCl3=CuCl↓+4FeCl2+2S↓
CuFeS2+3FeCl3=CuCl↓+4FeCl2+2S↓
;②写出反应Ⅳ中发生反应的离子方程式:
Cl-+CuCl=[CuCl2]-
Cl-+CuCl=[CuCl2]-
.③反应Ⅲ是FeCO3在空气中煅烧,写出化学方程式:
4FeCO3+O2═4CO2+2Fe2O3
4FeCO3+O2═4CO2+2Fe2O3
.④反应Ⅴ所得溶液A中含有的溶质有
CuCl2、NaCl
CuCl2、NaCl
.(2012?山东)工业上由黄铜矿(主要成分CuFeS2)冶炼铜的主要流程如下:

(1)气体A中的大气污染物可选用下列试剂中的
a.浓H2SO4 b.稀HNO3
c.NaOH溶液 d.氨水
(2)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在
(3)由泡铜冶炼粗铜的化学反应方程式为
(4)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
(5)利用反应2Cu+O2+2H2SO4═2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,其正极电极反应式为
查看习题详情和答案>>

(1)气体A中的大气污染物可选用下列试剂中的
cd
cd
吸收.a.浓H2SO4 b.稀HNO3
c.NaOH溶液 d.氨水
(2)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在
Fe3+
Fe3+
(填离子符号),检验溶液中还存在Fe2+的方法是取少量溶液,滴加KMnO4溶液,KMnO4溶液紫色褪去;
取少量溶液,滴加KMnO4溶液,KMnO4溶液紫色褪去;
(注明试剂、现象).(3)由泡铜冶炼粗铜的化学反应方程式为
3Cu2O+2Al
Al2O3+6Cu
| ||
3Cu2O+2Al
Al2O3+6Cu
.
| ||
(4)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是
bd
bd
.a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
(5)利用反应2Cu+O2+2H2SO4═2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,其正极电极反应式为
4H++O2+4e-=2H2O
4H++O2+4e-=2H2O
.黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可以制备硫及铁的化合物.
(1)冶炼铜的反应为8CuFeS2+21O2
8Cu+4FeO+2Fe2O3+16SO2
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是
(2)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是
(3)过二硫酸钾(K2S2O8)具有强氧化性,可将I-氧化为I2:S2O82-+2I-=2SO42-+I2
通过改变反应途径,Fe3+、Fe2+均可催化上述反应.试用离子方程式表示Fe3+对上述反应的催化过程.
(4)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、AI2O3)可制备Fe2O3.方法为
①用稀盐酸浸取炉渣,过滤.
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得.
据以上信息回答下列问题:
a.除去AI2O3的离子方程式是
b.选用提供的试剂,设计实验验证炉渣中含有FeO.
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水
所选试剂为
查看习题详情和答案>>
(1)冶炼铜的反应为8CuFeS2+21O2
| ||
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是
Cu、O
Cu、O
(填元素符号).(2)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是
AD
AD
(填字母).| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 铜绿的主成分是碱酸铜 | 可用稀盐酸除铜器表面的铜绿 | Ⅰ对;Ⅱ对;有 |
| B | 铜表易形成致密的氧化膜 | 铜容器可以盛放浓硫酸 | Ⅰ对;Ⅱ对;有 |
| C | 铁比铜活泼 | 例在铜板上的铁钉在潮湿空气中不易生锈 | Ⅰ对;Ⅱ对;有 |
| D | 蓝色硫酸铜晶体受热转化为白色硫酸铜粉末是物理变化 | 硫酸铜溶液可用作游泳池的消毒剂 | Ⅰ错;Ⅱ对;无 |
通过改变反应途径,Fe3+、Fe2+均可催化上述反应.试用离子方程式表示Fe3+对上述反应的催化过程.
2Fe3++2I-=2Fe2++I2
2Fe3++2I-=2Fe2++I2
、S2O82-+2Fe2+=2SO42-+2Fe3+
S2O82-+2Fe2+=2SO42-+2Fe3+
(不必配平).(4)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、AI2O3)可制备Fe2O3.方法为
①用稀盐酸浸取炉渣,过滤.
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得.
据以上信息回答下列问题:
a.除去AI2O3的离子方程式是
6H++AI2O3=3H2O+2Al3+、Al3++4OH-=2H2O+AlO2-
6H++AI2O3=3H2O+2Al3+、Al3++4OH-=2H2O+AlO2-
.b.选用提供的试剂,设计实验验证炉渣中含有FeO.
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水
所选试剂为
稀硫酸、KMnO4溶液
稀硫酸、KMnO4溶液
.证明炉渣中含有的实验现象为稀硫酸浸取炉渣所得溶液使KMnO4溶液褪色
稀硫酸浸取炉渣所得溶液使KMnO4溶液褪色
.