摘要: (1). H2.HF,H2O,NH3,NO(2)①2F2+2H2O=4HF+O2 .②4NH3+5O2=4NO+6H2O ③4NH3+6NO=5N2+6H2O
网址:http://m.1010jiajiao.com/timu_id_3728678[举报]
(1)写电离方程式:①H2SO4
(2)写出下列盐溶液的水解离子方程式:
①Fe(NO3)3
②NaF
③K2CO3
(3)在T℃下,将1mol N2和3mol H2的混合气体通入固定体积为2L的密闭容器内,起始压强为101KPa,经过30s达到平衡,测得平衡混合气体的平均相对分子质量为10.试求:
①此反应过程中N2的平均反应速率为
②H2的转化率为
③维持一定温度和压强不变,在起始体积为2L的体积可变的容器中充入1mol N2、3mol H2,达平衡时N2的转化率与上述平衡相等,则该平衡时,容器的体积为
(4)有可逆反应A(g)+B(g)?2C(g),在不同温度下经过一定时间,混合物中C的体积分数与温度的关系如图所示.填写下列空白:
①反应在
②正反应为
③由T3向T4变化时,v正
查看习题详情和答案>>
H2SO4═2H++SO42-
H2SO4═2H++SO42-
;②NaHCO3NaHCO3=Na++HCO3-
NaHCO3=Na++HCO3-
;HCO3-?CO32-+H+
HCO3-?CO32-+H+
;(2)写出下列盐溶液的水解离子方程式:
①Fe(NO3)3
Fe3++3H2O?Fe(OH)3+3H+
Fe3++3H2O?Fe(OH)3+3H+
;②NaF
F-+H2O?HF+OH-
F-+H2O?HF+OH-
;③K2CO3
CO32-+H2O?HCO3-+OH-
CO32-+H2O?HCO3-+OH-
(以第一步为主)(3)在T℃下,将1mol N2和3mol H2的混合气体通入固定体积为2L的密闭容器内,起始压强为101KPa,经过30s达到平衡,测得平衡混合气体的平均相对分子质量为10.试求:
①此反应过程中N2的平均反应速率为
0.005mol?L-1?s-1
0.005mol?L-1?s-1
.②H2的转化率为
30%
30%
.③维持一定温度和压强不变,在起始体积为2L的体积可变的容器中充入1mol N2、3mol H2,达平衡时N2的转化率与上述平衡相等,则该平衡时,容器的体积为
1.7
1.7
L.
(4)有可逆反应A(g)+B(g)?2C(g),在不同温度下经过一定时间,混合物中C的体积分数与温度的关系如图所示.填写下列空白:
①反应在
T3
T3
温度下达到平衡.②正反应为
放热
放热
热反应(填“放”或“吸”).③由T3向T4变化时,v正
<
<
v逆(填“>”、“<”或“=”).2013年12月2日,我国在西昌卫星发射中心用“长征三号甲”运载火箭将“嫦娥三号”探月卫星成功送入太空,进一步向广寒宫探索.“长征三号甲”是三级液体助推火箭,一、二级为常规燃料,常规燃料通常指以肼(N2H4)为燃料,以二氧化氮做氧化剂.
Ⅰ.常规燃料通常指以肼(N2H4)为燃料,以二氧化氮做氧化剂.但有人认为若用氟气代替二氧化氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体).
已知:N2H4(g)+O2(g)═N2(g)+2H2O(g),△H=-543kJ?mol-1;
H2(g)+
F2(g)═HF(g),△H=-269kJ?mol-1;H2(g)+
O2(g)═H2O(g),△H=-242kJ?mol-1
请写出肼和氟气反应的热化学方程式: .
Ⅱ.氧化剂二氧化氮可由NO和O2生成,已知在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2ΝΟ2(g)△H的体系中,n(NO)随时间的变化如表:
(1)已知:K800℃>K1000℃,则该反应的△H 0(填“大于”或“小于”),用O2表示从0~2s内该反应的平均速率为 .
(2)能说明该反应已达到平衡状态的是 .
a.容器内颜色保持不变 b. 2v逆(NO)=v正(O2)
c.容器内压强保持不变 d.容器内密度保持不变
(3)为使该反应的速率增大,提高NO的转化率,且平衡向正反应方向移动应采取的措施有 .
(4)在上述条件下,计算通入2mol NO和1mol O2的平衡常数K= .
(5)在上述条件下,若开始通入的是0.2mol NO2气体,达到化学平衡时,则NO2的转化率为 .
查看习题详情和答案>>
Ⅰ.常规燃料通常指以肼(N2H4)为燃料,以二氧化氮做氧化剂.但有人认为若用氟气代替二氧化氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体).
已知:N2H4(g)+O2(g)═N2(g)+2H2O(g),△H=-543kJ?mol-1;
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
请写出肼和氟气反应的热化学方程式:
Ⅱ.氧化剂二氧化氮可由NO和O2生成,已知在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2ΝΟ2(g)△H的体系中,n(NO)随时间的变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.200 | 0.100 | 0.080 | 0.050 | 0.050 | 0.050 |
| n(O2)(mol) | 0.100 | 0.050 | 0.040 | 0.025 | 0.025 | 0.025 |
(2)能说明该反应已达到平衡状态的是
a.容器内颜色保持不变 b. 2v逆(NO)=v正(O2)
c.容器内压强保持不变 d.容器内密度保持不变
(3)为使该反应的速率增大,提高NO的转化率,且平衡向正反应方向移动应采取的措施有
(4)在上述条件下,计算通入2mol NO和1mol O2的平衡常数K=
(5)在上述条件下,若开始通入的是0.2mol NO2气体,达到化学平衡时,则NO2的转化率为
已知:H2(g)+F2(g)═2HF(g)△H=-270kJ/mol,下列说法正确的是( )
| A、氟化氢气体分解生成氢气和氟气的反应是放热反应 | B、1 mol H2与1 mol F2反应生成2 mol液态HF放出的热量大于270 kJ | C、在相同条件下,1 mol H2与1 mol F2的能量总和大于2 mol HF气体的能量 | D、 该反应中的能量变化可用图来表示 |
已知:H2(g)+F2(g)→2HF(g)+270kJ/mol,下列说法正确的是( )
| A、在相同条件下,1 mol H2与1 mol F2的能量总和大于2 mol HF气体的能量 | B、1 mol H2与1 mol F2反应生成2 mol液态HF放出的热量小于270 kJ | C、该反应的逆反应是放热反应 | D、该反应过程的能量变化可用如图来表示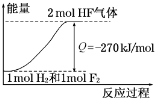 |