摘要:碳酸钠和碳酸氢钠 名称 碳酸钠 碳酸氢钠 化学式 俗名 水溶液酸碱性 色态 溶解性 与盐酸反应的现象及离子方程式 与澄清石灰水反应 与BaCl2溶液反应的现象及离子方程式 与硫酸铝溶液反应现象及离子方程式 稳定性 用途 相互转化 (感悟高考)2.除去NaHCO3溶液中混有的少量Na2CO3.可采取的方法是( ) A.通入二氧化碳气体 B.加入氢氧化钡溶液 C.加入澄清石灰水 D.加入稀盐酸 思考与交流:(1)Na2CO3溶液与盐酸作用时.滴加顺序不同.现象一样吗? (2)根据上述性质用多种方法区别Na2CO3与NaHCO3. [教学反思]
网址:http://m.1010jiajiao.com/timu_id_3728274[举报]
碳酸钠、碳酸氢钠是两种重要的化学试剂.根据要求回答:
Ⅰ.兴趣小组设计三种方案,鉴别浓度均为0.01mol?L-1碳酸钠和碳酸氢钠两种溶液:
(1)甲方案中pH较大的是 ;
(2)结果表明方案乙无法实现鉴别目的,用离子方程式表示方案乙发生的反应: ; .
(3)经过查阅资料获得如下信息:Ksp(CaCO3)=4.96×10-9;0.01mol?L-1 NaHCO3、Na2CO3溶液中
c(CO32-)如表所示:
丙方案能否实现鉴别目的? ;理由是 ;
Ⅱ.纯碱生产过程中,所得产品往往混有一定量的氯化钠.为检测纯碱的纯度,可采用多种方案来进行.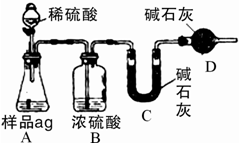
(4)如图为学生丁设计的方案,试图通过测定样品(a g)与足量的稀硫酸反应产生的CO2质量来实现目的.
①本方案存在缺陷,对纯碱纯度检测的影响.
缺陷: ;所测纯碱的纯度将 (填“偏大”或“偏小”).
②方案经改进后,丁进行了实验,并测得B、C、D三套装置的质量分别增重了m1、m2和m3.则纯碱的纯度为 .
(5)现只有少量(约1g)纯碱样品、0.100mol?L-1硫酸和蒸馏水,同学戊拟通过测定一定质量的纯碱样品与硫酸反应时消耗硫酸体积来确定纯碱的纯度.实验过程中,需用 (填仪器名称)测量硫酸的体积,而且实验过程中还需用到的一种试剂是 .
查看习题详情和答案>>
Ⅰ.兴趣小组设计三种方案,鉴别浓度均为0.01mol?L-1碳酸钠和碳酸氢钠两种溶液:
| 序号 | 甲 | 乙 | 丙 |
| 方案 | 用广泛pH试纸 检测溶液pH |
滴加等体积0.1mol?L-1 Ba(OH)2溶液 |
滴加等体积0.1mol?L-1 CaCl2溶液 |
(2)结果表明方案乙无法实现鉴别目的,用离子方程式表示方案乙发生的反应:
(3)经过查阅资料获得如下信息:Ksp(CaCO3)=4.96×10-9;0.01mol?L-1 NaHCO3、Na2CO3溶液中
c(CO32-)如表所示:
| 0.01mol?L-1溶液 | NaHCO3 | Na2CO3 |
| c(CO32-)/mol?L-1 | 0.00011 | 0.0087 |
Ⅱ.纯碱生产过程中,所得产品往往混有一定量的氯化钠.为检测纯碱的纯度,可采用多种方案来进行.

(4)如图为学生丁设计的方案,试图通过测定样品(a g)与足量的稀硫酸反应产生的CO2质量来实现目的.
①本方案存在缺陷,对纯碱纯度检测的影响.
缺陷:
②方案经改进后,丁进行了实验,并测得B、C、D三套装置的质量分别增重了m1、m2和m3.则纯碱的纯度为
(5)现只有少量(约1g)纯碱样品、0.100mol?L-1硫酸和蒸馏水,同学戊拟通过测定一定质量的纯碱样品与硫酸反应时消耗硫酸体积来确定纯碱的纯度.实验过程中,需用
碳酸氢钠是生活中常见的物质.请回答下列问题.
(1)碳酸氢钠俗称 ,其水溶液显 性(填“酸”、“碱”或“中”).
(2)有33.6g碳酸氢钠加热分解止无气体产生为止,剩余的固体是 (填名称).
(3)计算(2)剩余固体的物质的量和质量.(写出计算过程) 查看习题详情和答案>>
(1)碳酸氢钠俗称
(2)有33.6g碳酸氢钠加热分解止无气体产生为止,剩余的固体是
(3)计算(2)剩余固体的物质的量和质量.(写出计算过程) 查看习题详情和答案>>
碳酸钠俗称纯碱,是一种常用化学品。工业上制取碳酸钠的方法是:将二氧化碳和氨气通入饱和食盐水中,控制一定温度,制得碳酸氢钠,再煅烧碳酸氢钠使其转化为碳酸钠。有关反应的化学方程式为:?

(1)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是________ (填标号)。
A.碳酸氢钠难溶于水?
B.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出?
C.碳酸氢钠受热易分解?
(2)某探究活动小组根据工业制取碳酸钠的原理,进行碳酸氢钠的制备实验, 同学们按各自设计的方案实验。?
①一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出)。?
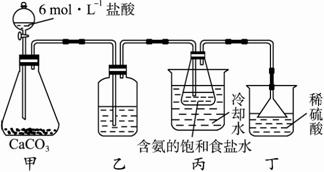
i.乙装置中的试剂是_______________(填标号)。?
A.烧碱溶液?
B.澄清石灰水?
C.浓氨水?
D.蒸馏水?
ii.丁装置的作用是_________________________。?
iii.实验结束后,分离出NaHCO3晶体的操作是_________________(填名称)。
②另一位同学用下图中戊装置(其他装置未画出)进行实验。
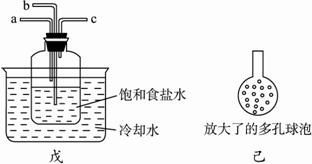
i.实验时,须先从a管通入_________气体,再从b管通入____________气体。?
ii.有同学建议在b管下端连接上图中己装置,理由是__________________________。?
(3)请你再写出一种实验室制取少量碳酸氢钠的方法。____________________________。
查看习题详情和答案>>碳酸锰(MnCO3)是理想的高性能强磁性材料,也是制备Mn2O3、MnO2等锰的氧化物的重要原料,广泛用于电子、化工、医药等行业.一种制备MnCO3的生产流程如图所示.

已知生成氢氧化物的pH和有关硫化物的Ksp如下表:
软锰矿主要成分为MnO2,其中含有铁、铝、硅的氧化物和少量重金属化合物杂质,SO2来自工业废气.流程①中主要发生的反应有:MnO2+SO2=MnSO4 2Fe3++SO2+2H2O=2Fe2++SO42-+4H+.
(1)流程①中所得MnSO4溶液的pH比软锰矿浆的pH______(填“大”或“小”),该流程可与______(填工业生产名称)联合,生产效益更高.
(2)反应②的目的是将溶液中的Fe2+氧化成Fe3+,其离子反应方程式为______,这样设计的目的和原理是______
(3)反应③中硫化钠的作用是使重金属离子转化为硫化物沉淀,碳酸钙的作用是______.
(4)反应④发生的化学反应为:MnSO4+2NH4HCO3=MnCO3↓+(NH4)2SO4+CO2↑+H2O.
反应中通常需加入稍过量的NH4HCO3,且控制溶液的pH为6.8~7.4.加入稍过量的NH4HCO3的目的是______,溶液的pH不能过低的原因是______.
(5)软锰矿中锰的浸出有两种工艺:
工艺A:软锰矿浆与含SO2的工业废气反应 工艺B:软锰矿与煤炭粉混合,焙烧后加稀硫酸溶解.
其中工艺A的优点是______.(答对1个即可)
查看习题详情和答案>>

已知生成氢氧化物的pH和有关硫化物的Ksp如下表:
| 物质 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 8.3 |
| 完全沉淀pH | 3.7 | 9.6 | 9.8 |
| 物质 | MnS | CuS | PbS |
| Ksp | 2.5×10-13 | 6.3×10-36 | 8.0×10-28 |
(1)流程①中所得MnSO4溶液的pH比软锰矿浆的pH______(填“大”或“小”),该流程可与______(填工业生产名称)联合,生产效益更高.
(2)反应②的目的是将溶液中的Fe2+氧化成Fe3+,其离子反应方程式为______,这样设计的目的和原理是______
(3)反应③中硫化钠的作用是使重金属离子转化为硫化物沉淀,碳酸钙的作用是______.
(4)反应④发生的化学反应为:MnSO4+2NH4HCO3=MnCO3↓+(NH4)2SO4+CO2↑+H2O.
反应中通常需加入稍过量的NH4HCO3,且控制溶液的pH为6.8~7.4.加入稍过量的NH4HCO3的目的是______,溶液的pH不能过低的原因是______.
(5)软锰矿中锰的浸出有两种工艺:
工艺A:软锰矿浆与含SO2的工业废气反应 工艺B:软锰矿与煤炭粉混合,焙烧后加稀硫酸溶解.
其中工艺A的优点是______.(答对1个即可)