摘要:(四).离子方程式正误判断 一看反应能否用离子方程式表示. 1.看离子反应是否符合客观事实.不可主观臆造产物及反应.如:铁和稀盐酸的反应: 2Fe+6H+=2Fe3++3H2↑ 2.是离子反应.但不能写离子方程式.如: NH4Cl2(s)→ Cu+H2SO4(浓) → 二看连接符号和状态符号是否准确. 1. 一般离子反应用“= 连接.可逆反应.弱电解质的电离.盐类水解反应用“ 连接. 2. 大多离子反应要用“↑ “↓ 注明产物的状态.而盐类水解反应由于水解程度极弱.不能使用状态符号. 三看表示各物质的化学式是否准确. 1.强酸.强碱和易溶于水的盐要拆写为离子.难溶物质.难电离物质.挥发性物质.单质.氧化物.非电解质等要书写为化学式. 2.微溶物作为反应物.若是澄清溶液拆写为离子.若是悬浊液写为化学式.微溶物作为生成物.一般写为化学式.并标“↓ 符号. 3.多元弱酸酸式根离子.在离子方程式中不能拆写. 四看是否漏写离子反应.如强硫酸与氢氧化钡的离子反应写为:Ba2++SO42-=BaSO4↓. 五看质量.电荷是否守恒.即离子方程式是否配平.离子方程式要做到两守恒:原子数目守恒.电荷数目守恒.如:Fe3++Cu=Fe2++Cu2+. 六看反应物或产物的配比是否正确.是否符合题设条件及要求.如“过量 .“少量 .“适量 .“足量 以及特殊的数值比等.
网址:http://m.1010jiajiao.com/timu_id_3717240[举报]
(2012?上海模拟)X、Y、Z、W是短周期的四种元素,有关它们的信息如下表所示.
填写下列空白:(提示:不能用字母X、Y、Z、W作答)
(1)X单质分子的结构式是
 ,Z元素原子最外层共有
,Z元素原子最外层共有
(2)X、Y、Z三元素的最高价氧化物的水化物酸性由强到弱的顺序是
(3)常温时,W的硫酸盐溶液的pH
(4)25℃、101kPa时,32g Y的最低价气态氢化物完全燃烧生成稳定的氧化物时放出1780.6kJ的热量,写出该反应的热化学方程式
查看习题详情和答案>>
| 元素 | 部分结构知识 | 部分性质 |
| X | X的单质由双原子分子构成,分子中有14个电子 | X有多种氧化物,如XO、XO2、X2O4等;通常情况下XO2与X2O4共存 |
| Y | Y原子的次外层电子数等于最外层电子数的一半 | Y能形成多种气态氢化物 |
| Z | Z原子的最外层电子数多于4 | Z元素的最高正化合价与最低负化合价代数和等于6 |
| W | W原子的最外层电子数等于2n-3(n为原子核外电子层数) | 化学反应中W原子易失去最外层电子形成Wn+ |
(1)X单质分子的结构式是


17
17
种不同运动状态的电子.(2)X、Y、Z三元素的最高价氧化物的水化物酸性由强到弱的顺序是
HClO4>HNO3>H2CO3
HClO4>HNO3>H2CO3
.(3)常温时,W的硫酸盐溶液的pH
<
<
7(填“=”、“>”或“<”),理由是:Al3++3H2O?Al(OH)3+3H+
Al3++3H2O?Al(OH)3+3H+
(用离子方程式表示).(4)25℃、101kPa时,32g Y的最低价气态氢化物完全燃烧生成稳定的氧化物时放出1780.6kJ的热量,写出该反应的热化学方程式
CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3KJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3KJ/mol
.(2012?南昌三模)X、Y、Z、W是短周期的四种元素,有关他们的信息如下表所示.
填写下列空白:(提示:不能用字母X、Y、Z、W作答)
(1)X的气态氢化物分子的电子式是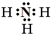
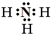 ,Z元素在周期表中的位置是
,Z元素在周期表中的位置是
(2)X、Y、Z三元素的最高价氧化物的水化物酸性由强到弱的顺序是
(3)常温时,W的硫酸盐溶液的pH
(4)实验室用X的氢化物的水溶液制取W的氢氧化物的方法是(用离子方程式表示)
(5)25℃、101kPa时,32g Y的最低价气态氢化物完全燃烧生成稳定的氧化物时放出1780.6kJ的热量,写出该反应的热化学方程式
查看习题详情和答案>>
| 元素 | 部分结构知识 | 部分性质 |
| X | X的单质由双原子分子构成,分子中有14个电子 | X有多种氧化物,如XO、XO2、X2O4等;通常情况下XO2与X2O4共存 |
| Y | Y原子的次外层电子数等于最外层电子数的一半 | Y能形成多种气态氢化物 |
| Z | Z原子的最外层电子数多于4 | Z元素的最高正化合价与最低负化合价代数和等于6 |
| W | W原子的最外层电子数等于2n-3(n为原子核外电子层数) | 化学反应中W原子易失去最外层电子形成Wn+ |
(1)X的气态氢化物分子的电子式是
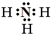
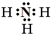
第三周期第ⅦA族
第三周期第ⅦA族
.(2)X、Y、Z三元素的最高价氧化物的水化物酸性由强到弱的顺序是
HClO4>HNO3>H2CO3
HClO4>HNO3>H2CO3
.(3)常温时,W的硫酸盐溶液的pH
<
<
7(填“=”、“>”或“<”),理由是:Al3++3H2O Al(OH)3+3H+
Al(OH)3+3H+
 Al(OH)3+3H+
Al(OH)3+3H+Al3++3H2O Al(OH)3+3H+
Al(OH)3+3H+
(用离子方程式表示). Al(OH)3+3H+
Al(OH)3+3H+(4)实验室用X的氢化物的水溶液制取W的氢氧化物的方法是(用离子方程式表示)
Al3++3NH3?H2O═Al(OH)3↓+3NH4+
Al3++3NH3?H2O═Al(OH)3↓+3NH4+
.(5)25℃、101kPa时,32g Y的最低价气态氢化物完全燃烧生成稳定的氧化物时放出1780.6kJ的热量,写出该反应的热化学方程式
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3kJ/mol
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3kJ/mol
.原子序数依次增大的主族元素A、B、C、D分别处于第一至第四周期,其中A原子核是一个质子;B原子核外电子有6种不同的运动状态,B与C可形成正四面体型分子,D原子外围电子排布为3d104s1. 回答下列问题:
(1)这四种元素中电负性最大的是
(2)C所在的主族元素气态氢化物中,沸点最低的是
(3)B元素可形成多种单质,其中“只有一层原子厚”的物质,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,该材料晶体 结构如图所示,其原子的杂化类型为
(4)D的水合醋酸盐晶体局部结构如图,该晶体中含有的化学键是
①极性键 ②非极性键 ③配位键 ④金属键
(5)某学生所做的有关D元素的实验流程如图:
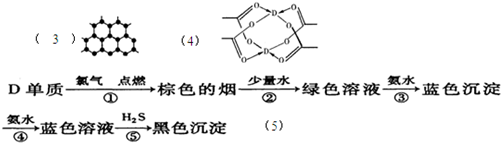
请书写第⑤反应的离子方程式:
查看习题详情和答案>>
(1)这四种元素中电负性最大的是
Cl
Cl
(填元素符号)、第一电离能最小的是Cu
Cu
(填元素符号);(2)C所在的主族元素气态氢化物中,沸点最低的是
HCl
HCl
(填化学式);(3)B元素可形成多种单质,其中“只有一层原子厚”的物质,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,该材料晶体 结构如图所示,其原子的杂化类型为
sp2
sp2
;(4)D的水合醋酸盐晶体局部结构如图,该晶体中含有的化学键是
①②③
①②③
;①极性键 ②非极性键 ③配位键 ④金属键
(5)某学生所做的有关D元素的实验流程如图:

请书写第⑤反应的离子方程式:
〔Cu(NH3)4〕2++H2S+2H2O=CuS↓+2NH4++2NH3?H2O
〔Cu(NH3)4〕2++H2S+2H2O=CuS↓+2NH4++2NH3?H2O
.现有下列10种物质
①NaHCO3;②NH4HCO3;③BaSO4;④HF;⑤C2H5OH;⑥Al;⑦食盐水;⑧CH3COOH; ⑨HCl;=10 ⑩NaOH.
(1)其中属于非电解质的是 (填序号,下同),既能跟盐酸反应又能跟NaOH溶液反应的是 .
(2)NaHCO3溶液显 性(填“酸”、“碱”或“中”),原因是(结合离子方程式表示)
.
(3)常温时有四种溶液:Ⅰ.pH=4的CH3COOH溶液;Ⅱ.pH=4的HCl溶液;Ⅲ.pH=10的NaOH溶液;Ⅳ.pH=10的CH3COONa溶液.(已知常温时醋酸的电离常数为1.75×10-5)
下列有关叙述正确的是 .(忽略溶液混合时的体积变化)
A.Ⅱ、Ⅲ溶液分别与10g铝粉充分反应,生成H2的量Ⅲ一定更多
B.Ⅰ与Ⅱ等体积混合后,溶液中的c(CH3COO-)为原溶液浓度的
C.将Ⅰ和Ⅲ等体积混合后,溶液pH一定小于7
D.四种溶液各10mL分别加水稀释至100mL后,溶液的pH:Ⅲ>Ⅳ>Ⅰ>Ⅱ
(4)常温时某HCl溶液中由水电离出的C(H+)=1×10-amol/L,而相同pH的AlCl3溶液中由水电离出的C(H+)=1×10-bmol/L (已知a,b均为小于14的正整数),则a和b之间满足的关系为 , (用一个等式和一个不等式表示).
查看习题详情和答案>>
①NaHCO3;②NH4HCO3;③BaSO4;④HF;⑤C2H5OH;⑥Al;⑦食盐水;⑧CH3COOH; ⑨HCl;=10 ⑩NaOH.
(1)其中属于非电解质的是
(2)NaHCO3溶液显
(3)常温时有四种溶液:Ⅰ.pH=4的CH3COOH溶液;Ⅱ.pH=4的HCl溶液;Ⅲ.pH=10的NaOH溶液;Ⅳ.pH=10的CH3COONa溶液.(已知常温时醋酸的电离常数为1.75×10-5)
下列有关叙述正确的是
A.Ⅱ、Ⅲ溶液分别与10g铝粉充分反应,生成H2的量Ⅲ一定更多
B.Ⅰ与Ⅱ等体积混合后,溶液中的c(CH3COO-)为原溶液浓度的
| 1 | 2 |
C.将Ⅰ和Ⅲ等体积混合后,溶液pH一定小于7
D.四种溶液各10mL分别加水稀释至100mL后,溶液的pH:Ⅲ>Ⅳ>Ⅰ>Ⅱ
(4)常温时某HCl溶液中由水电离出的C(H+)=1×10-amol/L,而相同pH的AlCl3溶液中由水电离出的C(H+)=1×10-bmol/L (已知a,b均为小于14的正整数),则a和b之间满足的关系为
(2013?黄山一模)X、Y、Z、W是短周期的四种元素,有关它们的信息如下表所示.
填写下列空白:
(1)X有多种同素异形体,写出X2电子式是
 ,
,
(2)X,Y,Z三种元素电负性由大到小顺序为
(3)W元素原子基态时原子的电子排布式
(4)Z位于元素周期表第
(5)含W的一种硫酸盐是常用的净水剂,常温时该溶液的pH
(6)25℃、101kPa时,32g Y的最低价气态氢化物完全燃烧生成稳定的氧化物时放出1780.6kJ的热量,写出该反应的热化学方程式
查看习题详情和答案>>
| 元素 | 部分结构知识 | 部分性质 |
| X | X原子核外电子占有9个原子轨道 | X的一种氧化物是形成酸雨的主要物质 |
| Y | Y原子的次外层电子数等于最外层电子数的一半 | Y能形成多种气态氢化物 |
| Z | Z原子的最外层电子数多于4 | Z元素的最高正化合价与最低负化合价代数和等于6 |
| W | W原子的最外层电子数等于2n-3(n为原子核外电子层数) | 化学反应中W原子易失去最外层电子形成Wn+ |
(1)X有多种同素异形体,写出X2电子式是


(2)X,Y,Z三种元素电负性由大到小顺序为
Cl>S>C
Cl>S>C
.(3)W元素原子基态时原子的电子排布式
1s22s22p63s23p1
1s22s22p63s23p1
.(4)Z位于元素周期表第
三
三
周期第ⅦA
ⅦA
族(5)含W的一种硫酸盐是常用的净水剂,常温时该溶液的pH
<
<
7(填“=”、“>”或“<”),理由是:Al3++3H2O?Al(OH)3+3H+
Al3++3H2O?Al(OH)3+3H+
(用离子方程式表示).(6)25℃、101kPa时,32g Y的最低价气态氢化物完全燃烧生成稳定的氧化物时放出1780.6kJ的热量,写出该反应的热化学方程式
CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3KJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3KJ/mol
.