摘要:某一可逆反应.在一定条件下.经过不同的途径建立平衡时.各组分的百分含量(质量百分含量.体积分数.物质的量分数)对应相等的状态互称为等效平衡状态. 比如.我们到达的目的地是郭店.可以从新郑或新村出发.也可以从郑州或龙湖出发.行走的方向可能相同也可能相反.走的途径不一样.路程也可能不相等.但最终目的是一样的.都是郭店.即都达到了相同的效果.就是等效的.
网址:http://m.1010jiajiao.com/timu_id_3716449[举报]
 在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g).其化学平衡常数K和温度T的关系如下表,回答下列问题:
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g).其化学平衡常数K和温度T的关系如下表,回答下列问题:| T℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
>
>
0;若该反应符合如图所示的关系,则在图中,Y轴是指CO2或H2的百分含量等
CO2或H2的百分含量等
. (答出一种即可)(2)能判断该反应达到化学平衡状态的依据是
bc
bc
(多选扣分).a.容器中压强不变 b.混合气体中c(CO)不变
c.v(H2)正=v(H2O)逆 d.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式:0.9?c(CO2)?c(H2)=c(CO)?c(H2O),由此可以判断此时的温度为
800
800
℃.其它条件不变,升高温度,原化学平衡向逆
逆
反应方向移动(填“正”或“逆”),容器内混合气体的平均相对分子质量不变
不变
(填“增大”、“减小”或“不变”).在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g)。其化学平衡常数K和温度T的关系如下表:
CO(g)+H2O(g)。其化学平衡常数K和温度T的关系如下表:
| T℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |

回答下列问题:
(1)该反应正向为ΔH 0;若该反应符合下图所示的关系,则在图中,Y轴是指 。
(2)能判断该反应达到化学平衡状态的依据是 (多选扣分)。
a.容器中压强不变 b.混合气体中c(CO)不变
c.v (H2)正=v (H2O)逆 d.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式: 0.9·c(CO2)·c(H2)=c(CO)·c(H2O),由此可以判断此时的温度为 ℃。其它条件不变,升高温度,原化学平衡向 反应方向移动(填“正”或“逆”
 ),容器内混合气体的密度 (填“增大”、“减小”或“不变”),气体平均相对分子质量 (填“增大”、“减小”或“不变”)。
),容器内混合气体的密度 (填“增大”、“减小”或“不变”),气体平均相对分子质量 (填“增大”、“减小”或“不变”)。(4)若在一密闭容器中,将一定量的CO与H2O混合加热到830℃下达到平衡。若反应开始时CO与H2O的浓度分别为0.200 mol/L和0.100 mol/L,平衡时CO的转化率 。 查看习题详情和答案>>
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g).其化学平衡常数K和温度T的关系如下表,回答下列问题:
(1)该反应正向为△H______0;若该反应符合如图所示的关系,则在图中,Y轴是指______. (答出一种即可)
(2)能判断该反应达到化学平衡状态的依据是______(多选扣分).
a.容器中压强不变 b.混合气体中c(CO)不变
c.v(H2)正=v(H2O)逆 d.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式:0.9?c(CO2)?c(H2)=c(CO)?c(H2O),由此可以判断此时的温度为______℃.其它条件不变,升高温度,原化学平衡向______反应方向移动(填“正”或“逆”),容器内混合气体的平均相对分子质量______(填“增大”、“减小”或“不变”).
 查看习题详情和答案>>
查看习题详情和答案>>
| T℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(2)能判断该反应达到化学平衡状态的依据是______(多选扣分).
a.容器中压强不变 b.混合气体中c(CO)不变
c.v(H2)正=v(H2O)逆 d.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式:0.9?c(CO2)?c(H2)=c(CO)?c(H2O),由此可以判断此时的温度为______℃.其它条件不变,升高温度,原化学平衡向______反应方向移动(填“正”或“逆”),容器内混合气体的平均相对分子质量______(填“增大”、“减小”或“不变”).
 查看习题详情和答案>>
查看习题详情和答案>>
一定温度下,向1.0L密闭容器中加入0.60molX(g),发生反应X(g)?Y(s)+2Z(g)△H>0测得反应物X浓度与反应时间的数据如下表
(1)3min时用Z表示的平均反应速率v(Z)= .
(2)分析该反应中反应物的浓度与时间的规律,得出的结论是 .由此规律推出反应在6min时反应物的浓度a为 mol?L-1.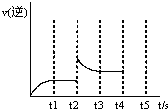
(3)反应的逆反应速率随时间变化的关系如图,t2时改变了某一种条件,改变的条件可能是 、 (填写两顶)
(4)下列哪些情况表明容器中已达平衡状态 (填字母序号)
A.容器体积一定时气体密度不再变化
B.反应的平衡常数不再变化
C.容器中气体的平均相对分子质量不随时间而变化
D.Y的物质的量不再发生变化
E.Z的生成速率等于X的消耗速率的2倍.
查看习题详情和答案>>
| 反应时间t/min | 0 | 1 | 2 | 3 | 4 | 6 | 8 |
| c(X)/(mol?L-1) | 0.60 | 0.42 | 0.30 | 0.21 | 0.15 | a | 0.0375 |
(2)分析该反应中反应物的浓度与时间的规律,得出的结论是

(3)反应的逆反应速率随时间变化的关系如图,t2时改变了某一种条件,改变的条件可能是
(4)下列哪些情况表明容器中已达平衡状态
A.容器体积一定时气体密度不再变化
B.反应的平衡常数不再变化
C.容器中气体的平均相对分子质量不随时间而变化
D.Y的物质的量不再发生变化
E.Z的生成速率等于X的消耗速率的2倍.
已知可逆反应:Fe(s) + CO2(g)![]() FeO(s) + CO(g),其温度与平衡常数K的关系如下表:
FeO(s) + CO(g),其温度与平衡常数K的关系如下表:
| T(K) | 938 | 1173 |
| K | 1.47 | 2.15 |
(1)写出该反应的平衡常数表达式____________________。
(2)若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,改变下列条件再达平衡后判断(选填“增大”、
“减小”、“不变”):
①升高温度,混合气体的平均相对分子质量_________;
②充入氦气,混合气体的密度__________。
(3)该反应的逆反应速率随时间变化情况如右图所示。
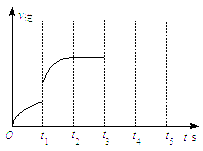
①从右图可知,在t1时改变了某种反应条件,反应在
t2时达到平衡,改变的条件可能是_______(选填编号)。
a.升高温度 b.增大CO2的浓度
c.减小CO2的浓度 d.使用催化剂
②如果在t3时增加CO2的量,t4时反应又处于新平衡状态,请在上图![]() 画出t3~ t5时间段的v逆变化曲线。
画出t3~ t5时间段的v逆变化曲线。
③能作为判断该反应达到平衡状态的依据是 (选填编号)。
a.v正(CO2)=v逆(CO) b.容器内气体总压强不再变化
c.容器内气体密度不再变化 d.使用催化剂后,正、逆反应速率同比例加快
查看习题详情和答案>>