网址:http://m.1010jiajiao.com/timu_id_3715189[举报]
氮有多种氧化物,其中N2O5是一种新型硝化剂,其性质和制备收到人们的关注。
(1)一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g)
 4NO2(g)+O2(g) ;⊿H>0
4NO2(g)+O2(g) ;⊿H>0
①反应达到平衡后,若再通入一定量氩气,则N2O5的转化率将___(填“增大”、“减小”、“不变”)。
②下表为反应在T1温度下的部分实验数据:
|
t/s |
0 |
500 |
1000 |
|
c(N2O5)/mol·L—1 |
5.00 |
3.52 |
2.48 |
则500s内N2O5的分解速率为______________。
③一定温度下,在2L恒容密闭容器中加入2mol
N2O5,达到平衡时,气体的压强为原来的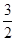 ,(不考虑NO2聚合成N2O4),则N2O5的转化率a1= ,该温度下反应的平衡常数K=_______。
,(不考虑NO2聚合成N2O4),则N2O5的转化率a1= ,该温度下反应的平衡常数K=_______。
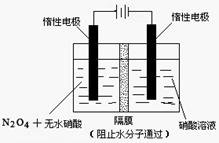
(2)如图所示装置可用于制备N2O5,则N2O5在电解池的__________区生成,其电极反应式为_________________________________。

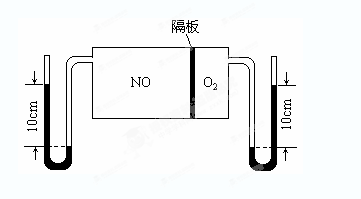
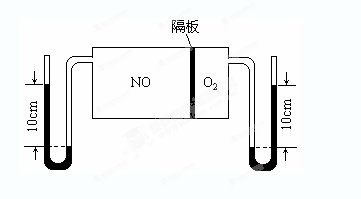
(3)如图:V(NO):V(O2)=3:1。当抽去NO和O2之间的隔板后,NO和O2反应后成NO2,部分NO2聚合成N2O4(N2O4此时为气态)。当体系达到平衡后,U形毛细管两端汞面高度差由反应前10cm变为7.1cm。假设温度不变,且隔板及U形毛细管的体积都忽略不计,此时混合气体的平均相对分子质量为__________。
查看习题详情和答案>>
氮有多种氧化物,其中N2O5是一种新型硝化剂,其性质和制备收到人们的关注。
(1)一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g) 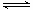 4NO2(g)+O2(g) ;⊿H>0
4NO2(g)+O2(g) ;⊿H>0
①反应达到平衡后,若再通入一定量氩气,则N2O5的转化率将___(填“增大”、“减小”、“不变”)。
②下表为反应在T1温度下的部分实验数据:
| t/s | 0 | 500 | 1000 |
| c(N2O5)/mol·L—1 | 5.00 | 3.52 | 2.48 |
③一定温度下,在2L恒容密闭容器中加入2mol N2O5,达到平衡时,气体的压强为原来的
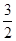 ,(不考虑NO2聚合成N2O4),则N2O5的转化率a1= ,该温度下反应的平衡常数K=_______。
,(不考虑NO2聚合成N2O4),则N2O5的转化率a1= ,该温度下反应的平衡常数K=_______。(2)如图所示装置可用于制备N2O5,则N2O5在电解池的__________区生成,其电极反应式为_________________________________。
(3)如图:V(NO):V(O2)=3:1。当抽去NO和O2之间的隔板后,NO和O2反应后成NO2,部分NO2聚合成N2O4(N2O4此时为气态)。当体系达到平衡后,U形毛细管两端汞面高度差由反应前10cm变为7.1cm。假设温度不变,且隔板及U形毛细管的体积都忽略不计,此时混合气体的平均相对分子质量为__________。
 查看习题详情和答案>>
查看习题详情和答案>>
 非金属元素氮有多种氧化物,如NO、NO2、N2O4等.
非金属元素氮有多种氧化物,如NO、NO2、N2O4等.(1)对反应N2O4(g)?2NO2(g),△H=+57kJ?mol-1在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.
下列说法正确的是
a.A、C两点的反应速率:A>C
b.B、C两点的气体的平均相对分子质量:B<C
c.A、C两点气体的颜色:A深,C浅
d.由状态B到状态A,可以用加热的方法
(2)在100℃时,将0.400mol的NO2气体充入2L抽空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
②已知100℃反应2NO2?N2O4的平衡常数K=2.8.若该温度下某时刻测得c(NO2)=1.00mol/L,c(N2O4)=0.20mol/L,则该时刻的v正
③若在相同情况下最初向该容器只充入的是N2O4气体,要达到上述同样的平衡状态,N2O4的起始浓度是
④计算在题③的条件下达到平衡后混合气体的平均相对分子质量为
(3)肼(N2H4)通常是航天航空的重要燃料,我们常用的一种肼燃料电池,是以肼与氧气的反应为原理设计的(N2H4+O2=N2+2H2O),其电解质溶液是KOH溶液.写出该电池负极的电极反应式
某研究性学习小组验证浓硝酸与铜银合金反应时除生成NO2气体外还会生成少量的NO气体。查阅资料得知:常温下NO2与N2O4混合存在,在低于0℃时几乎只有无色的N2O4液体或晶体存在。为此,他们设计了如下图所示的验证实验装置(图中略去了次要装置)
![]()

![]() 请回答下列问题:
请回答下列问题:
![]() (1)写出A瓶中铜与硝酸可能发生的反应方程式:
(1)写出A瓶中铜与硝酸可能发生的反应方程式:
![]() 、 。
、 。
![]() (2)实验开始时要先打开A中的活塞K1,持续通一段时间的氮气再关闭K1,这样做的目的是 ;装置中B瓶的作用是 。
(2)实验开始时要先打开A中的活塞K1,持续通一段时间的氮气再关闭K1,这样做的目的是 ;装置中B瓶的作用是 。
![]() (3)A中的反应停止后,打开D中的活塞K2,并通入氧气,若反应确有NO气体产生,则D中应出现的现象是 ;实验发现,通入氧气温度的高低对实验现象有较大影响,为了便于观察应通入 (填“冷”或“热”)的氧气。
(3)A中的反应停止后,打开D中的活塞K2,并通入氧气,若反应确有NO气体产生,则D中应出现的现象是 ;实验发现,通入氧气温度的高低对实验现象有较大影响,为了便于观察应通入 (填“冷”或“热”)的氧气。
![]() (4)已知合金的质量为ag,且合金完全溶解。若还想测定铜的质量分数,只需利用A装置中反应后的溶液进行简单的实验操作就可以过到目的,其实验过程为: 。
(4)已知合金的质量为ag,且合金完全溶解。若还想测定铜的质量分数,只需利用A装置中反应后的溶液进行简单的实验操作就可以过到目的,其实验过程为: 。
(11分)某研究性学习小组验证浓硝酸与铜银合金反应时除生成NO2气体外还会生成少量的NO气体。查阅资料得知:常温下NO2与N2O4混合存在,在低于0℃时几乎只有无色的N2O4液体或晶体存在。为此,他们设计了如下图所示的验证实验装置(图中略去了次要装置)
请回答下列问题:
(1)写出A瓶中铜与硝酸可能发生的反应方程式:
、 。
(2)实验开始时要先打开A中的活塞K1,持续通一段时间的氮气再关闭K1,这样做的目的是 ;装置中B瓶的作用是 。
(3)A中的反应停止后,打开D中的活塞K2,并通入氧气,若反应确有NO气体产生,则D中应出现的现象是 ;实验发现,通入氧气温度的高低对实验现象有较大影响,为了便于观察应通入 (填“冷”或“热”)的氧气。
(4)已知合金的质量为ag,且合金完全溶解。若还想测定铜的质量分数,只需利用A装置中反应后的溶液进行简单的实验操作就可以过到目的,其实验过程为: 。
查看习题详情和答案>>