摘要:13.下列有关气态氢化物某些性质的归纳正确的是( ) ①H2S.H2Se在水中的溶解度较小.CH4.SiH4.C2H2不溶于水 ②HF最稳定.SiH4较稳定 ③NH3.H2Se.H2Te能在纯氧中燃烧.常温下SiH4能自燃 ④H2S.HI还原性较弱.NH3.HBr还原性较强 ⑤H2S.HF溶液的导电性较弱 A.①③ B.③④ C.②④⑤ D.①③⑤
网址:http://m.1010jiajiao.com/timu_id_3715151[举报]
原子序数依次增大的主族元素A、B、C、D分别处于第一至第四周期,其中A原子核是一个质子;B原子核外电子有6种不同的运动状态,B与C可形成正四面体型分子,D原子外围电子排布为3d104s1. 回答下列问题:
(1)这四种元素中电负性最大的是
(2)C所在的主族元素气态氢化物中,沸点最低的是
(3)B元素可形成多种单质,其中“只有一层原子厚”的物质,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,该材料晶体 结构如图所示,其原子的杂化类型为
(4)D的水合醋酸盐晶体局部结构如图,该晶体中含有的化学键是
①极性键 ②非极性键 ③配位键 ④金属键
(5)某学生所做的有关D元素的实验流程如图:
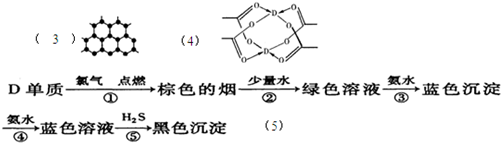
请书写第⑤反应的离子方程式:
查看习题详情和答案>>
(1)这四种元素中电负性最大的是
Cl
Cl
(填元素符号)、第一电离能最小的是Cu
Cu
(填元素符号);(2)C所在的主族元素气态氢化物中,沸点最低的是
HCl
HCl
(填化学式);(3)B元素可形成多种单质,其中“只有一层原子厚”的物质,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,该材料晶体 结构如图所示,其原子的杂化类型为
sp2
sp2
;(4)D的水合醋酸盐晶体局部结构如图,该晶体中含有的化学键是
①②③
①②③
;①极性键 ②非极性键 ③配位键 ④金属键
(5)某学生所做的有关D元素的实验流程如图:

请书写第⑤反应的离子方程式:
〔Cu(NH3)4〕2++H2S+2H2O=CuS↓+2NH4++2NH3?H2O
〔Cu(NH3)4〕2++H2S+2H2O=CuS↓+2NH4++2NH3?H2O
.(2011?奉贤区一模)A、B、C、D、E为五种短周期元素,其中A、B、C位于同一周期,A元素的气态氢化物是一种广泛应用的优质气体燃料,B元素的氢化物是用途最为广泛的溶剂.B元素可分别与A、C、D、E组成RB2型化合物.已知在DB2中,D与B的质量比为7:8;在EB2中,E与B的质量比为1:1.根据以上条件回答下列问题:
(1)请写出C单质分子的电子式
 ;DB2晶体中化学键的类型为
;DB2晶体中化学键的类型为
(2)C的气态氢化物易液化,原因是:
(3)C和D结合可生成一种超硬物质,有关该物质性质的叙述中不正确的是
①有润滑性 ②易磨损 ③抗腐蚀 ④强还原性 ⑤抗冷热
(4)B元素可分别与A、E形成多种阴离子.某溶液是由其中若干种阴离子组成的无机钠盐溶液,为了检验该溶液中的阴离子,分别取两份溶液进行如下实验:
①第一份溶液中加入足量盐酸,只产生无色气体;
②第二份溶液中加入足量的BaCl2溶液,有白色沉淀产生,再加入足量稀硝酸,白色沉淀质量减少.
由此得出的结论是
查看习题详情和答案>>
(1)请写出C单质分子的电子式


(极性)共价键
(极性)共价键
;写出AE2的结构式S=C=S
S=C=S
.(2)C的气态氢化物易液化,原因是:
氨气分子之间存在有氢键,使其沸点较高
氨气分子之间存在有氢键,使其沸点较高
.(3)C和D结合可生成一种超硬物质,有关该物质性质的叙述中不正确的是
①②④
①②④
.①有润滑性 ②易磨损 ③抗腐蚀 ④强还原性 ⑤抗冷热
(4)B元素可分别与A、E形成多种阴离子.某溶液是由其中若干种阴离子组成的无机钠盐溶液,为了检验该溶液中的阴离子,分别取两份溶液进行如下实验:
①第一份溶液中加入足量盐酸,只产生无色气体;
②第二份溶液中加入足量的BaCl2溶液,有白色沉淀产生,再加入足量稀硝酸,白色沉淀质量减少.
由此得出的结论是
一定有CO32-,SO32-和SO42-至少有一种
一定有CO32-,SO32-和SO42-至少有一种
.