摘要:2 FeCl3 2 Fe3++Fe= 3Fe2+
网址:http://m.1010jiajiao.com/timu_id_3714805[举报]
回答下列关于铁元素及其化合物的知识:
(1)向一支装有FeCl3溶液的试管中滴加NaOH溶液,现象为
(2)为了检验某未知溶液是否含有Fe2+离子,两位同学分别设计了以下实验方案加以证明.方案一:向一支装有该未知溶液的试管中先通入氯气,再滴加KSCN溶液,溶液呈现红色,证明该未知溶液含有Fe2+离子;
方案二:向另一支装有该未知溶液的试管中先滴加KSCN溶液,无现象,再通入氯气,溶液变为红色,证明该未知溶液含有Fe2+离子;
则请回答:①你认为哪个方案较为合理
②写出Fe2+与氯气反应的离子方程式
③实验室在保存含有Fe2+离子的溶液时,为了防止Fe2+离子变质,经常向其中加入铁粉,
其原因是(用离子方程式表示)
(3)鲜榨苹果汁是人们喜爱的饮料.由于此饮料中含有Fe2+,鲜榨的苹果汁在空气中会由淡绿色的Fe2+变为棕黄色的Fe3+,则这个变色的过程中Fe2+被
A.氧化性 B.还原性 C.酸性 D.碱性.
查看习题详情和答案>>
(1)向一支装有FeCl3溶液的试管中滴加NaOH溶液,现象为
生成红褐色沉淀
生成红褐色沉淀
,其中含铁元素的产物的化学式是Fe(OH)3
Fe(OH)3
;(2)为了检验某未知溶液是否含有Fe2+离子,两位同学分别设计了以下实验方案加以证明.方案一:向一支装有该未知溶液的试管中先通入氯气,再滴加KSCN溶液,溶液呈现红色,证明该未知溶液含有Fe2+离子;
方案二:向另一支装有该未知溶液的试管中先滴加KSCN溶液,无现象,再通入氯气,溶液变为红色,证明该未知溶液含有Fe2+离子;
则请回答:①你认为哪个方案较为合理
方案二
方案二
;②写出Fe2+与氯气反应的离子方程式
2Fe2++Cl2═2Fe3++2Cl-
2Fe2++Cl2═2Fe3++2Cl-
;③实验室在保存含有Fe2+离子的溶液时,为了防止Fe2+离子变质,经常向其中加入铁粉,
其原因是(用离子方程式表示)
2Fe3++Fe═3Fe2+
2Fe3++Fe═3Fe2+
(3)鲜榨苹果汁是人们喜爱的饮料.由于此饮料中含有Fe2+,鲜榨的苹果汁在空气中会由淡绿色的Fe2+变为棕黄色的Fe3+,则这个变色的过程中Fe2+被
氧化
氧化
;若在榨汁的时候加入适量的维生素C,可有效防止这种现象的发生.这说明维生素C具有B
B
.A.氧化性 B.还原性 C.酸性 D.碱性.
(2012?东城区二模)SO2随意排放会造成严重的大气污染.下列是某小组同学设计处理烟气(主要含SO2、N2、O2、粉尘)中SO2的方法.
(1)方法一:利用氯碱工业产品处理含SO2的烟气,流程如下:
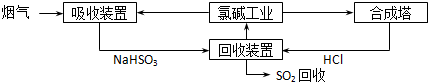
①“吸收装置”中发生反应的离子方程式是
②合成塔中每合成1mol 气体放出热量92.3kJ(25℃、101kPa),反应的热化学方程式是
③上述流程中循环利用的物质是
(2)方法二:利用FeCl3溶液的氧化性吸收烟气中的SO2.
①该反应的离子方程式是
②利用胶体的
③根据反应b,说明步骤ⅱ中液体颜色变化的原因是
④经讨论后得出结论:FeCl3溶液和SO2反应过程中,反应a、b在体系中共存.请从化学反应速率和反应限度的角度分析,SO2通入FeCl3溶液中产生上述现象的原因是
查看习题详情和答案>>
(1)方法一:利用氯碱工业产品处理含SO2的烟气,流程如下:

①“吸收装置”中发生反应的离子方程式是
SO2+OH-=HSO3-
SO2+OH-=HSO3-
;②合成塔中每合成1mol 气体放出热量92.3kJ(25℃、101kPa),反应的热化学方程式是
H2(g)+Cl2(g)=2HCl(g)△H=-184.6 kJ?mol-1
H2(g)+Cl2(g)=2HCl(g)△H=-184.6 kJ?mol-1
;③上述流程中循环利用的物质是
NaCl溶液
NaCl溶液
.(2)方法二:利用FeCl3溶液的氧化性吸收烟气中的SO2.
①该反应的离子方程式是
2Fe3++SO2+2H2O=2Fe2++SO42-+4H+
2Fe3++SO2+2H2O=2Fe2++SO42-+4H+
(反应a).为验证该反应,同学们将SO2通入0.05mol?L-1 FeCl3溶液中,溶液很快由黄色变为红褐色;将溶液长时间放置后,最终变为浅绿色.关于红褐色液体,以下是同学们的分析推测与实验.| 分析推测 | 实验步骤 | ||
| 甲:生成了Fe(OH)3胶体 乙:经查阅资料,可能发生反应: Fe3++6SO2 Fe(SO2)
|
ⅰ.制备Fe(OH)3胶体并检验 ⅱ.分别向Fe(OH)3胶体和该红褐色液体中加入适量铁粉,振荡后前者不变色,后者变为浅绿色 |
丁达尔效应
丁达尔效应
(填性质)可以检验步骤ⅰ中是否得到了Fe(OH)3胶体;③根据反应b,说明步骤ⅱ中液体颜色变化的原因是
加入铁粉时发生反应2Fe3++Fe=3Fe2+,c(Fe3+)减小,使反应b逆向移动
加入铁粉时发生反应2Fe3++Fe=3Fe2+,c(Fe3+)减小,使反应b逆向移动
(用离子方程式及必要的文字说明);④经讨论后得出结论:FeCl3溶液和SO2反应过程中,反应a、b在体系中共存.请从化学反应速率和反应限度的角度分析,SO2通入FeCl3溶液中产生上述现象的原因是
由于化学反应速率:b>a,化学反应限度:a>b,所以产生上述现象
由于化学反应速率:b>a,化学反应限度:a>b,所以产生上述现象
.