摘要:按密度不同 按密度
网址:http://m.1010jiajiao.com/timu_id_3714717[举报]
 某同学利用下列装置实现铜与浓硝酸、稀硝酸反应,过程如图所示:
某同学利用下列装置实现铜与浓硝酸、稀硝酸反应,过程如图所示:I. 取一段铜丝,用稀硫酸除去铜锈[主要成分是Cu2(OH)2CO3].
Ⅱ.将洗涤后的铜丝做成匝数较多的螺旋状.
Ⅲ.按如图所示装置连接仪器、检查气密性、装入化学试剂.
(1)过程I发生反应的离子方程式是
Cu2(OH)2CO3+4H+═2Cu2++CO2↑+3H2O
Cu2(OH)2CO3+4H+═2Cu2++CO2↑+3H2O
.(2)写出过程Ⅲ中检查气密性的方法
打开b和a,关闭分液漏斗的活塞,将左边导管插入盛水的烧杯中,轻轻拉动注射器活塞,若导管中液面上升则说明气密性好
打开b和a,关闭分液漏斗的活塞,将左边导管插入盛水的烧杯中,轻轻拉动注射器活塞,若导管中液面上升则说明气密性好
.(3)过程Ⅲ的后续操作如下:
①打开止水夹a和b,轻推注射器,使浓硝酸与铜丝接触,观察到的现象是
产生红棕色气体
产生红棕色气体
,一段时间后使反应停止的操作是轻轻将注射器活塞向右拉使铜丝和溶液分开
轻轻将注射器活塞向右拉使铜丝和溶液分开
,关闭a,取下注射器.②打开b和分液漏斗活塞,当玻璃管充满稀硝酸后,关闭b和分液漏斗活塞,打开a,观察到有气泡产生.稀硝酸充满玻璃管的实验目是
将玻璃管中的NO2和空气排出
将玻璃管中的NO2和空气排出
,该反应的离子方程式是3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
.(4)另取3支盛满NO2气体的小试管分别倒置在盛有常温水、热水和冰水的3只烧杯中,发现液面上升的高度明显不一致.结果如表所示(忽略温度对气体体积的影响):
| 实验编号 | 水温/℃ | 液面上升高度 | ||
| 1 | 25 | 超过试管的
| ||
| 2 | 50 | 不足试管的
| ||
| 3 | 0 | 液面上升超过实验1 |
低
低
(填“高”或“低”),进入试管中的溶液越多.②查阅资料:
a.NO2与水反应的实际过程为:2NO2+H2O=HNO3+HNO2 3HNO2=HNO3+2NO↑+H2O;
b.HNO2不稳定.
则产生上述现象的原因是
温度低,HNO2分解量减少,分解产生的NO气体量减少,所以进入试管的溶液多
温度低,HNO2分解量减少,分解产生的NO气体量减少,所以进入试管的溶液多
.三种不同条件下,分别向容积固定的2L密闭容器中充入2molA和1mol B,发生反应如下:2A(g)+B(g)?2D(g)△H=akJ?mol-1,相关条件和数据见下表.
请回答:
(1)实验Ⅲ,反应进行到30min时的平均速率v (D)为
(2)实验Ⅱ可能隐含的反应条件是
(3)下列描述中能说明上述反应已达平衡的是
a.c(A)=2c(B) b.2v (D)正=v (B)逆
c.容器内气体密度不随时间而变化 d.容器内气体压强不随时间而变化
(4)对比上述实验,可知该反应的反应热a
(5)若实验Ⅰ达到平衡后,保持温度不变,再向密闭容器中通入1mol D组成的气体,则平衡将
查看习题详情和答案>>
| 实验Ⅰ | 实验Ⅱ | 实验Ⅲ | |
| 反应温度/℃ | 800 | 800 | 850 |
| 达平衡时间/min | 40 | 10 | 30 |
| c( D )平衡/mol?L-1 | 0.5 | 0.5 | 0.15 |
| 反应的能量变化/kJ | Q1 | Q2 | Q3 |
(1)实验Ⅲ,反应进行到30min时的平均速率v (D)为
0.005mol?L-1?min-1
0.005mol?L-1?min-1
.(2)实验Ⅱ可能隐含的反应条件是
使用(效率更高的)催化剂
使用(效率更高的)催化剂
.(3)下列描述中能说明上述反应已达平衡的是
d
d
(填序号).a.c(A)=2c(B) b.2v (D)正=v (B)逆
c.容器内气体密度不随时间而变化 d.容器内气体压强不随时间而变化
(4)对比上述实验,可知该反应的反应热a
<
<
0(填“>”或“<”),并将Q1、Q2、Q3按从小到大的顺序排列:Q3<Q1=Q2
Q3<Q1=Q2
.(5)若实验Ⅰ达到平衡后,保持温度不变,再向密闭容器中通入1mol D组成的气体,则平衡将
逆向
逆向
移动(填“正向”、“逆向”或“不”),新平衡状态时c(D)为大于
大于
0.5mol?L-1 (填“大于”、“小于”或“等于”). 某同学利用下面装置实现铜与浓、稀硝酸反应,过程如下:
某同学利用下面装置实现铜与浓、稀硝酸反应,过程如下:
Ⅰ、取一段铜丝,用稀硫酸除去铜锈〔主要成分是 Cu2(OH)2CO3〕
Ⅱ、将洗涤后的铜丝做成匝数很多的螺旋状
Ⅲ、按如图所示连接仪器、检查气密性、装入化学试剂
(1)过程Ⅰ发生反应的离子方程式是______;
(2)过程Ⅱ将铜丝做成螺旋状的目的是______;
(3)过程Ⅲ的后续操作如下:
①为使浓硝酸与铜丝接触,操作是______.当红棕色气体较多时,轻抽注射器使反应停止,关闭a,取下注射器.生成红棕色气体的化学方程式是______.
②控制b和分液漏斗活塞,玻璃管充满稀硝酸时,关闭b打开a,可见无色气体.稀硝酸充满玻璃管的实验目的是______.
(4)将3支盛满红棕色气体的小试管分别倒置在盛有常温水、热水和冰水的3只烧杯中,发现液面上升的高度明显不一致.结果如下表所示:
| 实验编号 | 水温/0C | 液面上升高度 |
| 1 | 25 | 超过试管 |
| 2 | 50 | 不足试管 |
| 3 | 0 | 液面上升超过实验1 |
②查阅资料:
a.NO2与水反应的实际过程为:2NO2+H2O═HNO2+HNO3 3HNO2═HNO3+2NO↑+H2O
b.HNO2不稳定.
产生上述现象的原因是______. 查看习题详情和答案>>
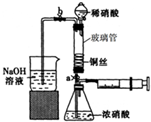 某同学利用下列装置实现铜与浓硝酸、稀硝酸反应,过程如图所示:
某同学利用下列装置实现铜与浓硝酸、稀硝酸反应,过程如图所示:
I. 取一段铜丝,用稀硫酸除去铜锈[主要成分是Cu2(OH)2CO3].
Ⅱ.将洗涤后的铜丝做成匝数较多的螺旋状.
Ⅲ.按如图所示装置连接仪器、检查气密性、装入化学试剂.
(1)过程I发生反应的离子方程式是______.
(2)写出过程Ⅲ中检查气密性的方法______.
(3)过程Ⅲ的后续操作如下:
①打开止水夹a和b,轻推注射器,使浓硝酸与铜丝接触,观察到的现象是______,一段时间后使反应停止的操作是______,关闭a,取下注射器.
②打开b和分液漏斗活塞,当玻璃管充满稀硝酸后,关闭b和分液漏斗活塞,打开a,观察到有气泡产生.稀硝酸充满玻璃管的实验目是______,该反应的离子方程式是______.
(4)另取3支盛满NO2气体的小试管分别倒置在盛有常温水、热水和冰水的3只烧杯中,发现液面上升的高度明显不一致.结果如表所示(忽略温度对气体体积的影响):
| 实验编号 | 水温/℃ | 液面上升高度 |
| 1 | 25 | 超过试管的 |
| 2 | 50 | 不足试管的 |
| 3 | 0 | 液面上升超过实验1 |
②查阅资料:
a.NO2与水反应的实际过程为:2NO2+H2O=HNO3+HNO2 3HNO2=HNO3+2NO↑+H2O;
b.HNO2不稳定.
则产生上述现象的原因是______. 查看习题详情和答案>>
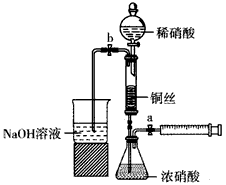
某同学利用下面装置实现铜与浓、稀硝酸的反应,过程如下:
I.取一段铜丝,用稀硫酸除去铜锈[主要成分是Cu2(OH)2CO3]。
Ⅱ.将洗涤后的铜丝做成匝数较多的螺旋状。
Ⅲ.按下图所示连接仪器,检查气密性,装入化学试剂。
I.取一段铜丝,用稀硫酸除去铜锈[主要成分是Cu2(OH)2CO3]。
Ⅱ.将洗涤后的铜丝做成匝数较多的螺旋状。
Ⅲ.按下图所示连接仪器,检查气密性,装入化学试剂。
(1)过程I发生反应的离子方程式是____________________。
(2)过程Ⅱ将铜丝做成螺旋状的目的是________________。
(3)过程Ⅲ的后续操作如下:
①为使浓硝酸与铜丝接触,操作是___________。当红棕色气体较多时,轻抽注射 器使反应停止,关闭a,取下注射器。生成红棕色气体的化学反应方程式是____________________。
②控制b和分液漏斗活塞,玻璃管充满稀硝酸时,关闭b打开a,可见无色气体产生。稀硝酸充满玻璃管的实验目的是___________。
(4)将3支盛满红棕色气体的小试管分别倒置在盛有常温水、热水和冰水的3只烧杯中,发现液面上升的高度明显不一致。结果如下表所示:
(2)过程Ⅱ将铜丝做成螺旋状的目的是________________。
(3)过程Ⅲ的后续操作如下:
①为使浓硝酸与铜丝接触,操作是___________。当红棕色气体较多时,轻抽注射 器使反应停止,关闭a,取下注射器。生成红棕色气体的化学反应方程式是____________________。
②控制b和分液漏斗活塞,玻璃管充满稀硝酸时,关闭b打开a,可见无色气体产生。稀硝酸充满玻璃管的实验目的是___________。
(4)将3支盛满红棕色气体的小试管分别倒置在盛有常温水、热水和冰水的3只烧杯中,发现液面上升的高度明显不一致。结果如下表所示:
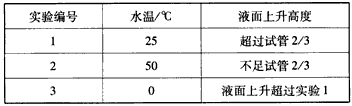
①根据上表得出的结论是_______________。
②查阅资料:
a.NO2与水反应的实际过程为2NO2+H2O=HNO3+HNO2、3HNO2=HNO3+2NO↑+H2O
b.HNO2不稳定。
产生上述现象的原因是_______________________。
查看习题详情和答案>>
②查阅资料:
a.NO2与水反应的实际过程为2NO2+H2O=HNO3+HNO2、3HNO2=HNO3+2NO↑+H2O
b.HNO2不稳定。
产生上述现象的原因是_______________________。