网址:http://m.1010jiajiao.com/timu_id_3714424[举报]
Ⅰ、写出精炼粗铜过程中阳极上发生的电极反应
Ⅱ、精炼过程中需定时除去其中的Fe2+、Zn2+.下表为部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| 开始沉淀 | 2.3 | 7.5 | 5.6 | 6.2 |
| 完全沉淀 | 3.9. | 9.7 | 6.4 | 8.0 |
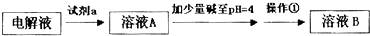
(1)试剂a是
(2)乙同学在查阅资料时发现,“工业原料氯化铵中含杂质氯化铁,使其溶入水,再加入氨水调节pH至7~8,可使Fe3+生成Fe(OH)3沉淀而除去.”乙同学认为甲同学的方案中也应该将溶液pH调至7~8,你认为乙同学的建议是否正确?
粗铜精炼后的阳极泥含有Cu、Au(金)和PbSO4等杂质,湿法处理阳极泥进行综合利用的流程如下:
(1)用CuSO4做电解液电解含铜、金、铅的粗铜,阳极的电极反应式有: 和Cu-2e-= Cu2+。
(2)焙烧阳极泥时,为了提高焙烧效率,采取的合理措施是 ,焙烧后的阳极泥中除含金、PbSO4外,还有 (填化学式)。
(3)操作I的主要步骤为 ,操作Ⅱ的名称是 。
(4)写出用SO2还原AuCl4-的离子方程式 。
(5)为了减少废液排放、充分利用有用资源,工业上将滤液1并入硫酸铜溶液进行循环操作,请指出流程图中另一处类似的做法 。
(6)已知298K时,Ksp(PbCO3)=1.46×10-13,Ksp(PbSO4)= 1.82×10-8,用离子方程式表示加入碳酸钠溶液的作用 。

(1)X的电极名称是 (填写“阳极”或“阴极”).
(2)若要用该装置电解精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是 ,Y电极的材料是 .
(3)若X、Y都是惰性电极,a是饱和食盐水,实验开始时,同时在两边各滴入几滴酚酞试液,一段时间后,在X极附近观察到的现象是 ,Y极上的电极反应式为 .
(4)若要用电镀方法在铁表面镀一层金属银,应该选择的方案是 .
| 方案 | X | Y | a溶液 |
| A | 银 | 石墨 | AgNO3 |
| B | 银 | 铁 | AgNO3 |
| C | 铁 | 银 | Fe(NO3)3 |
| D | 铁 | 银 | AgNO3 |
电解原理在化学工业中有广泛的应用.如图表示一个电解池.装有电解液c;A、B分别是两块电极板,通过导线与直流电源相连.

(1)若A、B都是惰性电极,电解质溶液c是饱和NaCl溶液,实验开始时,同时在U形管两边各滴入几滴酚酞试液,试判断:
①a是________极(填“正”或“负”),B是________极(填“阴”或“阳”);
②A电极上的电极反应式为________,
B电极上的电极反应式为________;
③检验A电极产物的方法是________.
(2)如用电解法精炼粗铜,电解液c选用CuSO4溶液,则:
①A电极的材料是________,电极反应式为________;
②B电极的材料是________,电极反应式为________.
(12分)电解原理在化学工业中有广泛应用。右图表示一个电解池,其中a为电解质溶液, X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:(1)X的电极名称是 (填写“阳极”或“阴极”)。

(2)若X、Y都是惰性电极,a是饱和食盐水,实验开始时,
同时在两边各滴入几滴酚酞试液,一段时间后,在X极附近
观察到的现象是 ,Y极上的电极反应为 。
(3)若X、Y都是惰性电极,a是CuSO4溶液,电解一段时间后,阳极上产生气体的体积为0.224L(标准状况下),则阴极上析出金属的质量为 g。
(4)若要用该装置电解精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是 ,Y电极的材料是 。
(5)若要用电镀方法在铁表面镀一层金属银,应该选择的方案是 。
| 方案 | X | Y | a溶液 |
| A | 银 | 石墨 | AgNO3 |
| B | 银 | 铁 | AgNO3 |
| C | 铁 | 银 | Fe(NO3)3 |
| D | 铁 | 银 | AgNO3 |
查看习题详情和答案>>