摘要:应用:电解的离子方程式为2Cl-+2H2O2OH-+H2↑+Cl2↑.阴极产物是H2和NaOH.阴极被电解的H+是由水电离产生的.故阴极水的电离平衡被破坏.阴极区溶液呈碱性.若在阴极区附近滴几滴酚酞试液.可发现阴极区附近溶液变红.阳极产物是氯气.将湿润的KI淀粉试纸放在阳极附近.试纸变蓝.
网址:http://m.1010jiajiao.com/timu_id_3714421[举报]
下列关于烧碱的制备、性质及其应用的表述错误的是( )
A.电解饱和食盐水制烧碱的离子方程式为:2Cl-+2H2O 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
B.1807年英国科学家戴维通过电解熔融烧碱在阴极获得金属钠
C.向石灰乳中加入纯碱是工业上制备烧碱的方法之一
D.不慎将酸沾到皮肤上,要立即用大量水冲洗,然后涂上烧碱溶液
查看习题详情和答案>>
A.电解饱和食盐水制烧碱的离子方程式为:2Cl-+2H2O
 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑B.1807年英国科学家戴维通过电解熔融烧碱在阴极获得金属钠
C.向石灰乳中加入纯碱是工业上制备烧碱的方法之一
D.不慎将酸沾到皮肤上,要立即用大量水冲洗,然后涂上烧碱溶液
查看习题详情和答案>>
钛(Ti )被称为继铁、铝之后的第三金属.如下图所示,将钛厂、氯碱厂和甲醇厂组成产业链可以大大提高资源利用率,减少环境污染.请填写下列空白:
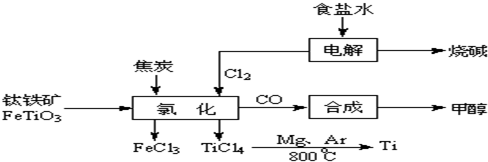
(l)电解饱和食盐水时,总反应的离子方程式是
(2)写出钛铁矿经氯化法得到四氯化钛的化学方程式(不用写条件)
(3)已知:①Mg(s)+Cl2(g)=MgCl2(s)△H=-641kJ?mol-1
②Ti(s)+2Cl2(g)=TiCl4(s)△H=-770kJ?mol-1
则2Mg(s)+TiCl4(s)=2MgCl2(s)+Ti(s)△H=
反应2Mg(s)+TiCl4(s) 2MgCl2(s)+Ti,在Ar气氛中进行的理由是:
2MgCl2(s)+Ti,在Ar气氛中进行的理由是:
(4)在上述产业链中,合成96t 甲醇理论上需额外补充H2
(5)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池.已知该燃料电池的总反应式为:2CH3OH+3O2+4OH-=2CO32-+6H2O,正极发生的电极方程式为:3O2+6H2O+12e-=12OH-.该电池中负极上的电极反应式是
查看习题详情和答案>>

(l)电解饱和食盐水时,总反应的离子方程式是
2Cl-+2H2O 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑2Cl-+2H2O 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
. 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑(2)写出钛铁矿经氯化法得到四氯化钛的化学方程式(不用写条件)
2FeTiO3+6C+7Cl2=2FeCl3+2TiCl4+6CO
2FeTiO3+6C+7Cl2=2FeCl3+2TiCl4+6CO
.(3)已知:①Mg(s)+Cl2(g)=MgCl2(s)△H=-641kJ?mol-1
②Ti(s)+2Cl2(g)=TiCl4(s)△H=-770kJ?mol-1
则2Mg(s)+TiCl4(s)=2MgCl2(s)+Ti(s)△H=
-512kJ/mol
-512kJ/mol
.反应2Mg(s)+TiCl4(s)
 2MgCl2(s)+Ti,在Ar气氛中进行的理由是:
2MgCl2(s)+Ti,在Ar气氛中进行的理由是:Mg和Ti都有强还原性,在Ar气氛中可以防止被氧化.
Mg和Ti都有强还原性,在Ar气氛中可以防止被氧化.
.(4)在上述产业链中,合成96t 甲醇理论上需额外补充H2
5
5
t (不考虑生产过程中物质的任何损失).(5)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池.已知该燃料电池的总反应式为:2CH3OH+3O2+4OH-=2CO32-+6H2O,正极发生的电极方程式为:3O2+6H2O+12e-=12OH-.该电池中负极上的电极反应式是
2CH3OH-12e-+16OH-=2CO32-+12H2O
2CH3OH-12e-+16OH-=2CO32-+12H2O
.