摘要:PbS+4H2O2=PbSO4+4H2O 讲析:21.根据氧化能力.Cl2将I2继续氧化成IO3-.
网址:http://m.1010jiajiao.com/timu_id_3713129[举报]
 碳是形成化合物最多的元素.
碳是形成化合物最多的元素.(1)由碳元素参与形成的物质多为分子晶体,也有少数原子晶体.下列关于分子晶体和原子晶体的说法正确的是
A、完全由非金属元素形成的物质一定是分子晶体或原子晶体
B、分子晶体中分子之间一定存在范德华力
C、SiC具有极高的熔点和较大的硬度,SiC分子中除存在共价键外,还存在分子间作用力
D、金刚石是由碳元素形成的原子晶体,性质稳定,不与任何物质反应
(2)意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的C4分子.C4分子结构如图所示.下列说法正确的是
A、C4属于一种新型的化合物 B、C4与P4(白磷)的晶体都属于分子晶体
C、C4气体分子内含有极性共价键 D、C4与C60互为同素异形
(3)与碳同主族元素锗为32号元素,与锗同周期,且未成对电子数与锗相同,电负性最大的元素的价电子排布式为
(4)邻硝基苯酚的熔点
(5)硼、碳、氮、氧是元素周期表第二周期相邻的四种元素.下列有关的四种化合
物中,键角最小的是
A、CO2 B、CF4 C、NF3 D、OF2
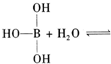
已知硼酸H3BO3为白色固体,溶于水显弱酸性,但它却是一元酸,可以用硼酸在水溶液中的电离平衡解释它是一元弱酸的原因.
请写出下面这个方程式右端的两种离子的表达式:
 查看习题详情和答案>>
查看习题详情和答案>>
 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示:(1)25°C时,水的电离平衡曲线应为哪一条?请说明理由
A 水的电离是吸热过程,温度低时,电离程度小,c(H+)、c(OH-)小
A 水的电离是吸热过程,温度低时,电离程度小,c(H+)、c(OH-)小
(2)95°C时,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,若所得混合溶液的pH=7,则NaOH溶液与硫酸溶液的体积比为为多少?
(3)95°C时,若10体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是?
(4)曲线B对应的温度下,pH=2的某酸HA与pH=10的NaOH溶液等体积混合后,溶液的pH=5,请分析其原因
曲线B对应95℃,此时水的离子积为10-12,HA若为强酸,最后应为pH=6,现pH=5,说明HA为弱酸,HA中和NaOH后,混合溶液中还剩余较多的HA分子,可继续电离出H+
曲线B对应95℃,此时水的离子积为10-12,HA若为强酸,最后应为pH=6,现pH=5,说明HA为弱酸,HA中和NaOH后,混合溶液中还剩余较多的HA分子,可继续电离出H+
.复分解反应存在这样一个规律:较强酸可制取较弱酸.中和反应、盐类的水解也是复分解反应,盐类的水解反应的逆反应是中和反应.盐类的水解反应中,弱酸强碱盐中弱酸根离子对应的弱酸越弱,其盐越容易发生水解.
已知在常温下测得浓度均为0.1mol/L的下列6种溶液的pH:
(1)请根据上述信息判断下列反应不能发生的是
A.CO2+H2O+2NaClO═Na2CO3+2HClO
B.CO2+H2O+NaClO═NaHCO3+HClO
C.CO2+H2O+C6H5ONa-→NaHCO3+C6H5OH
D.CO2+H2O+2C6H5ONa-→Na2CO3+2C6H5OH
E.Na2CO3+C6H5OH-→NaHCO3+C6H5ONa
F.CH3COOH+NaCN═CH3COONa+HCN
(2)一些复分解反应的发生还遵循其他的规律.下列变化都属于复分解反应:
①将石灰乳与纯碱溶液混合可制得苛性钠溶液
②向饱和碳酸氢铵溶液中加入饱和食盐水可获得小苏打固体
③蒸发KCl和NaNO3的混合溶液,首先析出NaCl晶体.
根据上述反应,总结出复分解反应发生的另一规律为
(3)物质的量浓度均为0.05mol/L的下列五种物质的溶液中,pH由大到小的顺序是
①C6H5OH(苯酚) ②CH3COOH ③HClO4 ④HClO ⑤H2SO4
(4)一定温度下,向等体积纯水中分别加入等物质的量的下列物质:①NaOH、②CH3COOH、③NaClO,则水的电离程度最大的是
(5)25℃时,M酸溶液的pH=a,N碱溶液的pH=b.
①若X为强酸,Y为强碱,且a+b=14,若两者等体积混合后,溶液的pH=
②若X的化学式为HR,Y的化学式为MOH,且a+b=14,两者等体积混合后溶液显酸性,则混合溶液中必定有一种离子能发生水解,该离子为
a c(MOH)>c(M+)>c(R-)>c(H+)>c(OH-)
b c(HR)>c(M+)>c(R-)>c(OH-)>c(H+)
c c(R-)>c(M+)>c(H+)>c(OH-)
d c(M+)>c(R-)>c(OH-)>c(H+)
e c(M+)+c(H+)=c(R-)+c(OH-)
查看习题详情和答案>>
已知在常温下测得浓度均为0.1mol/L的下列6种溶液的pH:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 8.1 | 11.6 | 10.3 | 11.1 | 11.3 |
AD
AD
(填编号).A.CO2+H2O+2NaClO═Na2CO3+2HClO
B.CO2+H2O+NaClO═NaHCO3+HClO
C.CO2+H2O+C6H5ONa-→NaHCO3+C6H5OH
D.CO2+H2O+2C6H5ONa-→Na2CO3+2C6H5OH
E.Na2CO3+C6H5OH-→NaHCO3+C6H5ONa
F.CH3COOH+NaCN═CH3COONa+HCN
(2)一些复分解反应的发生还遵循其他的规律.下列变化都属于复分解反应:
①将石灰乳与纯碱溶液混合可制得苛性钠溶液
②向饱和碳酸氢铵溶液中加入饱和食盐水可获得小苏打固体
③蒸发KCl和NaNO3的混合溶液,首先析出NaCl晶体.
根据上述反应,总结出复分解反应发生的另一规律为
反应能够由溶解度相对较大的物质向生成溶解度相对较小的物质的方向进行
反应能够由溶解度相对较大的物质向生成溶解度相对较小的物质的方向进行
.(3)物质的量浓度均为0.05mol/L的下列五种物质的溶液中,pH由大到小的顺序是
①④②③⑤
①④②③⑤
(填编号).①C6H5OH(苯酚) ②CH3COOH ③HClO4 ④HClO ⑤H2SO4
(4)一定温度下,向等体积纯水中分别加入等物质的量的下列物质:①NaOH、②CH3COOH、③NaClO,则水的电离程度最大的是
③
③
(填编号).(5)25℃时,M酸溶液的pH=a,N碱溶液的pH=b.
①若X为强酸,Y为强碱,且a+b=14,若两者等体积混合后,溶液的pH=
7
7
,此时溶液中金属阳离子浓度大于酸根阴离子浓度,其原因可能是酸为二元强酸,碱为一元强碱
酸为二元强酸,碱为一元强碱
.②若X的化学式为HR,Y的化学式为MOH,且a+b=14,两者等体积混合后溶液显酸性,则混合溶液中必定有一种离子能发生水解,该离子为
R-
R-
(填离子符号);混合后的溶液中,下列微粒浓度大小关系正确的是c e
c e
(填序号).a c(MOH)>c(M+)>c(R-)>c(H+)>c(OH-)
b c(HR)>c(M+)>c(R-)>c(OH-)>c(H+)
c c(R-)>c(M+)>c(H+)>c(OH-)
d c(M+)>c(R-)>c(OH-)>c(H+)
e c(M+)+c(H+)=c(R-)+c(OH-)
(2012?宜春模拟)一般较强酸可制取较弱酸,这是复分解反应的规律之一.已知在常温下测得浓度均为0.1mol/L的下列6种溶液的pH:
(1)①请根据上述信息判断下列反应不能发生的是
A.CH3COOH+NaCN═CH3COONa+HCN
B.CO2+H2O+2NaClO═Na2CO3+2HClO
C.2HCN+Na2CO3-→2NaCN+CO2+H2O
D.Na2CO3+C6H5OH-→NaHCO3+C6H5ONa
E.CO2+H2O+C6H5ONa-→NaHCO3+C6H5OH
②已知HA、H2B是两种弱酸,存在以下关系:H2B(少量)+2A-=B2-+2HA,则A-、B2-、HB-三种阴离子结合H+的难易顺序为
(2)一些复分解反应的发生还遵循其他规律.下列变化都属于复分解反应:
①将石灰乳与纯碱溶液混合可制得苛性钠溶液 ②向饱和碳酸氢铵溶液中加入饱和食盐水可获得小苏打固体 ③蒸发KCl和NaNO3的混合溶液,首先析出NaCl晶体.根据上述反应,总结出复分解反应发生的另一规律为
(3)常温下某电解质溶解在水中后,溶液中的c(H+)=10-9mol?L-1,则该电解质可能是
A. CuSO4 B. HCl C. Na2S D.NaOH E.K2SO4
(4)常温下,将pH=3的盐酸a L分别与下列三种溶液混合,结果溶液均呈中性.
①浓度为1.0×l0-3mol.L-1的氨水b L;
②c(OH -)=1.0×10-3mol.L-l的氨水c L;
③c(OH-)=1.0×10-3mol?L-1的氢氧化钡溶液d L.
则a、b、c、d之间由大到小的关系是:
(5)一定温度下,向等体积等物质的量浓度的下列三份溶液:①NaOH、②CH3COOH、③CH3COONa分别加等量水,pH变化最小的是
(6)己知常温时Ksp(AgCl)=1.8×10-10mol2?L-2,向50mL 0.018mol?L-1的AgNO3溶液中加入相同体积0.020mol?L-1的盐酸,则c(Ag+)=
查看习题详情和答案>>
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.1 | 8.8 | 11.6 | 10.3 | 11.1 | 11.3 |
BC
BC
(填编号).A.CH3COOH+NaCN═CH3COONa+HCN
B.CO2+H2O+2NaClO═Na2CO3+2HClO
C.2HCN+Na2CO3-→2NaCN+CO2+H2O
D.Na2CO3+C6H5OH-→NaHCO3+C6H5ONa
E.CO2+H2O+C6H5ONa-→NaHCO3+C6H5OH
②已知HA、H2B是两种弱酸,存在以下关系:H2B(少量)+2A-=B2-+2HA,则A-、B2-、HB-三种阴离子结合H+的难易顺序为
A->B2->HB-
A->B2->HB-
.(2)一些复分解反应的发生还遵循其他规律.下列变化都属于复分解反应:
①将石灰乳与纯碱溶液混合可制得苛性钠溶液 ②向饱和碳酸氢铵溶液中加入饱和食盐水可获得小苏打固体 ③蒸发KCl和NaNO3的混合溶液,首先析出NaCl晶体.根据上述反应,总结出复分解反应发生的另一规律为
由溶解度相对较大的物质向生成溶解度相对较小的物质的方向进行
由溶解度相对较大的物质向生成溶解度相对较小的物质的方向进行
.(3)常温下某电解质溶解在水中后,溶液中的c(H+)=10-9mol?L-1,则该电解质可能是
CD
CD
(填序号).A. CuSO4 B. HCl C. Na2S D.NaOH E.K2SO4
(4)常温下,将pH=3的盐酸a L分别与下列三种溶液混合,结果溶液均呈中性.
①浓度为1.0×l0-3mol.L-1的氨水b L;
②c(OH -)=1.0×10-3mol.L-l的氨水c L;
③c(OH-)=1.0×10-3mol?L-1的氢氧化钡溶液d L.
则a、b、c、d之间由大到小的关系是:
b>a=d>c
b>a=d>c
.(5)一定温度下,向等体积等物质的量浓度的下列三份溶液:①NaOH、②CH3COOH、③CH3COONa分别加等量水,pH变化最小的是
③
③
(填编号).一定温度下,向等体积纯水中分别加入等物质的量的CH3COONa和NaCN,两溶液中阴离子的总物质的量分别为n1和n2,则n1和n2的关系为n1>
>
n2(填“>”、“<”或“=”).(6)己知常温时Ksp(AgCl)=1.8×10-10mol2?L-2,向50mL 0.018mol?L-1的AgNO3溶液中加入相同体积0.020mol?L-1的盐酸,则c(Ag+)=
1.8×10-7mol/L
1.8×10-7mol/L
,此时所得混合溶液的pH=2
2
.碳是形成化合物最多的元素。
(1)由碳元素参与形成的物质多为分子晶体,也有少数原子晶体。下列关于分子晶体和原子晶体的说法正确的是 (填字母序号)。
A、完全由非金属元素形成的物质一定是分子晶体或原子晶体
B、分子晶体中分子之间一定存在范德华力
C、SiC具有极高的熔点和较大的硬度,SiC分子中除存在共价键外,还存在分子间作用力
D、金刚石是由碳元素形成的原子晶体,性质稳定,不与任何物质反应
(2)意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的C4分子。C4分子结构如图所示。下列说法正确的是 。
A、C4属于一种新型的化合物 B、C4与P4(白磷)的晶体都属于分子晶体
C、C4气体分子内含有极性共价键 D、C4与C60互为同素异形
(3)与碳同主族元素锗为32号元素,与锗同周期,且未成对电子数与锗相同,电负性最大的元素的价电子排布式为 。
(4)邻硝基苯酚的熔点 对硝基苯酚(填“>”、“=”或“<”=)。
(5)硼、碳、氮、氧是元素周期表第二周期相邻的四种元素。下列有关的四种化合物中,键角最小的是 。
A、CO2 B、CF4 C、NF3 D、OF2
已知硼酸H3BO3为白色固体,溶于水显弱酸性,但它却是一元酸,可以用硼酸在水溶液中的电离平衡解释它是一元弱酸的原因。
请写出下面这个方程式右端的两种离子的表达式: 。
。