摘要:按要求回答下列问题 ①石墨是层状晶体.每一层内.碳原子排列成正六边形.一个个六边形排列成平面的网状结构.如果将每对相邻的碳原子的化学键看成一个化学键.则石墨晶体的每一层中碳原子数与C-C化学键数的比是 石墨晶体中C-C键的键角为 .其中平均每个六边形所含的C原子数为 个. ④白磷分子中的键角为 .分子的空间结构为 .每个P原子与 个P原子结合成共价键.若将1分子白磷中的所有P-P键打开并各插入一个氧原子.共可结合 个氧原子,若每个P原子上的孤对电子再与氧原子配位.就可以得到磷的另一种氧化物 . ⑥晶体硼的基本结构单元都是由硼原子组成的正二十面体的原子晶体.其中含有20个等边三角形和一定数目的顶角.每个顶角各有一个原子.试观察图形回答.这个基本结构单元由 个硼原子组成.共含有 B-B键. ⑦NH3分子的空间结构为 .它具有碱性是由于分子中存在 .当结合H+后形成的NH4+离子的的空间结构为 .分子中N-H键的键角为 . ⑧晶体硼的基本结构单元都是由硼原子组成的正二十面体的原子晶体.其中含有20个等边三角形和一定数目的顶角.每个顶角各有一个原子.试观察图形回答.这个基本结构单元由 个硼原子组成.键角是 .共含有 个B-B键.
网址:http://m.1010jiajiao.com/timu_id_3712136[举报]
 A、B、C、D都是由短周期元素组成的常见物质,其中A、B、C均含同一种元素,在一定条件下相互转化关系如图所示(部分产物已略去).
A、B、C、D都是由短周期元素组成的常见物质,其中A、B、C均含同一种元素,在一定条件下相互转化关系如图所示(部分产物已略去).请按要求回答下列问题:
(1)若B、C 为氧化物,C能够与水反应生成一种强酸.
①当B为无色易溶于水的刺激性气体时,写出B转化为C的化学方程式:
2SO2+O2
SO3
| 催化剂 |
| △ |
2SO2+O2
SO3
.| 催化剂 |
| △ |
②当B为无色不溶于水的气体时,写出C与水反应的化学方程式:
3NO2+H2O=NO+2HNO3
3NO2+H2O=NO+2HNO3
.(2)若D为氧化物,A、B、C都是强电解质,C可用于食品发酵、泡沫灭火.写出A与D反应的离子方程式:
2OH-+CO2=CO32-+H2O
2OH-+CO2=CO32-+H2O
.(3)若D为强酸或强碱溶液时都能发生图示转化关系,且A和C在溶液中反应生成白色沉淀B.
当D为强酸时,A→B反应的离子方程式:
AlO2-+H2O+H+=Al(OH)3↓
AlO2-+H2O+H+=Al(OH)3↓
;当D为强碱时,B→C反应的离子方程式:
Al(OH)3+OH-=AlO2-+H2O
Al(OH)3+OH-=AlO2-+H2O
.A、B、C、D、E、F是原子序数依次增大的短周期主族元素.A与D同主族、C与E同主族;B原子的最外层电子数是次外层电子数的2倍;D的原子序数是A的11倍,E的原子序数是C的原子序数的2倍.按要求回答下列问题:
(1)B原子的轨道表示式为 .D离子的电子排布式为 .
(2)由上述元素组成的化合物中属于极性键形成的非极性分子是(写出其中的任意两种,用化学式表示) 、 .
(3)A、B、D分别与F形成的化合物,熔沸点由低到高的顺序是(用化学式表示) .
(4)乙、丙是由上述元素组成的化合物,它们都含有四种元素,其中乙、丙所含的元素种类完全相同.若将乙、丙形成的溶液相混合,有刺激性气味的气体生成,将该气体通入到F单质形成的水溶液中,生成两种强酸.试写出有关离子方程式:
①乙、丙形成的溶液相混合 ;
②刺激性气味气体通入F单质形成的水溶液中 .
查看习题详情和答案>>
(1)B原子的轨道表示式为
(2)由上述元素组成的化合物中属于极性键形成的非极性分子是(写出其中的任意两种,用化学式表示)
(3)A、B、D分别与F形成的化合物,熔沸点由低到高的顺序是(用化学式表示)
(4)乙、丙是由上述元素组成的化合物,它们都含有四种元素,其中乙、丙所含的元素种类完全相同.若将乙、丙形成的溶液相混合,有刺激性气味的气体生成,将该气体通入到F单质形成的水溶液中,生成两种强酸.试写出有关离子方程式:
①乙、丙形成的溶液相混合
②刺激性气味气体通入F单质形成的水溶液中
按要求回答下列问题:
(1)写出硅酸钠溶液在空气中变质的化学方程式:
(2)写出用熟石灰吸收氯气制漂白粉的化学方程式:
(3)将CaMg3Si4O12改写为氧化物的形式:
(4)有的科学家提出用金属过氧化物(如Na202)可实现宇宙飞船中氧气和C02的循环,请写出Na202和C02反应的化学方程式
查看习题详情和答案>>
(1)写出硅酸钠溶液在空气中变质的化学方程式:
Na2SiO3+CO2+H2O=H2SiO3↓+Na2CO3
Na2SiO3+CO2+H2O=H2SiO3↓+Na2CO3
;(2)写出用熟石灰吸收氯气制漂白粉的化学方程式:
2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
;(3)将CaMg3Si4O12改写为氧化物的形式:
CaO?3MgO?4SiO2
CaO?3MgO?4SiO2
.(4)有的科学家提出用金属过氧化物(如Na202)可实现宇宙飞船中氧气和C02的循环,请写出Na202和C02反应的化学方程式
2Na2O2+2CO2=2Na2CO3+O2
2Na2O2+2CO2=2Na2CO3+O2
,当生成1molO2,转移的电子数为2
2
NA.如图是几种中学化学常见物质的转化关系图,其中气体D、E为单质,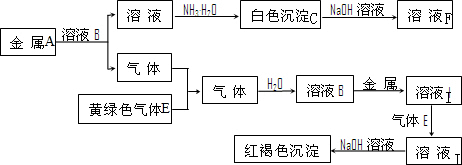
请按要求回答下列问题.
(1)C的化学式是
(2)写出反应“C→F”的离子方程式 ;
(3)写出反应“I→J”的离子方程式 ;
(4)写出金属A与NaOH溶液反应的离子方程式 .
查看习题详情和答案>>

请按要求回答下列问题.
(1)C的化学式是
(2)写出反应“C→F”的离子方程式
(3)写出反应“I→J”的离子方程式
(4)写出金属A与NaOH溶液反应的离子方程式
按要求回答下列问题
(1)某温度下,纯水中c (H+)=2.0×10-7mol?L-1,则此时c (OH-)=
(2)向0.020mol?L-1的HCN溶液中加入0.020mol NaCN固体,溶液pH增大,主要原因是
(3)向1L 0.10mol?L-1的HCN溶液中加入0.08molNaOH固体,得到混合溶液,则
查看习题详情和答案>>
(1)某温度下,纯水中c (H+)=2.0×10-7mol?L-1,则此时c (OH-)=
2.0×10-7
2.0×10-7
mol?L-1;0.9mol?L-1NaOH溶液与0.1mol?L-1HCl溶液等体积混合(不考虑溶液体积变化)后,溶液的pH=13
13
.(2)向0.020mol?L-1的HCN溶液中加入0.020mol NaCN固体,溶液pH增大,主要原因是
CN-浓度增大,抑制了HCN的电离,使c(H+)降低,pH值增大
CN-浓度增大,抑制了HCN的电离,使c(H+)降低,pH值增大
;已知该混合溶液中c (Na+)>c (CN-),则c (HCN)>
>
c (CN-)(用“>”、“<”、“=”符号填空).(3)向1L 0.10mol?L-1的HCN溶液中加入0.08molNaOH固体,得到混合溶液,则
HCN
HCN
和CN-
CN-
两种粒子的物质的量之和等于0.1mol;写出该混合溶液中存在的所有平衡的表达式HCN H++CN-、H2O
H++CN-、H2O H++OH-、CN-+H2O
H++OH-、CN-+H2O HCN+OH-
HCN+OH-
 H++CN-、H2O
H++CN-、H2O H++OH-、CN-+H2O
H++OH-、CN-+H2O HCN+OH-
HCN+OH-HCN H++CN-、H2O
H++CN-、H2O H++OH-、CN-+H2O
H++OH-、CN-+H2O HCN+OH-
HCN+OH-
. H++CN-、H2O
H++CN-、H2O H++OH-、CN-+H2O
H++OH-、CN-+H2O HCN+OH-
HCN+OH-