网址:http://m.1010jiajiao.com/timu_id_3711863[举报]
(1)从不同角度可以对上述反应进行分类:从反应前后能量变化角度看上述反应属于放热反应的是
(2)反应③在实验室中用于制备氢气,要提高生成氢气的速率下列措施合理的是
a.加入硝酸,增大氢离子的浓度 b.用浓硫酸代替稀硫酸
c.加入少量铜粉 d.将稀硫酸的体积加倍.
反应③可以设计成原电池反应,其中负极上反应的物质是
(3)反应②是可逆反应,常应用于工业生产,升高温度正反应速率
图表法、图象法是常用的科学研究方法.下表列出前20号元素中的某些元素性质的一些数据:
| 元素 性质 |
A | B | C | D | E | F | G | H | I | J |
| 原子半径(10-10m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| 最高价态 | +6 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| 最低价态 | -2 | - | -2 | - | -4 | -3 | -1 | - | -3 | -4 |
(1)以上10种元素中第一电离能最小的是:
(2)由上述C、E、G三种元素中的某两种元素形成的化合物中,每个原子的最外层都满足8电子稳定结构的可能是
(3)元素E与C及氢元素可形成一种相对分子质量为60的一元羧酸分子.其分子中共形成
(4)短周期某主族元素K的电离能情况如图(A)所示.则K元素位于周期表的第

图B是研究部分元素的氢化物的沸点变化规律的图象,折线c可以表达出第
[化学-物质结构与性质] (13分)
(1)中国古代四大发明之一——黑火药,它的爆炸反应为
![]() (已配平)
(已配平)
①除S外,上列元素的电负性从大到小依次为 。
②在生成物中,A的晶体类型为 ,含极性共价键的分子的中心原子轨道杂化类型为 。
③已知![]() 与
与![]() 结构相似,推算HCN分子中
结构相似,推算HCN分子中![]() 键与
键与![]() 键数目之比为 。
键数目之比为 。
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布为 ,![]() 的未成对电子数是 。
的未成对电子数是 。
(3![]() )在
)在![]() 的水溶液中,一定条件下存在组成为
的水溶液中,一定条件下存在组成为![]() (n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:
(n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:
![]()
交换出来的![]() 经中和滴定,即可求出x和n,确定配离子的组成。¥高#考#资%源*网
经中和滴定,即可求出x和n,确定配离子的组成。¥高#考#资%源*网
将含0.0015 mol ![]() 的溶液,与R-H完全交换后,中和生成的
的溶液,与R-H完全交换后,中和生成的![]() 需浓度为0.1200 mol·L-1 NaOH溶液25.00 ml,该配离子的化学式为 。
需浓度为0.1200 mol·L-1 NaOH溶液25.00 ml,该配离子的化学式为 。![]()
[化学-物质结构与性质]13分
(1)元素的第一电离能:Al Si(填“>”或:“<”)
(2)基态Mn2+的核外电子排布式为 。
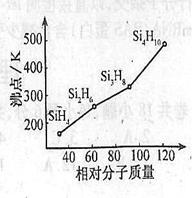
(3)硅烷(SinH2n+2)的沸点与其相对分子质量的变化关系如右图所示,呈现这种变化关系的原因是 。
(4)硼砂是含结晶水的四硼酸钠,其阴离子Xm—(含B、O、H三种元素)的球棍模型如右下图所示:
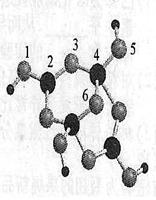
①在Xm—中,硼原子轨道的杂化类型有 ;配位键存在于 原子之间(填原子的数字标号);
m= (填数字)。
②硼砂晶体由Na+、Xm—和H2O构成,它们之间存在的作用力有 (填序号)。
A.离子键 B.共价键 C.金属键
D.范德华力 E.氢键
查看习题详情和答案>>[化学-物质结构与性质] (13分)
(1)中国古代四大发明之一——黑火药,它的爆炸反应为
![]() (已配平)
(已配平)
①除S外,上列元素的电负性从大到小依次为 。
②在生成物中,A的晶体类型为 ,含极性共价键的分子的中心原子轨道杂化类型为 。
③已知![]() 与
与![]() 结构相似,推算HCN分子中
结构相似,推算HCN分子中![]() 键与
键与![]() 键数目之比为 。
键数目之比为 。
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布为 ,![]() 的未成对电子数是 。
的未成对电子数是 。
(3)在![]() 的水溶液中,一定条件下存在组成为
的水溶液中,一定条件下存在组成为![]() (n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:
(n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:
![]()
交换出来的![]() 经中和滴定,即可求出x和n,确定配离子的组成。¥
经中和滴定,即可求出x和n,确定配离子的组成。¥
将含0.0015 mol ![]() 的溶液,与R-H完全交换后,中和生成的
的溶液,与R-H完全交换后,中和生成的![]() 需浓度为0.1200 mol·L-1NaOH溶液25.00 ml,该配离子的化学式为 。
需浓度为0.1200 mol·L-1NaOH溶液25.00 ml,该配离子的化学式为 。
查看习题详情和答案>>