摘要:(1)Fe2O3+6H+2Fe3++3H2O (2)CO+2H+H2O十CO2↑ (3)Cu2++SO+Ba2++2OH-BaSO4↓+Cu(OH)2↓ (4)Ca2++2OH-+CO2CaCO3↓+H2O
网址:http://m.1010jiajiao.com/timu_id_3709357[举报]
下列氧化还原反应中,实际参加反应的氧化剂与还原剂的物质的量之比正确的是( )
①KClO3+6HCl(浓)═KCl+3Cl2↑+3H2O;1:6
②Fe2O3+2Al
Al2O3+2Fe;1:2
③SiO2+3C═SiC+2CO↑;1:2
④3NO2+H2O═2HNO3+NO;2:1.
①KClO3+6HCl(浓)═KCl+3Cl2↑+3H2O;1:6
②Fe2O3+2Al
| ||
③SiO2+3C═SiC+2CO↑;1:2
④3NO2+H2O═2HNO3+NO;2:1.
查看习题详情和答案>>
(2013?江苏三模)实验室模拟回收某废旧含镍催化剂(主要成分为NiO,另含Fe2O3、CaO、CuO、BaO等)生产Ni2O3.其工艺流程为:
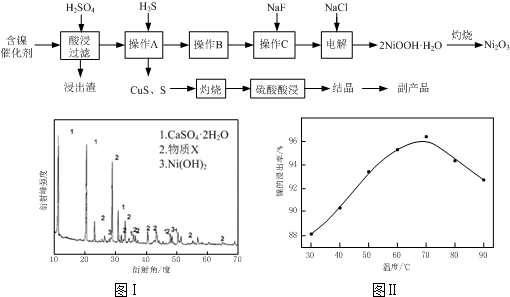
(1)根据图Ⅰ所示的X射线衍射图谱,可知浸出渣含有三种主要成分,其中“物质X”为
(2)工艺流程中“副产品”的化学式为
(3)已知有关氢氧化物开始沉淀和沉淀完全的pH如下表:
操作B是为了除去滤液中的铁元素,某同学设计了如下实验方案:向操作A所得的滤液中加入NaOH溶液,调节溶液pH为3.7~7.7,静置,过滤.请对该实验方案进行评价:
(4)操作C是为了除去溶液中的Ca2+,若控制溶液中F-浓度为3×10-3 mol?L-1,则Ca2+的浓度为
(5)电解产生2NiOOH?H2O的原理分两步:①碱性条件下Cl-在阳极被氧化为ClO-;②Ni2+被ClO-氧化产生2NiOOH?H2O沉淀.第②步反应的离子方程式为
查看习题详情和答案>>

(1)根据图Ⅰ所示的X射线衍射图谱,可知浸出渣含有三种主要成分,其中“物质X”为
BaSO4
BaSO4
.图Ⅱ表示镍的浸出率与温度的关系,当浸出温度高于70℃时,镍的浸出率降低,浸出渣中Ni(OH)2含量增大,其原因是温度升高,Ni2+的水解程度增大
温度升高,Ni2+的水解程度增大
.(2)工艺流程中“副产品”的化学式为
CuSO4?5H2O
CuSO4?5H2O
.(3)已知有关氢氧化物开始沉淀和沉淀完全的pH如下表:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 7.7 |
| 沉淀完全的pH | 3.7 | 9.7 | 9.2 |
方案错误;在调节pH前,应先在滤液中加入H2O2,使溶液中的Fe2+氧化为Fe3+
方案错误;在调节pH前,应先在滤液中加入H2O2,使溶液中的Fe2+氧化为Fe3+
(若原方案正确,请说明理由;若原方案错误,请加以改正).(4)操作C是为了除去溶液中的Ca2+,若控制溶液中F-浓度为3×10-3 mol?L-1,则Ca2+的浓度为
3×10-6
3×10-6
mol?L-1.(常温时CaF2的溶度积常数为2.7×10-11)(5)电解产生2NiOOH?H2O的原理分两步:①碱性条件下Cl-在阳极被氧化为ClO-;②Ni2+被ClO-氧化产生2NiOOH?H2O沉淀.第②步反应的离子方程式为
ClO-+2Ni2++4OH-=2NiOOH?H2O+Cl-
ClO-+2Ni2++4OH-=2NiOOH?H2O+Cl-
.工业上常回收冶炼锌废渣中的锌(含有ZnO、FeO、Fe2O3、CuO、Al2O3等杂质),并用来生产Zn(NO3)2?6H2O晶体,其工艺流程为:
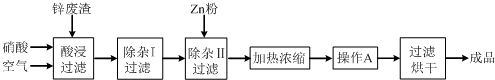
有关氢氧化物开始沉淀和沉淀完全的pH如下表:
(1)在“酸浸”步骤中,为提高锌的浸出速率,除通入空气“搅拌”外,还可采取的措是
(2)上述工艺流程中多处涉及“过滤”,实验室中过滤操作需要使用的玻璃仪器有
(3)在“除杂I”步骤中,需再加入适量H2O2溶液,H2O2与Fe2+反应的离子方程式为
(4)加入Zn粉的作用是
(5)在0.10mol?L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当pH=8时,溶液的c(Cu2+)浓度为
查看习题详情和答案>>

有关氢氧化物开始沉淀和沉淀完全的pH如下表:
| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| 开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 | 5.4 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 | 8.0 |
适当升高反应温度
适当升高反应温度
.(2)上述工艺流程中多处涉及“过滤”,实验室中过滤操作需要使用的玻璃仪器有
烧杯、玻璃棒、漏斗
烧杯、玻璃棒、漏斗
.(3)在“除杂I”步骤中,需再加入适量H2O2溶液,H2O2与Fe2+反应的离子方程式为
2Fe2++H2O2+2H+=2Fe3++2H2O
2Fe2++H2O2+2H+=2Fe3++2H2O
.为使Fe(OH)3、Al(OH)3沉淀完全,而Zn(OH)2不沉淀,应控制溶液的pH范围为5.2~5.4
5.2~5.4
.检验Fe3+是否沉淀完全的实验操作是静置片刻,取少量上层清液,滴加KSCN溶液,若不出现血红色,表明Fe3+沉淀完全
静置片刻,取少量上层清液,滴加KSCN溶液,若不出现血红色,表明Fe3+沉淀完全
.(4)加入Zn粉的作用是
除去溶液中的Cu2+
除去溶液中的Cu2+
.“操作A”的名称是冷却结晶
冷却结晶
.(5)在0.10mol?L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当pH=8时,溶液的c(Cu2+)浓度为
2.2×10-8
2.2×10-8
(Ksp[Cu(OH)2]=2.2×10-20).某同学对MnO2、CuO、Fe2O3、Cr2O3在氯酸钾受热分解反应中的催化作用进行了研究.实验所得数据如下表.就本实验的有关问题,请填空:
(1)本实验的装置由如图所示三部分组成,其正确的接口连接顺序为
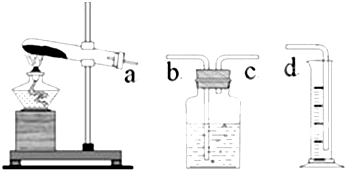
(2)为证明编号2的实验中MnO2起到催化作用,上述实验后还要测定反应剩余物MnO2的质量,实验的操作顺序是:溶解→
(3)从上表实验数据分析,对氯酸钾受热分解有催化作用的物质,按其催化能力从大到小的顺序为
(4)从编号3的实验数据,可计算出KClO3的分解率为
(5)在进行编号5的实验时,有刺激性的黄绿色气体产生,该气体可能是
查看习题详情和答案>>
| 实验 编号 |
KClO3(g) | 氧化物 | 产生气体(mL) (已折算为标况) |
耗时(s) | 化学式 | 质量(g) | 实际回收 | 1 | 0.6 | - | - | - | 10 | 480 | 2 | 0.6 | MnO2 | 0.20 | 90% | 67.2 | 36.5 | 3 | 0.6 | CuO | 0.20 | 90% | 67.2 | 79.5 | 4 | 0.6 | Fe2O3 | 0.20 | 90% | 67.2 | 34.7 | 5 | 0.6 | Cr2O3 | 0.20 | 异常 | 67.2 | 188.3 |
a→c→b→d
a→c→b→d
.
(2)为证明编号2的实验中MnO2起到催化作用,上述实验后还要测定反应剩余物MnO2的质量,实验的操作顺序是:溶解→
过滤
过滤
→洗涤
洗涤
→烘干
烘干
→称量
称量
.(3)从上表实验数据分析,对氯酸钾受热分解有催化作用的物质,按其催化能力从大到小的顺序为
Fe2O3 >MnO2 >CuO
Fe2O3 >MnO2 >CuO
(填物质的化学式).(4)从编号3的实验数据,可计算出KClO3的分解率为
40.8
40.8
%(保留一位小数).(5)在进行编号5的实验时,有刺激性的黄绿色气体产生,该气体可能是
Cl2
Cl2
(填化学式),常用湿润的淀粉碘化钾
湿润的淀粉碘化钾
试纸检验该气体,上述异常现象产生的原因是氯酸钾在加热条件下将Cr2O3氧化为可溶性化合物
氯酸钾在加热条件下将Cr2O3氧化为可溶性化合物
. 下图为五个椭圆交叉构成的图案,椭圆内分别写了C2H5OH、CO2、Fe2O3、FeCl3和NaOH五种物质,图中相连的两种物质均可归为一类,相交的部分A、B、C、D为其相应的分类标准代号.请回答下列问题:
下图为五个椭圆交叉构成的图案,椭圆内分别写了C2H5OH、CO2、Fe2O3、FeCl3和NaOH五种物质,图中相连的两种物质均可归为一类,相交的部分A、B、C、D为其相应的分类标准代号.请回答下列问题:(1)两种物质都是非电解质的是
A
A
(填分类标准代号,下同),两种物质在水溶液中都能导电的是D
D
.(2)分类标准代号C表示
ac
ac
(多项选择)a.两物质都是电解质b.两物质都可与酸反应
c.两物质都有氧化性d.两物质可以通过一步反应相互转化
(3)上述五种物质中的某一物质能与某种强酸反应生成上述中的另一种物质,该反应的化学方程式为
Fe2O3+6 HCl=2FeCl3+3H2O
Fe2O3+6 HCl=2FeCl3+3H2O
.(4)图中相连的两种物质可归为一类,又能相互反应的是
D
D
(填分类标准代号),其反应的基本类型是复分解
复分解
反应.(5)用洁净的烧杯取25mL蒸馏水,加热至沸腾,向烧杯中逐滴加入上述五种物质中的某一物质的饱和溶液,加热呈红褐色,得到的分散系称为
胶体
胶体
,该反应的化学方程式为FeCl3+3H2O
Fe(OH)3(胶体)+3HCl
| ||
FeCl3+3H2O
Fe(OH)3(胶体)+3HCl
.
| ||