摘要:解析:本题以课本上硫酸亚铁晶体制备实验为起点.进一步拓展和提升来制备摩尔盐. (1)中将铁屑在Na2CO3溶液中加热.Na2CO3溶液水解显碱性.可使铁屑上附着的油污水解而除去.在铁屑与稀硫酸的反应中.铁屑过量.故得到的是硫酸亚铁.其物质的量等于硫酸的物质的量=,根据.硫酸铵的质量为 (2)中由于硫酸亚铁具有较强的还原性.易被氧化.故在制备过程中必须避免与空气接触.在所有制备结晶水合物的操作中.均不可剧烈加热.否则会失去结晶水.由提供的溶解度数据可知(NH4)2Fe(SO4)2·6H2O溶解度最小.加热浓缩.溶剂减少.(NH4)2Fe(SO4)2·6H2O便结晶析出.KMnO4酸性溶液因具有强氧化性.能氧化碱式滴定管中的橡胶.故只能装入酸式滴定管中.KMnO4酸性溶液的浓度根据5Fe2+ + MnO4- + 8H+= 5Fe3++ Mn2+ + 4H2O计算. 答案:(1)①铁屑表面的油污 ②硫酸亚铁 0.045 ③5.94 (2) ①a过滤洗涤操作速度要快 b步骤③要缓缓加热.避免沸腾 ②因为析出的是硫酸亚铁铵晶体.带有结晶水.蒸干会使晶体分解.③因为相同温度下硫酸亚铁铵晶体在水中的溶解度比硫酸亚铁和硫酸铵的溶解度小 ④Ⅰ)酸式.右 Ⅱ) 5Fe2+ + MnO4- + 8H+= 5Fe3++ Mn2+ + 4H2O Ⅲ)当溶液变成紫红色.30S内不褪色.说明达到滴定终点 Ⅳ)1/V
网址:http://m.1010jiajiao.com/timu_id_3707175[举报]
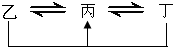 元素A、B、C、D、E、F是位于元素周期表前四周期元素,且原子序数依次增大.其中 D、F为常见金属元素;A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为0.759g?L-1,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族,由D或F元素组成的单质或某些离子(或化合物)在溶液中均有下列转化关系(其它参与反应的物质未列出):其中,均含D元素的乙、丙、丁微粒间的转化全为非氧化还原反应;均含F元素的乙、丙、丁微粒间的转化全为氧化还原反应;相邻的乙与丙或丙与丁两两间均互不发生化学反应.请回答下列问题:
元素A、B、C、D、E、F是位于元素周期表前四周期元素,且原子序数依次增大.其中 D、F为常见金属元素;A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为0.759g?L-1,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族,由D或F元素组成的单质或某些离子(或化合物)在溶液中均有下列转化关系(其它参与反应的物质未列出):其中,均含D元素的乙、丙、丁微粒间的转化全为非氧化还原反应;均含F元素的乙、丙、丁微粒间的转化全为氧化还原反应;相邻的乙与丙或丙与丁两两间均互不发生化学反应.请回答下列问题:(1)写出化合物甲的电子式:


(2)写出化合物甲的水溶液与D元素对应的金属阳离子反应的离子方程式
3NH3?H2O+Al3+=Al(OH)3↓+3NH4+
3NH3?H2O+Al3+=Al(OH)3↓+3NH4+
;写出均含有F元素的乙与丁在溶液中发生反应的离子方程式Fe+2Fe3+=3Fe2+
Fe+2Fe3+=3Fe2+
.(3)由A、C元素组成的化合物戊和A、E元素组成的化合物己,式量均为34.其中戊的熔沸点高于己,其原因是:
H2O2分子间存在氢键
H2O2分子间存在氢键
.(4)复盐是指由2种或2种以上阳离子和一种酸根离子组成的盐.请写出由A、B、C、E、F元素组成的一种具有还原性的复盐庚的化学式
NH4)2Fe(SO4)2或(NH4)2Fe(SO4)2?6H2O或(NH4)2SO4?FeSO4?6H2O
NH4)2Fe(SO4)2或(NH4)2Fe(SO4)2?6H2O或(NH4)2SO4?FeSO4?6H2O
.该复盐是一种重要的化学试剂,据中学课本介绍,工业上常用如下方法制取:将一定量的两种盐配成混合溶液,再加热浓缩混合溶液,冷却至室温则析出带有6个结晶水的该复盐晶体.写出相关反应的化学方程式(NH4)2SO4+FeSO4+6H2O=(NH4)2Fe(SO4)2?6H2O
(NH4)2SO4+FeSO4+6H2O=(NH4)2Fe(SO4)2?6H2O
,析出该复盐晶体的原理是硫酸亚铁铵在水中溶解度比硫酸铵、硫酸亚铁在水中的溶解度要小得多
硫酸亚铁铵在水中溶解度比硫酸铵、硫酸亚铁在水中的溶解度要小得多
.