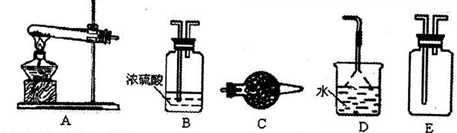
摘要:(1)NH3.CO2.NO.N2.NO2. (2)2Na2O2+ 2CO2= 2Na2CO3 + O2. 2NO+O2=2N02 (3)CO2 .NO .3:2.
网址:http://m.1010jiajiao.com/timu_id_3706978[举报]
(1)0.5mol H2O的质量为
(2)质量都是50g的 HCl、NH3、CO2、O2四种气体中,含有分子数目最少的是
(3)在
查看习题详情和答案>>
9g
9g
,其中共含有9.01×1023
9.01×1023
个原子.(2)质量都是50g的 HCl、NH3、CO2、O2四种气体中,含有分子数目最少的是
CO2
CO2
(填分子式,下同),在相同温度和相同压强条件下,体积最大的是NH3
NH3
.(3)在
125
125
mL 0.2mol/L NaOH溶液中含1g溶质;配制50mL 0.2mol/L CuSO4溶液,需要CuSO4?5H2O2.5
2.5
g.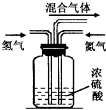 氨气是一种重要的化工原料,但随着工业化进程的加快,氨气也逐渐变成居室里一种重要的污染性气体.
氨气是一种重要的化工原料,但随着工业化进程的加快,氨气也逐渐变成居室里一种重要的污染性气体.(1)液氨和水类似,也能发生电离:NH3+NH3=NH4++NH2-,其离子积常数为l.0×l0-30.现将2.3g金属钠投入1.0L液氨中,则液氨电离平衡
正方向
正方向
移动(填“不”、“正方向”、“逆方向”);待反应结束后,假设溶液的体积不变,所得溶液中NH4+的浓度为1×10-29mol/L
1×10-29mol/L
.(2)实验室模拟工业上用氮气和氢气合成氨气时,在反应前将两种气体通过如图装置,该装置的作用有三个:
①将氮气和氢气干燥:
②使氮气和氢气充分混合;
③
通过观察气泡控制氮气和氢气的流量,使氮气和氢气的量达到最佳比例
通过观察气泡控制氮气和氢气的流量,使氮气和氢气的量达到最佳比例
,从而提高氮气和氢气的利用率.(3)实验室可用氨气通过红热的氧化铜制取氮气,写出该反应的化学方程式:
2NH3+3CuO
3Cu+N2+3H2O
| ||
2NH3+3CuO
3Cu+N2+3H2O
.
| ||
(4)家庭空气中的氨主要来自建筑施工中使用的混凝土外加剂,如混凝土防冻剂尿素会和水缓慢发生反应:CO(NH2)2(s)+H2O(g) 2NH3(g)+CO2(g),该反应的平衡常数表达式为K=
| C2(NH3)?C(CO2) |
| C(H2O) |
| C2(NH3)?C(CO2) |
| C(H2O) |
(5)已知:N2(g)+O2(g)=2NO(g);△H=180Kj?mol-l4NH3(g)+5O2(g)=4NO(g)+6H2O(g);△H=-908Kj?mol-l请写出氨气被一氧化氮氧化生成氮气和气态水的热化学方程式:
4NH3(g)+6NO(g)=5N2(g)+6H2O(g)△H=-1808KJ/mol
4NH3(g)+6NO(g)=5N2(g)+6H2O(g)△H=-1808KJ/mol
. 按要求完成下列小题.
按要求完成下列小题.(1)0.5mol H2O的质量为
9
9
g,共有0.5NA或3.01*1023
0.5NA或3.01*1023
个分子,5NA或3.01*1024
5NA或3.01*1024
个电子.(2)0.01mol某物质的质量为1.08g,则此物质的摩尔质量为
108g/mol
108g/mol
(3)配制50mL 0.2mol/L CuSO4溶液,需要CuSO4
1.6
1.6
g;需要CuSO4?5H2O2.5
2.5
g.(4)质量都是50g的 HCl、NH3、CO2、O2四种气体中,含有分子数目最少的是
CO2
CO2
,在相同温度和相同压强条件下,体积最大的是NH3
NH3
(5)同温同压下,气体A与氧气的质量比为1:2,体积比为1:4,气体A的相对分子质 量是
(6)VL 硫酸铁中含Fe3+离子质量为m g,则溶液中SO42-离子的物质的量浓度为
| 3m |
| 112V |
| 3m |
| 112V |
(7)如图是我校化学实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.
①该浓硫酸的物质的量浓度
18.4mol/L
18.4mol/L
②用该浓硫酸配制200mL1mol/L的稀硫酸,量筒所需量
取该浓硫酸的体积是
10.9
10.9
mL.(2010?徐汇区二模)卤水中的主要成分为食盐(假设其所含杂质仅为NaBr),为了充分利用资源,有研究人员开发了以晒盐卤水和化肥碳酸氢铵为原料制取纯碱的工艺,其生产流程如图.

(1)写出卤水和碳酸氢铵反应的化学方程式
(2)操作I是
(3)若滤渣中含有NH4Cl杂质,则可能导致纯碱中混有杂质,写出煅烧时产生杂质的副反应的化学方程式
(4)实验室检测滤渣中是否含有NH4Cl的操作是
(5)碳酸氢铵与氯化钠的配料比是影响纯碱质量的因素之一,如图是
(摩尔比)对NaHCO3产率的影响.实际生产中选择
=1.2.
①下列相关说法正确的是
a.碳酸氢铵过量是为了充分利用卤水
b.碳酸氢铵过量是为了减少纯碱中的NaCl
c.碳酸氢铵过量太多将会导致生产成本过高
②不考虑生产过程中的损耗,生产1mol纯碱,需消耗碳酸氢铵
查看习题详情和答案>>

(1)写出卤水和碳酸氢铵反应的化学方程式
NaCl+NH4HCO3=NaHCO3↓+NH4Cl
NaCl+NH4HCO3=NaHCO3↓+NH4Cl
;(2)操作I是
过滤、洗涤
过滤、洗涤
(填操作名称),试剂X为盐酸
盐酸
,残液除NH4Cl外,还含有NaBr
NaBr
;(3)若滤渣中含有NH4Cl杂质,则可能导致纯碱中混有杂质,写出煅烧时产生杂质的副反应的化学方程式
NaHCO3+NH4Cl
NaCl+NH3↑+H2O+CO2↑
| ||
NaHCO3+NH4Cl
NaCl+NH3↑+H2O+CO2↑
;
| ||
(4)实验室检测滤渣中是否含有NH4Cl的操作是
取洗涤液,加入足量硝酸至溶液呈酸性,再滴加硝酸银溶液,无沉淀说明纯净
取洗涤液,加入足量硝酸至溶液呈酸性,再滴加硝酸银溶液,无沉淀说明纯净
;
(5)碳酸氢铵与氯化钠的配料比是影响纯碱质量的因素之一,如图是
| n(NH4HCO3) |
| n(NaCl) |
| n(NH4HCO3) |
| n(NaCl) |
①下列相关说法正确的是
bc
bc
.a.碳酸氢铵过量是为了充分利用卤水
b.碳酸氢铵过量是为了减少纯碱中的NaCl
c.碳酸氢铵过量太多将会导致生产成本过高
②不考虑生产过程中的损耗,生产1mol纯碱,需消耗碳酸氢铵
2.4
2.4
mol.