摘要:[杂化轨道理论]同一原子中能量相近的原子轨道.在成键时组合成成键能力更强的新轨道的过程.称作原子轨道的杂化.形成的新轨道称作杂化轨道.有几条原子轨道参加杂化就能得到几条杂化轨道.杂化轨道理论是在电子配对为基础的价键理论上提出并发展的.杂化轨道理论能很好地解释有机化合物的分子空间结构问题.例如.碳原子最外层的电子排布为2s22p2.有两个未成对电子.按电子配对法只能形成两个共价键.而两个共价键的键角应是90°.但实际上甲烷分子中4个C-H键完全相同.键角是109°28′.杂化理论认为.碳原子成键时2s中的1个电子吸收能量被激发到2p轨道.形成4个未成对电子.然后1个s轨道和3个p轨道组合形成4个等价的sp3杂化轨道.分别与4个氢原子形成4个共价键.键角都是109°28′.是正四面体构型. [σ键]两个原子轨道沿键轴方向重叠而形成的一种以两个原子核之间的直线为对称轴的共价键叫σ键.构成σ键的电子叫σ电子.σ键是原子轨道沿轴向重叠的.具有较大的重叠程度.因而比较稳定.σ键可以自由旋转.而不影响电子云的分布. [π键]成键原子的未杂化的p轨道.通过平行侧向重叠所形成的共价键叫π键.两个p轨道侧向重叠.其重叠程度比轴向重叠的σ键小.稳定性不如σ键.两个p轨道在平行时才能较大地重叠.当形成π键的两个原子以核间轴为轴相对旋转时.会使p轨道重叠程度减小.导致π键的破坏.π键电子云密集在核间轴平面的上面和下面两部分.受两核的吸引力较弱.有较大的流动性. [大π键]大π键通常是指苯环的6个成环碳原子各以1个未杂化的2p轨道彼此重叠形成的封闭的共轭π键. [单键]分子中两个成键原子各以1个未成对电子形成一对共用电子对.这样的共价键叫单键.单键通常都是σ键. [双键]分子中两个原子间共用两对电子所形成的共价键叫双键.双键不是单键的简单加和.通常都是由1个σ键和1个π键构成的.如乙烯“C=C 键键能是598千焦/摩尔.小于乙烷“C-C 键键能的两倍.乙烯分子中的两个碳原子各形成3个sp2杂化轨道.两个碳原子间形成1个σ键.两个碳原子各以σ键再结合两个氢原子.这些σ键同处于一个平面上.各σ键间的键角约120°.而两个未杂化的p轨道垂直于该平面并侧向重叠形成π键.双键中的σ键不能象单键的σ键那样自由旋转.其中的π键易被破坏发生加成反应. [叁键]分子中两个原子间共用三对电子所形成的共价键叫叁键.参键不是单键或单键与双键的简单加和.叁键通常是由1个σ键和2个π键构成.如乙炔分子中两个碳原子各形成两个sp杂化轨道.两个碳原子间形成1个σ键.两个碳原子各以σ键再结合1个氢原子.这些σ键同处于一条直线上.两个碳原子各以两个未杂化而且相互垂直的P轨道.平行地侧向重叠形成两个π键.π键易被破坏发生加成反应. [苯环结构]苯环中每个碳原子各以3个电子按sp7杂化而形成三个σ键这三个σ键之间均为120°.6个碳原子处于同一平面上并形成正六边形.每个碳原子各剩余1个未杂化的p轨道.垂直于苯环的平面.彼此平行侧向重叠.形成一个π电子云完全平均化的闭合π键.这种大π键在通常情况下是稳定的. [诱导效应]分子中两个电负性不同的原子或原子团成键时.由于它们吸引电子的能力不同.就会产生永久偶极.这种极化作用可以沿σ键传递下去.这种作用叫诱导效应.诱导效应的传递由一个原子传至下一个原子.向同一方向.由近及远.明显减弱.超过三个原子时可以忽略不计.如氯乙的电负性强.产生诱导效应.导致生成物酸性增强: [共轭效应]由一个单键隔开的两个双键.如1.3-丁二烯CH2=CH-CH=CH2.叫共轭双键.含共轭双键的分子体系称为共轭体系.由于相邻的p轨道电子云互相发生作用.使键电子云分布趋于平均化.形成统一的整体.这种电子云分布平均化的结果.使得单键和双键的性质发生变化.与单独存在的单键和双键不同.这种变化叫共轭效应.共轭效应主要是通过π键传递.能从共轭体系的一端传递到较远的另一端.例如对硝基苯酚. 羟基中的氧原子上的负电荷能分散到包括硝基在内的共轭体系中.使得羟基的H-O键易断裂.其酸性比苯酚强得多.如2.4.6-三硝基苯酚.由于苯环上引入了3个硝基.使其酸性与无机强酸相近.取代基对有机物的影响往往同时具有共轭效应和诱导效应.这两种效应的方向可以一致.也可以不一致.如对氯苯酚中氯原子的诱导效应和把p电子云分散到整个共轭体系中的共轭效应在方向上是不一致的. [定位效应]苯环上原有取代基对新引入取代基位置的影响叫定位效应.苯环取代基的定位效应.可用诱导效应和共轭效应解释.取代基对苯环的诱导效应.导致苯环上与带取代基的碳原子上的π键电子云发生移动.使一些电子云分布相对较大的位置上活性较大.亲电取代反应主要发生在这些部位上.即为新导入的取代基确定了位置.苯环上原有取代基也叫定位基.邻对位定位基一般使苯环活化.取代反应比苯易于进行.常见的邻对位定位基有:-NH2.-OH.-NHCOCH3-CH3(-R).-X.一般邻对位定位基与苯环直接相连的原子具有未共用电子对或烷基.间位定位基一般使苯环钝化.取代反应比苯难于进行.取代反应主要发生在间位上.常见的间位定位基有-NO2.-CN.-SO3H.-CHO-COOH.-NR3+等.这类取代基直接和苯环相连的原子上一般有重键或带有正电荷. [同分异构]分子组成相同.但分子结构和性质不同的化合物叫做同分异构体.这种现象称为同分异构现象. [碳架异构]分子组成相同.但分子中碳原子相互连接的顺序不同的化合物叫碳架异构体.如C5H12有三种异构体: 碳架异构只涉及到碳原子的结合顺序.不涉及到分子中各原子在空间的排列和定向.随分子中碳原子数的增多.碳架异构的数目也随之增多. [位置异构]分子组成相同.但分子中的取代基或官能团在碳链或碳环上的位置不同的化合物叫做位置异构体.如丙醇有基或官能团的位置.通常是对碳架结构相同的化合物而言的. [类别异构]分子组成相同.但由于分子中各种原子结合的方式或顺序不同.因而具有不同官能团的化合物叫类别异构体.如乙醇和甲醚.乙酸和甲酸甲酯.丙醛和丙酮等互称为类别异构体.类别异构体与碳架异构体和位置异构体有很大的不同.类别异构体在化学性质上往往有本质的差别. [顺反异构]顺反异构即几何异构.通常存在于含有双键或环架结构的分子中.双键中的π键不能旋转.环架结构也阻碍了C-C单键的旋转.不同取代基在空间可形成不同的分布而产生异构.顺反异构分顺式和反式两种.若相同的原子或取代基在双键或碳架规定平面的同一侧叫顺式.若位于两侧叫反式.如含C=C双键和ab两种原子团 具体的物质象丁烯二酸.有顺丁烯二酸和反丁烯二酸 含环架结构的象1.4一二甲基环乙烷: [对映异构]对映异构即旋光异构.在分子中.与四个不同原子或原子团直接相连的碳原子叫做不对称碳原子.如乳酸分子中.与甲基.羟基.羧基.氢原子直接相连的碳原子.不对称碳原子周围的四个不同原子或原子团可以有两种互为镜象关系.但不能彼此重合的四面体空间构型.这两种构型互为对映异构体.对映异构体的物理及化学性质都相同.但在一定条件下的旋光方向相反.使偏振光左旋的为“左旋体 .使偏振光右旋的为“右旋体 .左旋体用L-或(-)-表示.右旋体用D-或(+)-表示.乳酸对映异构体费歇尔投影式可表示如下: 若将乳酸的左旋体和右旋体等量混和后.用“(±)-乳酸 表示.由于它们对偏振光的作用相互抵消.故不再有旋光性.叫外消旋体. [官能团]具有特定结构和性质.在有机物分子中容易发生化学反应并能决定有机化合物主要化学性质的原子或原子团. [烃基]烃分子中去掉一个或几个氢原子剩余的原子团叫做烃基.根据去掉的氢原子的数目.可将烃基分为一价基.二价基.三价基等,根据烃基对应的烃可分为烷基.乙烯基.苯基等. [烷基]从烷烃分子中去掉一个氢原子后得到的烃基叫烷基.烷基是一价基.可用通式CnH2n+1来表示.习惯上用字母R代表.常见的有: 能团.双键中的π键容易打开.发生加成反应.也可以发生聚合反应. 团.炔烃的不饱和性比烯烃更大.叁键中的两个π键可分两步打开.发生加成反应.最后得到饱和的化合物.炔烃也可以发生聚合反应. [乙烯基]乙烯分子中去掉一个氢原子剩余的部分叫做乙烯基.如乙烯基乙炔.苯乙烯等分子中都含有乙烯基. [苯基]苯分子去掉一个氢原子剩余的部分叫做苯基.如硝基 [苯甲基]亦称“苄基 .甲苯分子中甲基上去掉一个氢原子剩余的等分子中都含有苯甲基. [苄基]见苯甲基条. [羟基]亦称“氢氧基 .由H和O组成的一价原子团(-OH).在无机碱类.无机含氧酸及有机化合物的醇类.芳香醇类.酚类.羧酸等分子中都含有这种官能团. [氢硫基]见巯基条. [巯基]亦称“氢硫基 .由H和S组成的一价原子团.硫酚等分子中含有这种原子团. [氢硫基]见巯基条. 应.如丙醛与氢气加成生成1-丙醇.丙酮与氢气加成生成2-丙醇等. [酰基]无机含氧酸或羧酸分子中去掉羟基(-OH)后剩余的部分.如等. [硝基]亦称“硝酰基 .硝基可以看成是硝酸分子中物如硝基甲烷等的官能团. [磺酸基]亦称“磺基 .是硫酸分子中去掉一个羟基后剩余的部分.用-SO3H来表示.磺酸基与烃基的碳原子直接相连时叫做磺酸.R可入磺酸基后可增加其酸性.又因为磺酸基是亲水性基团.可增加其水溶性. [氨基]氨分子中去掉一个氢原子后剩余的一价原子团.用-NH2来表示. 有机物分子中引入氨基后.其碱性增强. [氰基]亦称“氰根 .由碳.氮两种原子构成的一价原子团.用-C≡N或-CN来表示.无机氰化物及有机腈类物质如丙烯 [偶氮基]系基团-N=N-两端都与烃基的碳原子相连的原子团.有机化分子中都含有偶氮基.偶氮化合物都有颜色.有的可用作染料. [卤原子]卤原子通常是指F.Cl.Br.I等元素.有机化合物如卤代烃.酰卤等分子中都含有卤原子.象溴乙烷和乙酰氯
网址:http://m.1010jiajiao.com/timu_id_3706617[举报]
下列说法中正确的是( )
| A.分子中键能越大,键长越长,则分子越稳定 |
| B.sp3杂化轨道是由同一个原子中能量相近的s 轨道和p轨道混合起来形成的一组能量相近的新轨道 |
| C.PCl5分子中P原子和Cl原子最外层都满足8电子结构 |
| D.用价层电子互斥理论预测H2S和BF3的立体结构,分别为V形和平面正三角形 |
[化学一选修物质结构与性质]
A、B、C、D、E都是短周期主族元素,原子序数依次增大,B、C同周期,A、D同主族,E的单质既可溶于稀硫酸又可溶于氢氧化钠溶液.a、b能形成两种在常温下呈液态的化合物甲和乙,原子个数比分别为2:1和1:1.根据以上信息回答下列1-3问:
(1)C和D的离子中,半径较小的是______ (填离子符号).
(2)实验室在测定C的气态氢化物的相对分子质量时,发现实际测定值比理论值大出许多,其原因是______.
(3)C、D、E可组成离子化合物DxE6其晶胞(晶胞是在晶体中具有代表性的最小重复单元)结构如图所示,阳离子D+(用0表示)位于正方体的棱的中点和正方体内部;阴离子EC6x-(用 示)位于该正方体的顶点和面心,该化合物的化学式是______.
示)位于该正方体的顶点和面心,该化合物的化学式是______.

(4)Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据列于下表:
回答下列问题:
Mn元素价电子层的电子排布式为______,比较两元素的I2J3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难.对此的解释是______;
(5)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物.
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是______.
②六氰合亚铁离子(Fe(CN)64-)中的配体CN-中c原子的杂化轨遣类型是______;
写出一种与CN-互为等电子体的单质分子的路易斯结构式______.
查看习题详情和答案>>
A、B、C、D、E都是短周期主族元素,原子序数依次增大,B、C同周期,A、D同主族,E的单质既可溶于稀硫酸又可溶于氢氧化钠溶液.a、b能形成两种在常温下呈液态的化合物甲和乙,原子个数比分别为2:1和1:1.根据以上信息回答下列1-3问:
(1)C和D的离子中,半径较小的是______ (填离子符号).
(2)实验室在测定C的气态氢化物的相对分子质量时,发现实际测定值比理论值大出许多,其原因是______.
(3)C、D、E可组成离子化合物DxE6其晶胞(晶胞是在晶体中具有代表性的最小重复单元)结构如图所示,阳离子D+(用0表示)位于正方体的棱的中点和正方体内部;阴离子EC6x-(用
 示)位于该正方体的顶点和面心,该化合物的化学式是______.
示)位于该正方体的顶点和面心,该化合物的化学式是______.
(4)Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据列于下表:
| 元素 | Mn | Fe | |
| 电离 能/kj?mol-1[来源:] | Ⅰ1 | 717 | 759 |
| Ⅱ2 | 1509 | 1561 | |
| Ⅲ3 | 3248 | 2957 |
Mn元素价电子层的电子排布式为______,比较两元素的I2J3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难.对此的解释是______;
(5)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物.
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是______.
②六氰合亚铁离子(Fe(CN)64-)中的配体CN-中c原子的杂化轨遣类型是______;
写出一种与CN-互为等电子体的单质分子的路易斯结构式______.
查看习题详情和答案>>
[化学一选修物质结构与性质]
A、B、C、D、E都是短周期主族元素,原子序数依次增大,B、C同周期,A、D同主族,E的单质既可溶于稀硫酸又可溶于氢氧化钠溶液.a、b能形成两种在常温下呈液态的化合物甲和乙,原子个数比分别为2:1和1:1.根据以上信息回答下列1-3问:
(1)C和D的离子中,半径较小的是______ (填离子符号).
(2)实验室在测定C的气态氢化物的相对分子质量时,发现实际测定值比理论值大出许多,其原因是______.
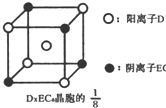
(3)C、D、E可组成离子化合物DxE6其晶胞(晶胞是在晶体中具有代表性的最小重复单元)结构如图所示,阳离子D+(用0表示)位于正方体的棱的中点和正方体内部;阴离子EC6x-(用

示)位于该正方体的顶点和面心,该化合物的化学式是______.
(4)Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据列于下表:
回答下列问题:
Mn元素价电子层的电子排布式为______,比较两元素的I2J3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难.对此的解释是______;
(5)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物.
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是______.
②六氰合亚铁离子(Fe(CN)64-)中的配体CN-中c原子的杂化轨遣类型是______;
写出一种与CN-互为等电子体的单质分子的路易斯结构式______.
查看习题详情和答案>>
A、B、C、D、E都是短周期主族元素,原子序数依次增大,B、C同周期,A、D同主族,E的单质既可溶于稀硫酸又可溶于氢氧化钠溶液.a、b能形成两种在常温下呈液态的化合物甲和乙,原子个数比分别为2:1和1:1.根据以上信息回答下列1-3问:
(1)C和D的离子中,半径较小的是______ (填离子符号).
(2)实验室在测定C的气态氢化物的相对分子质量时,发现实际测定值比理论值大出许多,其原因是______.
(3)C、D、E可组成离子化合物DxE6其晶胞(晶胞是在晶体中具有代表性的最小重复单元)结构如图所示,阳离子D+(用0表示)位于正方体的棱的中点和正方体内部;阴离子EC6x-(用

示)位于该正方体的顶点和面心,该化合物的化学式是______.

(4)Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据列于下表:
| 元素 | Mn | Fe | |
| 电离 能/kj?mol-1[来源:] |
Ⅰ1 | 717 | 759 |
| Ⅱ2 | 1509 | 1561 | |
| Ⅲ3 | 3248 | 2957 |
Mn元素价电子层的电子排布式为______,比较两元素的I2J3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难.对此的解释是______;
(5)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物.
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是______.
②六氰合亚铁离子(Fe(CN)64-)中的配体CN-中c原子的杂化轨遣类型是______;
写出一种与CN-互为等电子体的单质分子的路易斯结构式______.
(2011?西安模拟)[化学一选修物质结构与性质]
A、B、C、D、E都是短周期主族元素,原子序数依次增大,B、C同周期,A、D同主族,E的单质既可溶于稀硫酸又可溶于氢氧化钠溶液.a、b能形成两种在常温下呈液态的化合物甲和乙,原子个数比分别为2:1和1:1.根据以上信息回答下列1-3问:
(1)C和D的离子中,半径较小的是
(2)实验室在测定C的气态氢化物的相对分子质量时,发现实际测定值比理论值大出许多,其原因是
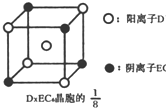
(3)C、D、E可组成离子化合物DxE6其晶胞(晶胞是在晶体中具有代表性的最小重复单元)结构如图所示,阳离子D+(用0表示)位于正方体的棱的中点和正方体内部;阴离子EC6x-(用 示)位于该正方体的顶点和面心,该化合物的化学式是
示)位于该正方体的顶点和面心,该化合物的化学式是
(4)Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据列于下表:
回答下列问题:
Mn元素价电子层的电子排布式为
(5)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物.
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是
②六氰合亚铁离子(Fe(CN)64-)中的配体CN-中c原子的杂化轨遣类型是
写出一种与CN-互为等电子体的单质分子的路易斯结构式
查看习题详情和答案>>
A、B、C、D、E都是短周期主族元素,原子序数依次增大,B、C同周期,A、D同主族,E的单质既可溶于稀硫酸又可溶于氢氧化钠溶液.a、b能形成两种在常温下呈液态的化合物甲和乙,原子个数比分别为2:1和1:1.根据以上信息回答下列1-3问:
(1)C和D的离子中,半径较小的是
Na+
Na+
(填离子符号).(2)实验室在测定C的气态氢化物的相对分子质量时,发现实际测定值比理论值大出许多,其原因是
由于HF中含有氢键相结合的聚合氟化氢分子(HF)n
由于HF中含有氢键相结合的聚合氟化氢分子(HF)n
.(3)C、D、E可组成离子化合物DxE6其晶胞(晶胞是在晶体中具有代表性的最小重复单元)结构如图所示,阳离子D+(用0表示)位于正方体的棱的中点和正方体内部;阴离子EC6x-(用
 示)位于该正方体的顶点和面心,该化合物的化学式是
示)位于该正方体的顶点和面心,该化合物的化学式是Na3AlF6
Na3AlF6
.
(4)Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据列于下表:
| 元素 | Mn | Fe | |
| 电离 能/kJ?mol-1 |
Ⅰ1 | 717 | 759 |
| Ⅱ2 | 1509 | 1561 | |
| Ⅲ3 | 3248 | 2957 |
Mn元素价电子层的电子排布式为
3d54s2
3d54s2
,比较两元素的I2J3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难.对此的解释是由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转为不稳定的3d4状态需要的能量较多;而Fe2+到Fe3+时,3d能级由不稳定的3d6到稳定的3d5半充满状态,需要的能量相对要少
由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转为不稳定的3d4状态需要的能量较多;而Fe2+到Fe3+时,3d能级由不稳定的3d6到稳定的3d5半充满状态,需要的能量相对要少
;(5)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物.
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是
具有弧对电子
具有弧对电子
.②六氰合亚铁离子(Fe(CN)64-)中的配体CN-中c原子的杂化轨遣类型是
sp
sp
;写出一种与CN-互为等电子体的单质分子的路易斯结构式
N≡N
N≡N
.