摘要:[铁]元素符号Fe.原子序数26.原子量55.847.外围电子排布3d64s2.位于第四周期第Ⅷ族.原子半径124.1皮米.离子半径Fe2+74皮米.Fe3+64皮米.第一电离能764千焦/摩尔.电负性1.8.银白色金属.密度7.86克/厘米3.熔点1535℃.沸点2750℃.常见化合价+2.+3.有良好延展性和传热导电性.纯铁容易磁化.也容易去磁.化学性质较活泼.在干燥空气中较稳定.在潮湿空气中易锈蚀.高温时能跟卤素.氧.硫.硅.磷.碳等化合.红热时跟水蒸气反应生成四氧化三铁和氢气.溶于盐酸和稀硫酸生成亚铁盐和氢气.常温下在浓硫酸或浓硝酸中发生钝化.主要用于炼钢.制造铸铁和锻铁.还原铁粉用于冶金.在古代被发现.在地壳中丰度为4.75%.主要铁矿有磁铁矿.赤铁矿.褐铁矿和菱铁矿等.工业用焦炭还原铁矿石制得. [钢]指含碳量小于2%的铁碳合金.根据成分不同.又可分为碳素钢和合金钢.根据性能和用途不同.又可分为结构钢.工具钢和特殊性能钢. [氧化铁]通常指三氧化二铁.化学式Fe2O3.式量159.69.棕红色粉末.俗称铁红.密度5.24克/厘米3.熔点1565℃.不溶于水.不与水反应.跟酸反应.生成铁盐.在高温下可被氢气.一氧化碳等还原成铁.用作颜料.抛光剂.催化剂等.灼烧硫酸亚铁或氢氧化铁制得. [氧化亚铁]化学式FeO.式量71.85.黑色粉末.密度5.7克/厘米3.不稳定.在空气中加热时迅速被氧化成四氧化三铁.溶于盐酸.稀硫酸生成亚铁盐.不溶于水.不与水反应.在隔绝空气条件下加热草酸亚铁制得: FeC2O4=FeO+CO+CO2 [四氧化三铁]化学式Fe3O4.式量231.54.铁在四氧化三铁中有两种化合价.经研究证明了Fe3O4是一种铁(Ⅲ)酸盐.即FeⅡFeⅢ[FeⅢO4].黑色晶体.密度5.18克/厘米3.有磁性.故又称磁性氧化铁.潮湿状态的四氧化三铁在空气中容易氧化成三氧化二铁.不溶于水.溶于酸.用作颜料和抛光剂.磁性氧化铁用于制录音磁带和电讯器材.用红热铁跟水蒸气反应制得. [氢氧化铁]化学式Fe(OH)3.式量106.87.红棕色无定形粉末.密度3.44-3.6克/厘米3.不溶于水.加热时分解成氧化铁和水.略具两性.碱性强于酸性.新制的易溶于酸.稍加放置后则难溶.新制的能溶于强碱溶液生成铁酸盐.用作颜料.药物和砷的解毒剂.由铁盐溶液跟氨水反应制得. [氯化铁]化学式FeCl5.式量162.61.亦称三氯化铁.棕黑色六方晶体.密度2.898克/厘米3.在空气中易吸水潮解.易溶于水.由于水解呈黄褐色.显酸性.能跟水形成2-6个水分子的水合物.FeCl3·6H2O是桔黄色晶体.有氧化性.用作氯化试剂.氧化剂.止血剂.催化剂.印刷制版.制备铁盐和染料等.用盐酸跟氧化铁或用氯气跟氯化亚铁反应制得. [氯化亚铁]化学式FeCl2.式量126.75.绿黄色六方晶体.密度3.16克/厘米3.溶于水和乙醇.由于水解.水溶液显酸性.从饱和溶液析出的晶体是FeCl2·4H2O.浅天蓝色单斜晶体.易潮解.在空气中易被氧化.有还原性.用作还原剂.媒染剂.医药.冶金及污水处理.由过量铁跟盐酸反应制得. [硫酸亚铁]化学式FeSO4.常见的是含七个结晶水的硫酸亚铁FeSO4·7H2O.俗称绿矾.浅蓝绿色单斜晶体.密度1.898克/厘米3.64℃熔于结晶水.溶于水.水溶液显酸性.在空气中逐渐风化.同时被氧化为黄褐色的碱式铁盐.300℃时失去全部结晶水.无水物是白色粉末.有还原性.易被氧化.如被空气氧化时发生下列反应: 4FeSO4+2H2O+O2=4Fe(OH)SO4 强热时.分解为Fe2O3.SO2和SO3.用作还原剂.媒染剂.除草剂.木材防腐剂.净水剂.煤气净化剂.缺铁性贫血的补血剂.植物的杀菌剂.还可用于制备氧化铁.蓝黑墨水等.由铁跟稀硫酸反应制得. [绿矾]见硫酸亚铁条. [黄铁矿]矿物名.又称硫铁矿.主要化学成分为FeS2.等轴晶系.晶体多呈八面体.立方体或五角十二面体.晶面上有条纹.淡黄铜色.有金属光泽.条痕绿黑色.硬度6-6.5.密度4.9-5.1克/厘米3.有弱导电性.主要用于制硫酸. [硫铁矿]见黄铁矿条. [氢氧化亚铁]化学式Fe(OH)2.式量89.866.白色固体.难溶于水.密度3.4克/厘米3.受热易分解.溶于酸.不溶于碱.易被氧化.用碱溶液跟亚铁盐溶液反应可制得.但不易制得纯物.因Fe(OH)2在空气中迅速被氧化.变成灰绿色最后变成棕红色的Fe(OH)3. [硫酸铁]化学式Fe2(SO4)3.式量399.7.浅黄色粉末.密度3.097克/厘米3.在潮湿空气中易潮解.变成棕色溶液.易溶于水.容易水解.溶液显酸性.480℃时分解生成氧化铁和三氧化硫.水合物很多.常见的有九水合物Fe2(SO4)3·9H2O.式量562.01.呈黄色.密度 2.1克/厘米3.在酸性溶液中有较强氧化性.可溶解铁.铜等.用于制颜料.药物.还用作媒染剂.净水剂.用氧化物或氢氧化铁跟硫酸反应制得. [硝酸铁]化学式Fe(NO3)3·9H2O.式量404.02.无色或浅紫色单斜晶体.密度1.63克/厘米3.47.2℃溶于结晶水.在125℃分解.易潮解.溶于水和乙醇.微溶于硝酸.有氧化性.水溶液在紫外线照射下生成硝酸亚铁和氧气.用作化学试剂.催化剂.媒染剂.铜着色剂.医药.用氧化铁跟硝酸反应制得. [硫化亚铁]化学式FeS.式量87.91.深棕色或黑色固体.密度4.74克/厘米3.不溶于水.溶于非氧化性酸产生硫化氢.主要用于制备硫化氢.用铁粉.硫粉混合共热制得. [铁钾矾]化学式K2SO4·Fe2(SO4)3·24H2O.或写作KFe(SO4)2·12H2O.又称硫酸铁钾.俗称铁矾.硫酸铁和硫酸钾的复盐.无色或淡紫色晶体.密度1.83克/厘米3.33℃熔于结晶水.在干燥空气中逐渐风化生成黄白色粉状物.溶于水.难溶于乙醇.80℃时分解为硫酸和碱式硫酸铁钾.主要用作媒染剂.将硫酸钾与硫酸铁溶液混合后结晶制得. [铁矾]见铁钾矾条. [硫酸亚铁铵]化学式(NH4).SO4·FeSO4·6H2O.式量392.18.俗称莫尔盐.是一种复盐.透明淡蓝绿色单斜晶体.密度1.864克/厘米3.100-110℃失去结晶水.有潮解性.溶于水.不溶于乙醇.在空气中比硫酸亚铁稳定.有还原性.用作化学试剂.医药.还用于冶金.电镀等.由硫酸亚铁溶液与硫酸铵溶液混合后.经浓缩.结晶制晶. [莫尔盐]见硫酸亚铁铵条. [铁锈]铁和铁基合金在含有二氧化碳的潮湿空气中受腐蚀生成的红褐色疏松多孔物质.是一种成分不定的混和物.主要成分有氧化铁.水合氧化铁.水合氧化亚铁等.不溶于水.可溶于酸. [铁铵矾]化学式3·24H2O.即硫酸铁铵.式量968.42.无色或淡紫色晶体.密度1.71克/厘米3.230℃时失去结晶水.溶于水.不溶于乙醇.用作化学试剂和媒染剂.由硫酸铁与硫酸铵溶液混合后.浓缩.结晶制得. [铁合金]炼钢用原料.在炼钢时作为脱氧剂与合金元素添加剂加入钢水中.常用的有硅铁.锰铁.铬铁等.铁合金比纯金属熔点低.比重大.容易加入钢水中.同时生产铁合金比生产纯金属简单经济.所以生产熔炼合金钢时.各合金元素多以铁合金状态加入. [生铁]铁碳合金.一般把含碳量在2-4.3%的铁碳合金叫做生铁.在高炉冶炼过程中.常将铁矿石和焦炭中的硫.磷.硅等带入生铁内.因而使生铁有脆性.生铁产量的90%用于炼钢.10%用于铸造. [白口铁]生铁中的一种.含碳量约2.5%.硅在1%以下.白口铁中的碳以碳化铁Fe3C存在.断面呈白色.质硬且脆.不易进行机械加工.主要用炼钢. [灰口铁]生铁中的一种.含碳量约3%.含硅约2%.灰口铁中碳以片状石墨状态存在.断面呈深灰色.质较软.可进行切削加工.热时容易流动.铸造性能好.较耐磨.强度及延展性差.主要用于铸造. [球墨铸铁]生铁中的一种.球墨铸铁中碳形成球状石墨.它的抗张强度.延展性都优于灰口铁.硬度高.因此.球墨铸铁可代替一部钢制造内燃机汽缸.汽缸套.大齿轮.金).再加入硅铁.使石墨完全球化. [合金钢]又叫特种钢.除铁.碳以外.还含有一种或多种一定量的合金元素的钢.合金元素有硅.锰.钼.镍.铬.钒.钛.铌.硼.钨和稀土元素等.按照合金元素种类可分为:镍钢.铬钢.锰钢.钨钢.镍铬钢.硅钢等.按照合金元素的多少可分为:高合金钢.中合金钢和低合金钢.根据用途不同可分为:合金工具钢.合金结构钢和特种合金钢等.不同的合金钢具有不同的特性. [不锈钢]能抵抗空气.水及一般酸.碱.盐等腐蚀作用的合金钢的总称.主要是含铬合金钢.常用的有铬不锈钢和镍铬不锈钢两类.铬在钢中能提高钢的硬度.耐热性和耐腐蚀性.镍在钢中能提高钢的强度和韧性.所以镍铬不锈钢的耐腐蚀性和机械加工性能更优良.广泛用于制汽轮机和化工设备. [特种钢]见合金钢条. [赤铁矿]矿物名.主要化学成分为Fe2O3.三方晶系.晶体呈片状或菱面体状集合体.常呈致密块状或肾状.结晶质的赤铁矿呈铁黑至钢灰色,有金属或半金属光泽.胶态赤铁矿呈赭红色.无光泽.条痕均呈樱红色.硬度5.5-6.0.密度5-5.3克/厘米3.产于沉积矿床及各式内生矿床中.是炼铁的重要原料. [磁铁矿]矿物名.主要化学成分是Fe3O4.等轴晶系.晶体常呈八面体和菱形十二面体.集合体呈粒状或块状.铁黑色.条痕呈黑色.金属光泽或半金属光泽.硬度5.6-6.密度4.9-5.2克/厘米3.有强磁性.生于变质矿床和内生矿床中.氧化后变为赤铁矿或褐铁矿.是炼铁的重要原料. [钛铁矿]矿物名.主要化学成分为FeTiO3.三方晶系.晶体呈厚板状.菱面体状或不规则粒状.铁黑色或钢灰色.条痕黑色至棕红色.半金属光泽.微带磁性.硬度5-6.密度4.7-5.0克/厘米3.常和磁铁矿共生.是炼钛铁合金和制钛白的主要原料. [钴]元素符号Co.原子序数27.原子量58.93.外围电子排布3d74s2.位于第四周期Ⅷ族.金属半径125.3皮米.第一电离能763千焦/摩尔.电负性1.8.主要氧化数+1.+3.+4.银白色金属.硬而有延展性.具有铁磁性.密度8.9克/厘米3.熔点1495℃.沸点2870℃.常温下不跟空气.水反应.白热时燃烧生成四氧化三钴.也能分解水蒸气.能跟卤素直接化合.能溶解于盐酸.硫酸和硝酸中.能被氢氟酸.氨水和氢氧化钠溶液缓慢侵蚀.用于制超硬耐热合金.磁性合金和切削工具用合金.同位素60Co是一种放射源.用于医疗.科研和生产中.1735年瑞典人布朗特煅烧钻矿得到钴.主要钴矿有辉钴矿.砷钴矿.先将钴矿转化为氧化钴.然后用铝还原制取钴. [氯化钴]别名氯化亚钴或二氯化钴.化学式CoCl2.式量129.83.无水物为蓝色六方晶体.结晶水合物中由于结晶水数不同而呈不同颜色.它们的相互转变温度及特征颜色如下: 易潮解.易溶于水.乙醇.水溶液呈粉红色.密度3.356克/厘米3.熔点724℃.沸点1049℃.用作分析试剂.氨的吸收剂.还用硅胶吸湿情况的指示剂.由钴跟氯气直接反应可制得. [硝酸钴]别名硝酸亚钴.化学式Co(NO3)2·6H2O.式量291.03.红色晶体.有潮解性.易溶于水和乙醇.微溶于氨水.有强氧化性.与有机物摩擦和撞击能引起燃烧和爆炸.55℃时熔于结晶水.用作分析试剂.测定钾.用于制催化剂.蓝宝石抛光膏等.由钴跟硝酸反应或由碱式碳酸钴跟硝酸反应制得. [氧化高钴]别名三氧化二钴.化学式Co2O3.式量165.86.灰黑色结晶性粉末.溶于热盐酸或热稀硫酸.分别放出氯气和氧气.不溶于水和醇.熔点895℃.用作分析试剂.氧化剂.催化剂.还用于制取钴或钴盐.在空气中加热碳酸钴可制得三氧化二钴. [三氧化二钴]见氧化高钴条. [镍]元素符号Ni.原子序数28.原子量58.71.外围电子排布3d84s2.位于第四周期第Ⅷ族.金属半径124.6皮米.第一电离能741.1千焦/摩尔.电负性1.8.主要氧化数+2.+3.+4.银白色金属.有良好延展性.具有中等硬度.有铁磁性.密度 8.902克/厘米3.熔点1453℃.沸点2732℃.化学性质较活泼.有较好的耐腐蚀性.室温时在空气中难氧化.不易与浓硝酸反应.能耐碱腐蚀.细镍丝可燃.加热时与卤素反应.在稀酸中缓慢溶解.能吸收相当数量氢气.用于制不锈钢.抗腐蚀合金.蓄电池.化学器皿.陶瓷制品.还用作催化剂.1751年瑞典人克朗斯埃特首先从红砷镍矿制得镍.主要矿物有红砷镍矿.针镍矿等.矿石经煅烧成氧化物后.再用水煤气或炭还原得到镍. [一氧化镍]别名氧化镍或氧化亚镍.化学式NiO.式量74.71.绿色立方晶体或绿色粉末.密度6.67克/厘米3.熔点1984℃.不溶于水或醇.可溶于酸或氨水.用作催化剂.电子元件材料.蓄电池材料.搪瓷涂料.制备镍盐.用镍在空气中加热或者用草酸镍在隔绝空气条件下加热分解制得. [氧化镍]见一氧化镍条. [氧化亚镍]见一氧化镍条. [硫酸镍]化学式NiSO4·7H2O.式量280.88.亮绿色菱形晶体.俗称翠矾.密度1.948克/厘米3.于31.5℃时失去1分子结晶水.99℃时熔于结晶水中.278.4℃时失全部结晶水.无水硫酸镍为淡黄色晶体.七水合硫酸镍在干燥空气中易风化.溶于水.水溶液呈酸性.能跟碱金属或铵的硫酸盐作用生成水合复盐.用作加氢催化剂.媒染剂.配电镀液.由镍或氧化镍溶于稀硫酸制得. [硝酸镍]化学式Ni(NO3)2·6H2O.式量290.81.绿色单斜晶体.有潮解性.在干燥空气中微风化.易溶于水.水溶液呈酸性.溶于乙醇.密度2.05克/厘米3.56.7℃熔于结晶水中.沸点136.7℃.有氧化性.用作催化剂.镀镍.由镍溶于稀硝酸制得. [钌]元素符号Ru.原子序数44.原子量101.1.外围电子排布4d75s1.位于第五周期第Ⅷ族.银白色有金属光泽金属.很硬.冷时延展性小.密度12.30克/厘米3.熔点2310℃.沸点2900℃.第一电离能716千焦/摩尔.电负性2.2.主要氧化数+2.+4.+6.+7.+8.化学性质很稳定.不被普通酸.王水侵蚀.室温下氯水.溴水.碘酒能轻微腐蚀钌.能与熔融的碱.碳酸盐反应.用作铂和钯的硬化剂.钌合金用于电气接触点以及钢笔尖和工具枢轴上.还用作氢化.异构化.氧化和重整的催化剂.1844年俄国人克劳斯从铂矿渣里制得钌.分布极为分散.常与铂.铱.钯.锇共存.从天然铂金属合金中提取. [铑]元素符号Rh.原子序数45.原子量102.9.外围电子排布4d85s1.位于第五周期第Ⅷ族.第一电离能724千焦/摩尔.电负性2.2.主要氧化数+2.+4.+6.银白色金属.很硬.但有相当的延展性.密度12.41克/厘米3.熔点1966±3℃.沸点3727±100℃.在常温下在空气中稳定保持光亮.加热时形成氧化物保护膜.不跟普通酸和王水反应.在200-600℃时能跟卤素.浓硫酸.氢溴酸.次氯酸钠反应.能和熔融的酸式硫酸盐.碱金属硝酸盐反应.用于制铂铑合金.电热丝.热电偶.用于镀反光镜.宝石的抛光剂.催化剂.电器的接触部件.1803-1804年英国人武拉斯顿在提炼钯铂的废渣中发现了铑.存在于铂矿中.用氢气还原氯化铑制得. [锇]元素符号Os.原子序数76.原子量190.2.外围电子排布5d66s2.位于第六周期Ⅷ族.蓝灰色金属.六方密堆积晶体.非常硬.密度为 22.57克/厘米3.金属中密度最大.熔点3045±30℃.沸点5027±100℃.原子半径134皮米.第一电离能842千焦/摩尔.电负性2.2.主要氧化数+2.+3.+4.+6.+8.具有硬度高.难熔.耐磨.耐腐蚀的特性.在室温时易形成蓝色氧化膜.受热时氧化生成四氧化锇OsO4.能溶于热浓硝酸.浓硫酸.溶于次氯酸钠溶液生成锇酸钠.用来制超高硬度耐磨耐腐蚀的合金.用于仪器枢轴.电器插头.电唱机针.钢笔尖等.还用作催化剂.1803年英国人台奈特从铂矿中发现了锇.存在于锇铱矿中.用氢气还原其硫化物或氢氧化物制得. [铱]元素符号Ir.原子序数77.原子量192.22.外围电子排布5d76s2.位于第六周期第Ⅷ族.原子半径135.7皮米.第一电离能885千焦/摩尔.电负性2.2.主要氧化数+3.+4.+6.银白色金属.硬度很大.质脆.加热时有良好延展性.密度22.42克/厘米3.熔点2410℃.沸点4130℃.化学性质很稳定.常温下耐腐蚀性很强.不溶于酸.稍溶于王水和熔融碱.1803年由英国人台奈特等发现.纯铱用在飞机火花塞中.还用于制造科学仪器.热电偶.电阻丝.自来水笔尖.耐高温合金.催化剂.国际标准米尺用铂铱合金制成.主要存在于锇铱矿和铂矿中.从分离矿石中制得. [铂]元素符号Pt.原子序数78.原子量195.09.外围电子排布5d96s1.位于第六周期第Ⅷ族.原子半径138皮米.第一电离能868.4千焦/摩尔.电负性2.2.主要氧化数+2.+4.俗称白金.银白色金属.面心立方体晶体.质柔软.有良好的延展性.密度21.45克/厘米3.熔点1772℃.沸点3827±100℃.化学性质稳定.常温下不锈蚀.不受一般酸碱侵蚀.能溶于王水和熔融碱.还溶于盐酸和过氧化氢.盐酸和高氯酸的混合物中.粉状铂能吸收氢气.氧气和一氧化碳.用作催化剂.热电偶.电极.喷丝嘴.电阻温度计.化学仪器.首饰等.西班牙人乌罗阿和武德分别于1935年和1941 年发现了铂主要以游离态和合金形式存在.主要矿物有铂矿和锇铱矿.极分散.由分离铂矿获得. [白金]见铂条. [四氯化铂]化学式PtCl.式量336.9.棕红色晶体.密度4.303克/厘米3.370℃时分解为二氯化铂和氯气.有吸湿性.能溶于水.微溶于乙醇.溶于盐酸生成氯铂(氢)酸.自水溶液中析出时可得到含有5个结晶水的晶体.晶体为红色晶体.密度为2.43克/厘米3.用作分析试剂.催化剂.由氯铂(氢)酸在氯气流中加热而制得. [氯铂酸]也叫氢氯铂酸.化学式HPtCl6.一般为含六个结晶水的晶体H2PtCl6·6H2O.式量517.92.红棕色晶体.密度2.431克/厘米3.60℃时熔于结晶水.易溶于水.乙醇.灼烧或电解后即得到铂黑.用作化学分析试剂.检验钾.铵等离子.将铂溶于含有过量盐酸的王水中或将四氯化铂溶于盐酸制得. [铂黑]元素符号Pt.原子量195.05.黑色粉末.在0℃时能吸附大量氢气.不溶于无机酸或有机酸.可溶于王水.用作催化剂.气体吸收剂.灼烧或电解氯铂酸可制得铂黑. [铂石棉]附有铂的灰黑色石棉纤维.能液于王水.用作催化剂.气体分析中用作氢的吸收剂.将石棉浸入氯铂酸或氯铂酸铵溶液中取出灼烧即得铂石棉. [钯]元素符号Pd.原子序数46.原子量106.4.外围电子排布4d105s0.位于第五周期第Ⅷ族.原子半径137.6皮米.第一电离能809千焦/摩尔.电负性2.2.主要氧化数+2.+4.银白色金属.柔软.有延展性.密度12.02克/厘米3.熔点1552℃.沸点3140℃.化学性质不活泼.常温下不跟盐酸.硫酸.氢氟酸反应.能被潮湿的氯.溴.碘侵蚀.易与硝酸.王水.三氯化铁.次氯酸盐.以及熔融碱反应.容易吸收氢.氧等气体.室温101.33帕.1体积海绵状钯可吸收800体积左右的氢气.制成合金用于热电偶.电阻器.钟表零件.补牙.还用作加氢.脱氢.异构化和裂变反应的催化剂.1803年英国人武拉斯顿分离粗铂时得到钯.存在于铂矿中.从分离铂矿中获得. [铜]元素符号Cu.原子序数29.原子量63.55.外围电子排布3d104s1.位于第四周期IB族.原子半径127.8皮米.Cu2+半径72皮米.第一电离能为750千焦/摩尔.电负性1.9.常见氧化数+1.+2.紫红色有光泽的金属.有良好的延展性和传热.导电性.密度8.96克/厘米3.熔点1083.4±0.2℃.沸点2567℃.化学性质不很活泼.在干燥空气中稳定.在含有二氧化碳的潮湿空气中易生成碱式碳酸铜.俗称铜绿.加热时跟氧生成氧化铜.跟卤素反应生成卤化铜.加热时跟硫反应生成硫化亚铜.不与水反应.不溶于稀盐酸和稀硫酸.可溶于硝酸和热浓硫酸.也能溶于浓盐酸生成H2CuCl3和H2.缓慢溶于氨水.容易被碱侵蚀.主要用于电器工业.如制电线.电缆.各种电器设备.也用于制各种合金.如黄铜.青铜.白铜等.也用于电镀.古代就发现了铜.主要矿物有黄铜矿.赤铜矿2CO3).铜矿石经冶炼得粗铜.最后经电解精炼得纯铜. [氧化铜]化学式CuO.式量79.54.黑色立方晶体.密度 6.4克/厘米3.熔点1326℃.不溶于水.溶于稀酸.氰化钾与碳酸铵溶液.缓慢溶于氨水.在1000℃以上分解为氧化亚铜与氧气.加热时易被氢.碳.一氧化碳.氨等还原为铜.可用作制玻璃或瓷器的着色剂.有机合成的催化剂.油类的脱硫剂.还用于气体分析.由碳酸铜或硝酸铜受热分解制得. [氢氧化铜]化学式Cu(OH)2.式量97.56.淡蓝色粉末状晶体.密度3.368克/厘米3.难溶于水.受热易分解为氧化铜和水.微显两性.既溶于酸又溶于氨水和浓碱溶液 Cu(OH)2+2NaOH=Na2[Cu(OH)4] Cu4](OH)* 用作媒染剂.颜料.纸张着色.由铜盐溶液和碱溶液反应制得. [硫酸铜]化学式CuSO4.式量159.6.白色粉末.密度3.608克/厘米3.有强吸水性.吸水后变蓝.生成五水硫酸铜.在650℃时分解为氧化铜和三氧化硫.常见的是五水合硫酸铜蓝色晶体CuSO4·5H2O.俗称胆矾或蓝矾.三斜晶体.晶体中四个水分子以配位键与Cu2+结合.一个水分子以氢键与硫酸根离子结合.易溶于水.在干燥空气中易风化.可用作媒染剂.杀虫剂.杀菌剂.还用于镀铜.由氧化铜跟稀硫酸反应.再经浓缩结晶可制得胆矾. [胆矾]见硫酸铜条. [氯化铜]化学式CuCl2.式量134.44.棕黄色粉状结晶.共价化合物.密度 3.386克/厘米3.熔点620℃.993℃分解为氯化亚铜.有毒!易潮解.易溶于水.很浓的溶液显黄绿色.稀溶液显蓝色.黄色是由于[CuCl4]2-络离子存在.蓝色是由于有[Cu(H2O)4]2+的存在.两者共存时显绿色.CuCl2·2H2O为蓝绿色斜方晶体.易潮解.受热分解失去氯化氢生成碱式盐Cu(OH)2·CuCl2.用作化学试剂.氧化剂.媒染剂.木材防腐剂.还用于石油馏分的脱硫.脱臭.由铜跟氯直接化合或由碱式碳酸铜跟盐酸反应制得. [硝酸铜]常见的是三水合硝酸铜Cu(NO3)2·3H2O.式量241.60.蓝色柱状晶体.密度2.32克/厘米3.易溶于水.易潮解.加热至170℃时失去硝酸生成碱式硝酸铜.加热至200℃分解为氧化铜.有氧化性.与碳.硫等物混和撞击容易爆炸或燃烧.用于镀铜.制农药和搪瓷及染料等.由铜或氧化铜与稀硝酸反应制得. [碱式碳酸铜]化学式Cu2(OH)2CO3.式量221.11.俗称碳酸铜或铜绿.是铜锈的主要成分.绿色无定形粉末.密度4.0克/厘米3.有毒.不溶于水.在200℃时分解成氧化铜.水和二氧化碳.溶于酸生成铜盐和二氧化碳.用作颜料.杀虫剂.饲料添加剂.磷毒的解毒剂.还用制烟火.由碳酸钠溶液跟硫酸铜溶液反应制得. [碳酸铜]见碱式碳酸铜条. [氧化亚铜]化学式Cu2O.式量143.08.由于晶体微粒大小不同.呈现多种颜色.如橙黄.鲜红.深棕色.密度6.0克/厘米3.熔点1235℃.不溶于水.在潮湿空气中易氧化.有毒.溶于稀硫酸.立即发生岐化反应: Cu2O+H2SO4=Cu2+SO4+H2O Cu2SO4=CuSO4+Cu 溶于氢卤酸生成无色络合物H[CuX2].溶于氨水生成无色趼绾衔铮跜u(NH3)2]+.很快被空气中氧气氧化成蓝色的[Cu(NH3)4]2+.用作玻璃或陶瓷的红色颜料.制作整流器材料.有机合成用催化剂.农业用作催化剂.实验室由含酒石酸钾钠的硫酸铜溶液用葡萄糖还原制得. [硫化铜]化学式CuS.式量95.612.黑色单斜或六方晶体.有金属光泽.密度4.6克/厘米3.熔点103℃.难溶于水.不溶于一般稀酸.溶于热的稀硝酸.生成硝酸铜.一氧化氮.硫.溶于氰化钾溶液.生成K3[Cu2.有天然矿物.用于提炼铜或制铜化合物.实验室将硫化氢通入硫酸铜溶液制得. [硫化亚铜]化学式Cu2S.式量159.15.灰黑色有光泽的结晶或粉末.对热稳定.导电性好.不溶于水和稀酸.溶于氨水.跟硝酸反应生成硝酸铜.硫和一氧化氮.熔点1130℃.有毒.用作催化剂.由过量铜跟硫共热制得.或者在硫酸铜溶液中加入硫代硫酸钠溶液共热也可制得. [孔雀石]化学式Cu2(OH)2CO3或CuCO3·Cu(OH)2.由铜的碱式盐组成.单斜晶系.晶体呈针状.通常为放射状或钟乳状集合体.绿色.有玻璃光泽或金刚光泽.硬度3.5-4,性脆.密度3.9-4.0克/厘米3.产在含铜硫化物矿床的氧化带.块大色美的孔雀石.可琢磨成各种装饰品.粉末用作颜料.遇酸产生二氧化碳并生成铜盐.还用于提炼铜和制备铜盐. [自然铜]矿物名.化学成分为Cu.等轴晶系.晶体少见.集合体常为不规的则树枝状.鳞片状及粒状.铜红色.富延展性.有良好导电导热性.自然铜为各种地质作用中还原条件下的产物.与赤铜矿.孔雀石矿共生.是一种铜矿石. [黄铜矿]含铜的主要矿石.化学成分CuFeS2.常以黄铜色块状存在.具有强烈金属光泽.正方晶系.性脆.解理不完全.密度4.1-4.3克/厘米3.硬度3.5-4.0.不溶于水.溶于硝酸.用于炼铜和制备铜化合物. [黄铜]铜与锌形成的合金.含铜64-67%.含锌33-36%.杂质少于0.3%.有良好可塑性和耐腐蚀性.如还含有一种或几种其它合金元素叫特种黄铜.具有较高的硬度.强度.耐磨性.耐腐蚀性.用于铸造机器零件.制造管材.板材.棒材等.军工用于制枪弹弹壳等. [青铜]通常指锡青铜.铜.锡为主形成的合金.含铜81-87%.含锡3-4.5%.锌5-7%.铅4-6%.有良好的铸造性能.抗磨性.抗腐蚀性.用于制轴承.阀门.小齿轮.钟表弹簧.热交换器等.此外.铜与铍.铝.锰.硅.磷等组成的二元或多元合金通常称为特种青铜.如铍青铜.磷青铜等.一般有良好的润滑性.高导电性.耐腐蚀性.用于制轴承.齿轮.连杆.仪器零件.板材.管材.棒材以及艺术器等. [白铜]铜.镍为主形成的合金.含铜78.5-80.5%.镍和钴18-20%.银白色.耐磨性和耐腐蚀性能好.用作医疗器械.精密机械.化工设备零件.日用品等. [铜绿]铜与含有二氧化碳的潮湿空气接触时.表面生成的绿锈.主要成分是碱式碳酸铜Cu2(OH)2CO3.有毒.易溶于酸和氨水. [银]元素符号Ag.原子序数47.原子量107.9.外围电子排布4d105s1.位于第五周期IB族.原子半径144.4皮米.Ag半径126皮米.第一电离能735千焦/摩尔.电负性1.9.银白色有光泽金属.柔软.有良好延展性和传热导电性.密度10.5克/厘米3.熔点961.93℃.沸点2213℃.化学性质稳定.不跟氧气和水反应.不与盐酸.稀硫酸和强碱反应.能溶于硝酸或热浓硫酸.在有空气和氧存在时溶于氰化钾溶液.能跟硫或硫化氢反应.在古代就发现了银.银矿主要有辉银矿Ag2S.角银矿AgCl.有自然银.用于制合金.银箔.电路上的接触点.银焊剂.蓄电池.科学仪器.银币.首饰以及用于电镀.由银矿以氰化钠溶液浸出.再加锌使银沉淀出来. [硝酸银]化学式AgNO3.式量 169.87.无色晶体.密度4.352克/厘米3.熔点212℃.有苦味.易溶于水.444℃时分解成银.二氧化氮和氧气.如有微量的有机物存在或在日光照射下逐渐分解变黑(分解出银.微粒银呈黑色).遇蛋白质变黑色蛋白银.有毒!有腐蚀性.有氧化性.用作照像乳剂.化学试剂.药物.镀银.制镜.将银溶于硝酸.经浓缩.结晶制得. [溴化银]化学式AgBr.式量187.78.黄色立方晶体.密度6.473克/厘米3.熔点432℃.加热到1300℃以上即可分解.不溶于水.乙醇和酸.溶于氰化钾.硫代硫酸钠溶液.还溶于饱和溴化钾溶液.有感光性.遇光分解.形成极小颗粒银核.含银核的溴化银易被还原剂还原为金属银而呈黑色.用于制摄影胶卷和感光纸.在暗室红光下在硝酸银溶液中加入溴化钾溶液制得. [氯化银]化学式AgCl.式量143.32.白色立方晶体.熔点455℃.沸点1550℃.难溶于水.溶于氨水.硫代硫酸钠溶液.用于照像.镀银.和医药.在盐酸或食盐水中加入硝酸银溶液制得. [氧化银]化学式Ag2O.式量231.74.褐色固体.密度7.143克/厘米3.300℃时完全分解生成银和氧气.略溶于水.极易溶于硝酸.氨水.硫代硫酸钠及氰化钾溶液.其氨溶液用完要及时处理.久置会析出强烈爆炸性的黑色晶体--氮化银或亚氨化银.用作氧化剂.玻璃着色剂.由硝酸银溶液跟氢氧化钠溶液反应制得. [碘化银]化学式AgI.式量234.77.有α黄色立方和β橙色立方两种晶体.α晶体密度5.683克/厘米3.于146℃转化为β型.后者密度为 6.010克/厘米3.熔点558℃.沸点1506℃.见光分解变黑.不溶于水.微溶于氨水.易溶于氰化钾溶液或硫代硫酸钠溶液.用于制照像底片或感光纸.还用于人工降雨.在暗室中或红光下在硝酸银溶液中加入碘化钾溶液.过滤.再用热水洗涤制得. [硫酸银]化学式Ag2SO4.式量311.8.无色结晶或白色结晶性粉末.密度 5.45克/厘米3.熔点652℃.1085℃时分解.微溶于水.溶于硝酸.氨水和浓硫酸.见光逐渐变黑.用作化学试剂.由硝酸银溶液与硫酸铵溶液反应制得. [碳酸银]化学式Ag2CO3.式量275.75.新制得的为浅黄色粉末.久置色变暗.感光性很强.不溶于水和醇.溶于氨水.稀硝酸.氰化钾和硫代硫酸钠溶液.用作分析试剂.镀银. [磷酸银]化学式Ag3PO4.式量418.58.黄色立方晶体.密度6.370克/厘米3.熔点849℃.加热或在日光照射下变为棕色.溶于硝酸.氨水.氰化钾.微溶于水.用于制溴化银.碘化银乳剂.由硝酸银溶液跟磷酸钠溶液反应制得. [硫化银]化学式Ag2S.式量247.8.黑色立方晶体.不溶于水和氨水.溶于浓硝酸.用于制陶瓷.将硫化氢通入硝酸银溶液可制得. [金]元素符号Au.原子序数79.原子量197.0.外围电子排布5d106s1.位于第六周期IB族.原子半径144.2皮米.第一电离能895千焦/摩尔.电负性2.4.金黄色有光泽金属.质柔软.富有延展性.1克金可拉成3000米金丝.可锤成只有0.00001毫米厚的半透明金箔.有良好的传热.导电性.密度 18.88克/厘米3.熔点1064.43℃.沸点为3080℃.主要氧化数+1.+3.化学性质很不活泼.在空气中不被氧化.不跟水.酸或强碱溶液反应.能溶于王水生成氯金酸HAuCl4.有氧存在时溶于氰化钾或氰化钠溶液.如: 4Au+8NaCN+2H2O+O2=4Na[Au(CN)2]+4NaOH 跟溴在常温下反应.与氟.氯.碘和碲在高温下反应.古代已发现并应用金.用作晶体管的部件.电接触合金.医药.装饰合金.大部用于货币和工艺品.在地球上分布广而稀少.多以游离态自然金形式存在.也有化合态的如碲金矿AuTe2.主要从岩脉金和冲积金矿提取. [三氯化金]也称氯化金.化学式AuCl3.式量303.33.紫红色晶体.密度3.9克/厘米3.熔点254℃.沸点265℃.易潮解.溶于水.乙醇和乙醚中.有氧化性.用于镀金.药物.摄影.将金跟过量氯气共热制得. [氯金酸]化学式AuCl3·HCl·4H2O.式量411.85.金黄色或橙黄色针状晶体.易潮解.在干燥空气中失去一个水分子.溶于水也溶于乙醇和乙醚.见光出现黑色斑点.有腐蚀性.从乙醇溶液中可结晶出无水氯金酸.用作分析试剂.铷.铯的微量分析,制备红色玻璃.还用于镀金.照像材料.将金溶于王水.蒸发除去盐酸而制得. [氢氧化金]化学式Au(OH)3.式量248.02.黄棕色固体.不溶于水.两性氢氧化物.溶于大多数酸,溶于过量强碱溶液.形成络合氢氧金酸盐.微热时分解生成三氧化二金.易还原成金属金.用于镀金.陶瓷着色等.由氯化金溶液跟氢氧化钠溶液反应制得. [氧化金]别名三氧化二金.化学式Au2O3.式量495.98.棕色粉末.不溶于水.两性氧化物.溶于盐酸和氢氧化钠溶液.见光逐渐分解.160℃时分解成Au2O.250℃时分解为金和氧.用于镀金.瓷器上釉等.将氢氧化金微热可制得. [锌]元素符号Zn.原子序数30.原子量65.38.外围电子排布3d104s2.位于第四周期ⅡB族.原子半径125皮米.第一电离能915千焦/摩尔.电负性1.6.主要氧化数+2.银白略带蓝色有光泽金属.硬度2.5.有延展性.良好的传热.导电性.密度为7.14克/厘米3.熔点419.58℃.沸点907℃.化学性质比较活泼.室温时在空气中较稳定.在潮湿空气中生成一层灰色碱式碳酸锌.可作保护膜.锌燃烧时有蓝绿色火焰.高温时跟水蒸汽反应放出氢气.加热时可跟卤素.硫等反应.易与酸反应.但高纯锌反应慢.若加入少量硫酸铜溶液.或跟铜.镍.铂等金属接触时.反应加快.溶于强碱溶液.生成锌酸盐.如: Zn+2NaOH=Na2ZnO2+H2↑ 溶于氨水和铵盐溶液中.如: Zn+2NH4Cl=Zn(NH3)2Cl2+H2↑ 主要用于制合金.金属表面镀锌.还用于制于电池.焰火.作催化剂和还原剂.我国明代以前已发现并使用锌.主要矿物有闪锌矿ZnS.菱锌矿ZnCO3等.先将矿石煅烧变成氧化锌.再用焦炭还原氧化锌制得. [氧化锌]化学式ZnO.式量81.37.俗名锌白.白色六方晶体或粉末.密度5.606克/厘米3.熔点1975℃.难溶于水.加热时变黄.冷却后仍为白色.两性氧化物.溶于酸生成锌盐.溶于强碱溶液生成锌酸盐.还能溶于氯化铵溶液.用作油漆颜料.橡胶填料.制药.粘合剂.釉药.橡皮膏.由锌在空气中燃烧制得. [硫酸锌]常见的是七水合硫酸锌ZnSO4·7H2O.俗称皓矾.式量287.54.无色晶体.密度 1.957克/厘米3.熔点100℃.易溶于水.280℃时失去结晶水成无水物.600℃时分解成氧化锌.溶于水.水溶液显酸性.用作媒染剂.收敛剂.杀菌剂.木材防腐剂.纸张漂白剂.饲料填加剂.镀锌.治疗缺锌的药剂.由锌与稀硫酸反应制得. [氯化锌]化学式 ZnCl.式量136.28.白色固体.密度2.91克/厘米3.熔点283℃.沸点732℃.易潮解.易溶于水.高温时浓的氯化锌溶液有溶解金属氧化物的能力.用作媒染剂.有抗合成的脱水剂和催化剂.牙科用作粘合剂.用于饲料添加剂.还用于镀锌.制干电池.石油炼制.焊药水.用盐酸溶解锌或氧化锌制得.经干燥脱水得无水物. [氢氧化锌]化学式Zn(OH)2.式量99.38.无色斜方晶体.密度3.053克/厘米3.难溶于水.125℃时分解为氧化锌和水.是两性氢氧化物.溶于强酸生成锌盐.溶于强碱生成锌酸盐.和氢氧化铝不同.能溶于氨水中生成锌氨络离子: Zn4]2++20H- 甭缋用作橡胶填加剂.外科药膏.由锌盐溶液加入适量强碱溶液制得. [锌白]见氧化锌条. [硫化锌]化学式ZnS.式量97.43.白色或微黄色粉末.α变体为无色六方晶体.密度3.98克/厘米3.熔点1700±28℃,β变体为无色立方晶体.密度4.102克/厘米3.于1020℃转化为α型.不溶于水.易溶于酸.见阳光色变暗.久置潮湿空气中转变为硫酸锌.若在晶体ZnS中加入微量的Cu.Mn.Ag做活化剂.经光照后.能发出不同颜色的荧光.用作分析试剂.涂料.制油漆.白色和不透明玻璃.充填橡胶.塑料.以及用于制备荧光粉.由硫跟锌共热制得. [磷化锌]化学式Zn3P2.式量258.08.深灰色四方晶体.有恶臭.密度 4.55克/厘米3.熔点高于420℃.干燥时较稳定.在空气中易吸水分解.放出剧毒的磷化氢气体.不溶于醇.可溶于酸.跟水反应可生成磷化氢和联膦P2H4的混和物.这混和物在空气中能自燃.用作杀鼠剂.也可用作海上照明灯.由锌粉跟红磷在500-600℃时反应制得. [硝酸锌]化学式Zn(NO3)2·6H2O.式量297.47.无色晶体.易潮解.易溶于水和乙醇.水溶液显酸性.36.4℃熔于结晶水.105℃时失去结晶水.有氧化性.与有机物摩擦或撞击能引起燃烧或爆炸.用作分析试剂和制药.将氧化锌溶于硝酸制得. [锌钡白]俗称立德粉.是硫化锌跟硫酸钡的混合晶体.是一种优良的白色颜料.由硫酸锌溶液跟硫化钡溶液混合制得: ZnSO4=ZnS·BaSO4↓ [皓矾]见硫酸锌条. [镉]元素符号Cd.原子序数48.原子量112.4.外围电子排布4d105s2.位于第五周期ⅡB族.原子半径141皮米.第一电离能873千焦/摩尔.电负性1.69.微带蓝色的银白色金属.粉末状的呈灰白色.较软.有延展性.密度8.65克/厘米3.熔点320.9℃.沸点765℃.氧化数+2.在空气中迅速生成一层氧化物薄膜并失去光泽.起保护作用.能溶于大多数酸中生成镉盐.用于电镀.轴承.制低熔合金.硬焊合金.制电池.磷光体等.还用于原子反应堆的中子吸收棒.1817年德国人斯特罗迈厄发现了镉.在自然界常与锌伴生.主要矿石是硫镉矿CdS.工业上主要从锌冶炼的副产物中提取. [硫化镉]化学式CdS.式量144.46.晶体有两种.α-式呈柠檬黄色粉末.β-式呈桔红色粉末.微溶于水.溶于酸.极易溶于氨水.可用于制焰火.玻璃釉.瓷釉.发光材料.颜料.高纯度硫化镉是良好的半导体.对可见光有强烈的光电效应.可用于制光电管.太阳能电池.将硫化氢通入镉盐的酸溶液中制取. [硝酸镉]化学式Cd(NO3)2·4H2O.式量308.47.白色针状或棱状晶体.密度2.455克/厘米3.59.4℃熔于结晶水.70-80℃时失去结晶水变成无水物.其熔点为350℃.当温度再升高时分解为氧化镉.二氧化氮和氧气.易潮解.溶于水和乙醇.水溶液显酸性.有氧化性.用于瓷器和玻璃着色.用于制备催化剂.由氧化镉.碳酸镉跟硝酸反应制得. [氯化镉]化学式CdCl3.式量183.32.无色六方晶体.密度4.047克/厘米3.熔点568℃.沸点960℃.易溶于水.微溶于醇.有毒.用作分析试剂.还用于照像.印染.镀镉.制特殊镜子.由氧化镉跟盐酸反应制得. [硫酸镉]化学式3CdSO4·8H2O.式量769.49.无色单斜晶系柱状结晶.密度3.09克/厘米3.41.5℃失去结晶水.无水物为白色正交晶体.密度4.691克/厘米3.熔点1000℃.易溶于水.不溶于醇.用作分析试剂.催化剂.制造镉锌电池.由镉或氧化镉跟硫酸反应制得. [汞]元素符号Hg.原子序数80.原子量200.59.外围电子排布5d106s2.位于第六周期ⅡB族.原子半径144皮米.第一电离能1013千焦/摩尔.电负性1.9.俗名水银.常温下唯一以液态存在的金属.银白色.熔点-38.87℃.沸点356.6℃.密度13.59克/厘米3.内聚力很强.在0-200℃间体积膨胀系数很均匀.蒸气有剧毒.在干燥空气中稳定.在潮湿空气中久置表面生氧化物膜.不溶于盐酸.稀硫酸和碱溶液.溶于硝酸和浓硫酸及王水中.能与卤素和硫直接化合.不与水反应.能溶解金.银.铂.铜.铅.钾.钠.所形成溶液称为汞齐.用于制温度计.气压计.催化剂.电极.汞蒸气灯.整流器.药物.雷汞等.古代已经发现.主要矿物有辰砂HgS.也有少量自然汞.将辰砂在空气中焙烧或与生石灰共热得到. [汞齐]又称汞合金.汞溶解其它金属形成的合金.汞量多时为液态.汞量少时为固体.有广泛用途.如钠汞齐作还原剂.锌汞齐制电池.银汞齐补牙.锡汞齐制镜. [氧化汞]化学式HgO.式量216.59.俗名三仙丹.有两种变体.红色晶体粉末.黄色晶体粉末.难溶于水.加热至500℃分解为汞和氧气.溶于盐酸生成氯化汞.溶于硝酸生成硝酸汞.有毒.有氧化性.用作氧化剂.分析试剂.医药制剂.陶瓷颜料.制有机汞化合物.在加热至300℃左右由汞和氧化合.或将硝酸汞徐徐加热可得红色氧化汞.将氢氧化钠或碳酸钠跟汞盐溶液反应得黄色氧化汞. [硝酸汞]化学式Hg(NO3)2·1/2H2O.式量333.61.淡黄色晶体.有毒.密度4.39克/厘米3.熔点79℃.易潮解.易溶于水.有氧化性.徐徐加热生成氧化汞.强热时生成汞.二氧化氮和氧气.用于分析试剂.制药.汞跟硝酸反应制得. [氯化汞]俗称升汞化学式HgCl.式量271.50.无色晶体.密度5.44克/厘米3.熔点276℃.沸点302℃.溶于水.有剧毒.共价型分子.熔融时不导电.在酸性溶液中有较强的氧化性.水溶液在空气和光的作用下逐渐分解为氯化亚汞.盐酸和氧.有腐蚀性.用作消毒剂.防腐剂.催化剂.医药.将氧化汞溶于盐酸.或将硫酸汞跟氯化钠混和共热制得. [氯化亚汞]因略带甜味俗称甘汞.化学式为Hg2Cl2.式量472.09.白色正方或四方晶体.密度7.15克/厘米3.熔点303℃.沸点384℃.不溶于水和乙醇.溶于浓硝酸.沸腾的盐酸.氯化铵和碱溶液.生成汞和氯化汞.在光照射下分解生成汞.氯化汞而逐渐变黑.用作杀菌剂.焰火制造.制甘汞电极.由硝酸亚汞溶液跟氯化钠溶液混合制得. [硫化汞]化学式HgS.式量232.65.有红色六角晶体.有金属光泽.密度 8.10克/厘米3.580℃升华.有黄色单斜晶体.在386℃以上稳定.还有黑色变体.密闭加热升华得红色变体.难溶于水和醇.溶于硫化钠溶液.硝酸和王水.在空气中加热生成汞和二氧化硫.有毒.用于油画颜料.印泥.油漆.油墨和朱红雕刻漆.还用于医药.天然产的俗称辰砂或朱砂.将汞与硫反应升华制得. [三仙丹]见氧化汞条. [升汞]见氯化汞条. [甘汞]见氯化亚汞条. [朱砂]天然产的硫化汞俗称.呈红褐色. [雷汞]又称雷酸汞.化学式Hg(ONC)2.式量284.62.白色或灰色结晶粉末.密度4.2克/厘米3.微溶于冷水.溶于热水和乙醇.有毒.加热或干燥时受轻微振动即爆炸.是常用的炸药起爆药.由硝酸汞在过量硝酸中与乙醇反应制得. [雷酸汞]见雷汞条. [钪]元素符号Sc.原子序数21.原子量44.96.外围电子排布3d14s2.位于第四周期ⅢB族.原子半径160.6皮米.第一电离能632千焦/摩尔.电负性1.3.主要氧化数+3.较软的银白色金属.密度2.989克/厘米3.熔点1541℃.沸点2831℃.化学性质活泼.在空气中易被氧化而变暗.跟热水反应放出氢气.跟酸反应放出氢气.用于制备合金和特种玻璃.它的化合物用作催化剂.1876年瑞典人尼尔森发现了钪.主要矿物有钪钇石.常跟钇镧伴生.电解氯化钪可制得钪. [钇]元素符号Y.原子序数39.原子量88.91.外围电子排布4d15s2.位于第五周期ⅢB族.原子半径181皮米.第一电离能615.6千焦/摩尔.电负性1.2.主要氧化数+3.稀土元素之一.灰色有光泽金属.熔点1522℃.沸点3338℃.与热水反应生成氢氧化物和氢气.也溶于稀酸和氢氧化钾溶液.能吸附氢气.用于制合金.激光器.反应堆的减速剂等.1794年芬兰人加德林发现钇土.用钙还原三氟化钇制得. [钛]元素符号Ti.原子序数22.原子量47.90.外围电子排布3d24s2.位于第四周期ⅣB族.原子半径144.8皮米.第一电离能 662千焦/摩尔.电负性1.5.主要氧化数+2.+3.+4.银白色有光泽金属.有良好的延展性.密度4.54克/厘米3.熔点1660±10℃.沸点 3287℃.表面易形成致密氧化物保护层.使化学性质变得不活动.加热时.在空气中燃烧生成TiO2.室温时不与水.稀盐酸.稀硫酸和硝酸反应.但能被氢氟酸.熔融碱侵蚀.也能跟热浓盐酸和王水反应.有良好的抗腐蚀性能.钛和钛的合金广泛用于制造飞机.火箭.卫星.宇宙飞船.舰艇.汽轮机.化工设备.电讯器材.人造骨骼等.1791年英国人格列高尔发现钛.在地壳中丰度0.42%.主要矿物有金红石TiO.钛铁矿FeTiO3等.用镁.钠还原四氯化钛制得. [二氧化钛]俗称钛白或钛白粉.化学式TiO2.式量79.90.白色无定形粉末.加热时变黄色.受高温变棕色.冷时再呈白色.不溶于水.化学性质相当稳定.不溶于盐酸.硝酸和稀硫酸.溶于热浓硫酸.氢氟酸.是弱的两性氧化物.与硫酸氢钾熔融生成硫酸钛,与氢氧化钠熔融生成钛酸钠.用作重要的白色颜料和瓷器釉药.还用于制金属钛.钛铁合金.硬质合金.橡胶.造纸用作填料.电机工业用于制绝缘体.电瓷等.工业上用硫酸分解钛铁矿.除铁后再经水解制得. [钛白]见二氧化钛条. [四氯化钛]化学式TiCl4.式量189.91.无色或淡黄色液体.易挥发.密度1.726克/厘米3.熔点-25℃.沸点136.4℃.容易水解.在潮湿空气中发烟 TiCl4+3H2O=H2TiO3+4HCl↑ 是制备金属钛的中间产物.在797℃时用熔融镁跟四氯化钛蒸气反应可得海绵状钛.还可用作天然纤维和合成纤维的防水剂.将二氧化钛和碳粉混合加热至800℃左右.用氯处理.可制得: TiO2+2C+2Cl2=TiCl4+2CO2↑ [锆]元素符号Zr.原子序数40.原子量91.22.外围电子排布4d25s2.位于第五周期ⅣB族.原子半径160皮米.第一电离能664千焦/摩.电负性1.4.浅灰色.硬而脆.密度6.506克/厘米3.熔点1852±2℃.沸点4377℃.主要氧化数+2.+3.+4.常温下不活泼.在空气中形成致密氧化膜保持明亮光泽.耐腐蚀性较好.不溶于盐酸.硝酸及强碱溶液.能溶于王水和氢氟酸.高温时可跟非金属和许多金属反应.金属锆主要用作核反应堆中铀燃料元件的包壳.化学工业用于制耐腐蚀的容器和管道.1789年德国人克拉普罗德发现了锆土.用镁还原四氧化锆制得. [铪]元素符号Hf.原子序数72.原子量178.49.外围电子排布5d26s2.位于第六周期ⅣB族.原子半径156.4皮米.第一电离能533千焦/摩尔.电负性1.3.主要氧化数+4.银白色有光泽金属.密度13.31克/厘米3.熔点2227℃.沸点4602℃.自然界中与锆伴生.化学性质与锆相似.常温下在空气和水中稳定.不与稀酸和强碱溶液反应.易溶于氢氟酸和王水.对中子有较好的吸收能力.用作核反应堆的控制棒.制X射线管的阴极.1923年德国人科斯特.匈牙利人冯·郝维西由X射线光谱发现.自然界很少.用钠在加热时还原四氯化铪制得. [钒]元素符号V.原子序数23.原子量50.94.外围电子排布3d34s2.位于第四周期VB族.原子半径132.1皮米.第一电离能654千焦/摩尔.电负性1.6.银白色金属.有良好的延展性.密度 5.96克/厘米3.熔点 1890±10℃.沸点3380℃.主要氧化数+2.+3.+4.+5.常温下化学性质不活动.有较强的耐腐蚀性.不与空气.水反应.也不和非氧化性酸及强碱溶液反应.能溶于氢氟酸.硝酸和王水.高温条件下.钒和氧.氮.碳能反应.主要用于制合金钠和催化剂.1830年瑞典的塞夫斯唐姆发现了钒.主要矿物有钒酸钾铀矿.铅钒矿等.用钙还原五氧化二钒或用镁还原三氯化钒制得. [五氧化二钒]化学式V2O5.黄色正交晶体.微溶于水.能溶于酸或碱溶液.在有机合成和硫酸工业上用它做催化剂.灼烧钒酸铵制得. [铌]元素符号Nb.原子序数41.原子量92.91.外围电子排布4d45s1.位于第五周期 V B族.原子半径142.9皮米.第一电离能667千焦/摩尔.电负性1.6.主要氧化数+2.+3.+4.+5.钢灰色有光泽金属.硬而有延展性.密度8.57克/厘米3.熔点2468±10℃.沸点4742℃.室温下在空气中稳定.加热时与卤素反应生成五卤化物.溶于氢氟酸和浓硫酸.能与氢氧化钠溶液反应.主要用于制特种不锈钢.高温合金.超导合金.超级硬质合金.核反应堆中用作铀燃料元件的包壳. 1801年英国人哈契特发现了铌.与钽共存于钽铁矿.铌铁矿中.电解熔融K2NbF7或用活泼金属.碳还原氧化物制得. [钽]元素符号 Ta.原子序数73.原子量 180.95.外围电子排布5d36s2.位于第六周期VB族.原子半径143皮米.第一电离能745千焦/摩尔.电负性1.5.银白色有光泽金属.有延展性.密度为16.54克/厘米3.熔点2996℃.沸点5425±100℃.化学性质稳定.耐腐蚀性强.除氢氟酸.发烟硫酸及熔碱外.一般不跟水.空气.盐酸.硝酸及王水反应.主要氧化数+5.能吸收氢.氧.氦等气体.用于制造超短波发射器.化学器皿.真空管.化工设备.高速车削工具和催化剂.1802年瑞典人瑞克贝格发现.1903年鲍尔登制得金属钽.主要矿物有铌钽铁矿.电解熔融K2TaF7或用活泼金属.碳还原氧化物制得. [铬]元素符号Cr.原子序数24.原子量51.996.外围电子排布3d54s1.位于第四周期ⅥB族.原子金属半径124.9皮米.第一电离能657千焦/摩尔.电负性1.6.主要氧化数+2.+3.+6.银白色有光泽金属.含有杂质的铬硬而脆.高纯铬有延展性.耐腐蚀性强.不溶于水.在空气中即便是在高温下氧化也很缓慢.高温下.铬能与卤素.硫.氮.碳等化合.也能跟水蒸气反应.能慢慢地溶于稀盐酸.稀硫酸.生成二价铬盐.与空气接触时很快被氧化成三价铬盐.铬能与浓硫酸反应.但不溶于浓硝酸.因表面生成致密氧化膜而呈钝态.能被熔融碱侵蚀.与氢反应生成CrH2.主要用于制不锈钢及耐高温耐腐蚀的高强度的合金.制电阻合金.还用于电镀.1797年法国人沃克兰发现了铬.主要矿物有铬铁矿Fe2.由电解铬氨钒溶液或铬酸溶液制得.也可用铝粉还原氧化铬制得. [三氧化二铬]亦称氧化铬.化学式Cr2O3.式量151.99.绿色六方晶体或无定形粉末.密度5.21克/厘米3.熔点2266±25℃.沸点4000℃.不溶于水.不溶于碱溶液.略溶于酸.具有磁性.用作分析试剂.催化剂.陶瓷釉彩原料.油漆颜料.制备铬合金和铬盐.实验室由重铬酸铵(NH4)2Cr2O7受热分解制得 [三氧化铬]亦称铬酸酐.化学式CrO3.式量99.99.红色正交晶体.常呈针状或柱状结晶.密度2.7克/厘米3.熔点196℃.易潮解.易溶于水.水溶液是铬酸.溶于醇.硝酸或硫酸.有强氧化性.有毒.有腐蚀性.用作分析试剂.强氧化剂.还用于镀铬.制铬酸盐.玻璃着色.由重铬酸钠与浓硫酸共热制得. [铬酐]铬酸酐的简称.见三氧化铬条. [氯化铬]别名三氯化铬.化学式CrCl3.式量158.38.无水氯化铬为强烈发光的紫色六角晶系的片状结晶.密度2.9克/厘米3.熔点1150℃.几乎不溶于水.与水长时间沸腾可形成绿色溶液.在空气中灼烧可变为三氧化三铬.六水合氯化铬CrCl3·6H2O有三种变体.分别呈深绿色.浅绿色和紫色.水合物易潮解.易溶于水.用作媒染剂.催化剂.无机合成.将三氧化二铬溶解在浓盐酸中.结晶可制得六水合氯化铬. [钼]元素符号Mo.原子序数42.原子量95.94.外围电子排布4d55s1.位于五周期ⅥB族.原子半径136.2皮米.第一电离能689千焦/摩尔.电负性1.8.主要氧化数+2.+3.+4.+5.+6.银灰色有光泽的金属.质硬而有延展性.密度10.22克/厘米3.熔点2610℃.沸点5560℃.在很高的温度下仍有很高的强度.常温时在空气中稳定.高温时燃烧生成三氧化钼.跟氯和溴能化合.不溶于盐酸和氢氟酸.能溶于浓硫酸.硝酸和王水.纯钼丝用于高温电炉.纯钼片用于制电子管.晶体管和X射线器材.灯泡.合金钢加钼可提高弹性.抗腐蚀性.保持永久磁性.1782年瑞典埃易姆用碳还原钼酸得到钼.主要矿物有辉钼矿MoS2.钼钨钙矿.用氢或铝还原三氧化钼制得. [三氧化钼]化学式MoO3.式量143.94.白色透明斜方晶体.加热时转为黄色.冷却后恢复原来颜色.密度4.692克/厘米3.熔点795℃.沸点1155℃.易升华.不溶于水.可熔于氨水和强碱溶液.生成钼酸盐.溶于强酸.生成二氧钼根和氧钼根络合阳离子.与酸根可形成可溶性络合物.氧化性极弱.在高温下可被氢.碳.铝还原.用作分析试剂.制备钼合金和钼盐.在空气中灼烧钼或二硫化钼或者焙烧钼酸制得. [钨]元素符号W.原子序数74.原子量183.85.外围电子排布5d46s2.位于第六周期ⅥB族.原子半径137皮米.第一电离能775千焦/摩尔.电负性1.7.主要氧化数+2.+3.+4.+5.+6.银灰色有光泽金属.硬度很大.密度19.3克/厘米3.熔点3410±20℃.沸点 5660℃.化学性质很稳定.常温时不跟空气和水反应.不溶于盐酸.硫酸.硝酸和碱溶液.溶于王水以及硝酸和氢氟酸的混合液.高温下能与氯.溴.碘.碳.氮.硫等化合.但不与氢化合.用于制钨丝.电学仪器.光学仪器.高速切削钢.特种钢.X射线靶等.1783年西班牙人德普尔亚发现钨.重要钨矿有钨锰铁矿WO4.钨锰矿MnWO4等.处理钨矿石得三氧化钨.再用氢还原三氧化钨制得钨粉. [三氧化钨]化学式WO3.式量231.85.黄色正交结晶或橙黄色粉末.密度7.16克/厘米3.熔点1473℃.不溶于水和一般无机酸.溶于氢氟酸和浓碱溶液.高温下可被氢.碳.铝等还原.用于制金属钨和钨合金.还用于制钨盐.釉彩.防火织物.X射线用屏.将钨在氧气中燃烧或将钨酸脱水可制得. [钨酸]化学式H2WO4.式量249.88.黄色或黄绿色粉末.密度5.5克/厘米3.熔点100℃.不溶于水.不溶于一般酸.溶于氢氟酸.溶于氢氧化钠溶液.用于制钨.钨丝.还用作纺织品的媒染剂.在钨酸钠热溶液中加入强酸即可析出黄色的钨酸. [锰]元素符号Mn.原子序数25.原子量54.94.外围电子排布3d54s2.位于第四周期ⅦB族.原子半径124皮米.第一电离能727千焦/摩尔.电负性1.5.主要氧化数+2.+4.+6.+7.银白色金属.硬而脆.密度7.20克/厘米3.熔点1244+3℃.沸点1962℃.固态时有四种同素异形体.常温下为α锰.在空气中易氧化生成褐色氧化物覆盖层.燃烧时生成四氧化三锰.红热时与水反应生成四氧化三锰和氢.溶于稀盐酸.稀硫酸生成二价锰盐.高温时跟卤素.硫.磷.碳.氮直接化合.用于制合金.少量锰能改善钢的抗冲击性能.锰铁用作炼钢过程的脱氧.脱硫添加剂.还用于冶炼铝合金.镁合金.1774年瑞典人甘恩用木炭跟软锰矿共热得到锰.主要矿物有软锰矿MnO2·xH2O.黑锰矿Mn3O4.最近发现大洋底部有大量锰结核矿.在地壳中丰度为0.1%.用铝还原软锰矿制得. [二氧化锰]化学式MnO2.式量86.94.钢灰色块状固体或黑色粉末.天然产的称软锰矿.密度5.026克/厘米3.不溶于水.溶于浓盐酸生成MnCl2和Cl2.在浓硫酸中放出氧气并生成硫酸锰.与氯酸钾.氢氧化钾共熔生成锰酸钾.在酸性介质中呈强氧化性.用作催化剂.氧化剂.制干电池.还用于炼钢.制玻璃.陶瓷.热敏电阻.将硝酸亚锰加热到200℃制得.也可从天然软锰矿制取. [硫酸锰]化学式MnSO4·4H2O.式量223.08.微红色细小晶体.密度2.107克/厘米3.在干燥空气中风化.280℃失去结晶水成白色无水物.溶于水.用于制锰肥.电解锰.油漆催干剂.由二氧化锰跟硫酸反应制得. [锝]元素符号Tc.原子序数43.原子量98.9.外围电子排市4d55s2位于第五周期ⅦB族.原子半径135.8皮米.第一电离能708千焦/摩尔.电负性1.9.主要氧化数+4.+7.银灰色金属.密度11.50克/厘米3.熔点2200℃.沸点4877℃.是第一个用人工方法得到的元素.它的同位素都有放射性.97Tc最稳定.半衰期为2.6×106年.化学性质与铼相似.高温与氧反应生成Tc2O7.不溶于稀硫酸.盐酸.溶于硝酸生高锝酸.溶于王水.1937年美国人佩里厄和塞格瑞在回旋加速器里用氘核轰击钼-98制得.在自然界中的铀裂变产物中有锝的同位素.用于原子能工业.主要由人工核反应制得. [铼]元素符号Re.原子序数75.原子量186.2.外围电子排布5d56s2.位于第6周期ⅦB族.原子半径137皮米.第一电离能765千焦/摩尔.电负性1.9.主要氧化数+3.+4.+7.银白色有光泽金属.质软.有良好延展性.电阻大.密度21.04克/厘米3.熔点3180℃.沸点5627℃.327℃时被氧化生成Re2O7.高温时能与氟.氯.溴.硫反应.不溶于盐酸.稀硫酸.可溶于硝酸或过氧化氢溶液生成高铼酸HReO4.可吸收氢.用于制耐热.耐腐蚀合金.这些合金用于制卫星和火箭的外壳.用于制高温热电偶.特种灯丝.有机合成工业的催化剂.地壳中丰度10-7%.主要存于辉钼矿中.1925年由德国人诺达克.塔克和贝格发现.用氢还原铼的化合物制得. [镧]元素符号La.原子序数57.原子量138.9.外围电子排布5d16s2.位于第六周期ⅢB族.原子半径187.7皮米.电负性1.1.主要氧化数+3.银白色金属.柔软.有延展性.密度6.145克/厘米3.熔点921℃.沸点3457℃.化学性质活泼与铝相似.在空气中易被氧化成白色粉末La2O3.燃烧时生成氧化物和氮化物.在氢气中加热生成氢化物.与水反应生成氢氧化镧和氢气.易溶于稀酸生成镧盐和氢气.应保存在煤油中.用来制镧盐.不锈钢.引火合金.医药.高级光学玻璃.超导体.1839年瑞典人莫桑德尔发现了镧.第一个稀土元素.在地壳中丰度0.0018%.在稀土元素中居第二位.常与其它稀土元素共生于独居石或氟碳锶镧矿中.用钠还原无水氯化镧.或电解熔融无水氯化镧制得. [铈]元素符号Ce.原子序数58.原子量140.12.外围电子排布4f15d16s2.位于第六周期ⅢB族.原子半径182.5皮米.电负性1.1.主要氧化数+3.+4.灰色金属.有延展性.密度:立方晶体6.76克/厘米3.六方晶体6.66克/厘米3.熔点799℃.沸点3426℃.化学性质活泼.在干燥空气中稳定.在潮湿空气中表面易氧化.加热时燃烧生成二氧化铈.能跟氢.氯.溴.碘.硫直接化合.能与沸水反应.溶于酸.不溶于碱.铈的着火点很低燃烧时放大量热.以铈为主的轻稀金属混合物.在摩擦或撞击时.其细末可自燃.用于制打火石和军用引火合金.还可用作催化剂.冶金时的吸气剂.玻璃工业的着色剂.抛光剂.电弧电极.特种玻璃.煤气灯纱罩.1803年德国人克拉普罗特.瑞典人贝采利乌斯和息辛格分别发现了铈.是稀土元素中最丰富的.在地壳中的丰度为0.004%.主要矿物有独居石.氟碳铈矿.用镁粉还原氧化铈.或电解熔融氯化铈制得. [镨]无素符号Pr.原子序数59.原子量140.9.外围电子排布4f36s2.位于第六周期ⅢB族.原子半径182.8皮米.电负性1.1.主要氧化数+3.+4.银灰色金属.有两种晶体.α六方晶体熔点为931℃.沸点为3512℃.密度为6.77克/厘米3,β型立方晶体熔点为935℃.沸点为3127℃.密度为6.64克/厘米3.化学性质活泼.在潮湿空气中易氧化生成氧化物膜.与水反应放出氢生成氢氧化物.易溶于盐酸.稀硫酸和硝酸.用于制合金.催化剂.特种玻璃.颜料.陶瓷着色.1885年由冯·威尔塞巴赫发现.主要存在于独居石矿中.电解熔融无水氯化镨制得. [钕]
网址:http://m.1010jiajiao.com/timu_id_3706616[举报]
[物质结构与性质]如图所示为血红蛋白和肌红蛋白的活性部分--血红素的结构.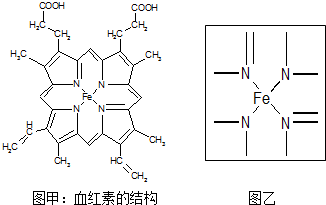
回答下列问题:
(1)血红素中含有C、H、O、N、Fe五种元素,C、H、N、O四种元素的电负性由小到大的顺序是
 .
.
(2)血红素中两种N原子的杂化方式分别为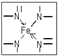
 .
.
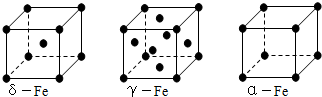
(3)铁有δ、γ、α三种同素异形体,γ晶体晶胞中所含有的铁原子数为
查看习题详情和答案>>

回答下列问题:
(1)血红素中含有C、H、O、N、Fe五种元素,C、H、N、O四种元素的电负性由小到大的顺序是
H<C<N<O
H<C<N<O
,根据以上电负性请判断H2N-CHO 中C和N的化合价分别为+2
+2
和-3
-3
.写出基态Fe原子的核外价电子排布图

(2)血红素中两种N原子的杂化方式分别为
sp2、sp3
sp2、sp3
,在图乙的方框内用“→”标出Fe2+的配位键

(3)铁有δ、γ、α三种同素异形体,γ晶体晶胞中所含有的铁原子数为
4
4
,δ、α两种晶胞中铁原子的配位数之比为4:3
4:3
;在δ晶胞中空间利用率为68%
68%
,与其具有相同堆积方式的金属还有Na、K
Na、K
(填元素符号).
某化学兴趣小组测定某FeCl3样品(含有少量FeCl2杂质)中铁元素的质量分数,实验时按以下步骤进行:
①称量ag样品,置于烧杯中,
②加入适量的蒸馏水,使样品溶解,然后准确配制成250mL溶液
③准确量取25.00mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,加热使反应完全
④趁热迅速加入过量氨水,充分搅拌,使沉淀完全
⑤过滤,洗涤沉淀
⑥将沉淀声称到坩埚内加热,搅拌直到固体全部由红褐色变为红棕色后在干燥器中冷却到室温后,称量
⑦…根据上面叙述,回答
(1)如图所示仪器中,本实验步骤①②中必须用到的仪器是
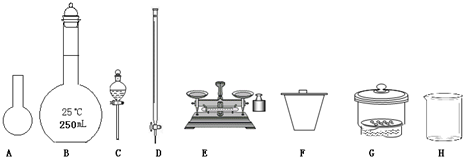
(2)写出步骤③和④中发生反应的离子方程式
(3)洗涤是洗去附着在沉淀上的
(4)若坩埚质量是W1,坩埚与加热后固体总质量是W2,则样品中铁元素的质量分数为
×100%
×100%(列出算式,不需化简)
(5)该兴趣小组中甲学生认为:实验步骤中不加氨水,其余步骤不变,仍可达到实验目的,你认为甲学的观点是否正确
查看习题详情和答案>>
①称量ag样品,置于烧杯中,
②加入适量的蒸馏水,使样品溶解,然后准确配制成250mL溶液
③准确量取25.00mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,加热使反应完全
④趁热迅速加入过量氨水,充分搅拌,使沉淀完全
⑤过滤,洗涤沉淀
⑥将沉淀声称到坩埚内加热,搅拌直到固体全部由红褐色变为红棕色后在干燥器中冷却到室温后,称量
⑦…根据上面叙述,回答
(1)如图所示仪器中,本实验步骤①②中必须用到的仪器是
BE
BE
.
(2)写出步骤③和④中发生反应的离子方程式
2Fe2++Cl2=2Fe3++2Cl-;Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+
2Fe2++Cl2=2Fe3++2Cl-;Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+
(3)洗涤是洗去附着在沉淀上的
NH4+、Cl-、OH-
NH4+、Cl-、OH-
(写离子符号).洗涤沉淀的操作是向过滤器中加入蒸馏水至没过沉淀,待滤液流出后重复上述操作多次直至洗净为止
向过滤器中加入蒸馏水至没过沉淀,待滤液流出后重复上述操作多次直至洗净为止
检验沉淀已洗净的方法是取最次一次洗出液置于小试管中,滴加AgNO3溶液若无沉淀产生证明已洗净
取最次一次洗出液置于小试管中,滴加AgNO3溶液若无沉淀产生证明已洗净
(4)若坩埚质量是W1,坩埚与加热后固体总质量是W2,则样品中铁元素的质量分数为
| (w2-w1)×112×10 |
| 160a |
| (w2-w1)×112×10 |
| 160a |
(5)该兴趣小组中甲学生认为:实验步骤中不加氨水,其余步骤不变,仍可达到实验目的,你认为甲学的观点是否正确
正确
正确
(填“正确”或“错误”)请说明理由(必要时可用化学方程式表示)氯化铁溶液中Fe3+水解Fe3++3H2O?Fe(OH)3+3H+,加热HCl挥发,促进水解进行,过一系列转化最终都能生成Fe2O3对后续实验无影响
氯化铁溶液中Fe3+水解Fe3++3H2O?Fe(OH)3+3H+,加热HCl挥发,促进水解进行,过一系列转化最终都能生成Fe2O3对后续实验无影响
.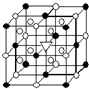 A.(1)右图所示为冰晶石(化学式为Na3AlF6)的晶胞.图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽图中●、○中的一种.图中●、○分别指代哪种粒子
A.(1)右图所示为冰晶石(化学式为Na3AlF6)的晶胞.图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽图中●、○中的一种.图中●、○分别指代哪种粒子AlF6-
AlF6-
、Na+
Na+
;大立方体的体心处▽所代表的是AlF6-
AlF6-
.冰晶石在化工生产中的用途电解炼铝的助熔剂
电解炼铝的助熔剂
.(2)H2S和H2O2的主要物理性质比较如下:
| 熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
| H2S | 187 | 202 | 2.6 |
| H2O2 | 272 | 423 | 以任意比互溶 |
H2O2分子间存在氢键,与水分子可形成氢键
H2O2分子间存在氢键,与水分子可形成氢键
(3)向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体.写出铜原子价电子层的电子排布式
3d104s1
3d104s1
,与铜同一周期的副族元素的基态原子中最外层电子数与铜原子相同的元素有Cr
Cr
(填元素符号).实验时形成的深蓝色溶液中的阳离子内存在的全部化学键类型有共价键和配位键
共价键和配位键
.实验过程中加入C2H5OH后可观察到析出深蓝色Cu(NH3)4SO4?H2O晶体.实验中所加C2H5OH的作用是降低Cu(NH3)4SO4?H2O的溶解度
降低Cu(NH3)4SO4?H2O的溶解度
.B.用含少量铁的氧化铜制取氯化铜晶体(CuCl2?xH2O).有如下操作:
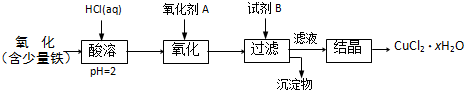
已知:在pH为4~5时,Fe3+几乎完全水解而沉淀,Cu2+却不水解.
(1)加热酸溶过程中发生反应的离子方程式有:
Fe+2H+=Fe2++H2↑、CuO+2H+=Cu2++H2O
Fe+2H+=Fe2++H2↑、CuO+2H+=Cu2++H2O
(2)氧化剂A可选用
①
①
(填编号,下同)①Cl2 ②KMnO4 ③HNO3
(3)要得到较纯的产品,试剂B可选用
③
③
①NaOH ②FeO ③CuO
(4)试剂B的作用是
①③
①③
①提高溶液的pH ②降低溶液的pH ③使Fe3+完全沉淀 ④使Cu2+完全沉淀
(5)从滤液经过结晶得到氯化铜晶体的方法是
②④①
②④①
(按实验先后顺序填编号)①过滤 ②蒸发浓缩 ③蒸发至干 ④冷却
(6)为了测定制得的氯化铜晶体(CuCl2?xH2O)中x值,某兴趣小组设计了两种实验方案:
方案一:称取m g晶体灼烧至质量不再减轻为止、冷却、称量所得无水CuCl2的质量为n g.
方案二:称取m g晶体、加入足量氢氧化钠溶液、过滤、沉淀洗涤后用小火加热至质量不再减轻为止、冷却、称量所得固体的质量为n g.
试评价上述两种实验方案,其中正确的方案是
二
二
,据此计算得x=| 80m-135n |
| 18n |
| 80m-135n |
| 18n |
黄铜矿(CuFeS2)是制取铜的主要原料,还可制备硫及铁的化合物.
(1)冶炼铜的反应为:
8CuFeS2+21O2
8Cu+4FeO+2Fe2O3+16SO2
若CuFeS2中Cu、Fe的化合价均为+2,反应中被氧化的元素有 (填元素符号).
(2)上述冶炼过程中产生大量的SO2,下列关于SO2的说法中正确的是 (填字母).
a.可处理后用于消毒杀菌
b.可排放到空气中消灭害虫
c.可处理后用于漂白织物
d.可用KMnO4溶液吸收制浓硫酸
(3)过二硫酸钾(K2S2O8)具有强氧化性,经少量K2S2O8处理过的KI溶液遇淀粉变蓝色,写出K2S2O与KI溶液反应的离子方程式: .
(4)用冶炼铜反应的固体产物配制FeCl2溶液,首先用 处理,然后过滤,再向溶液中加入过量的 .FeCl2溶液长期放置会变质,溶液变成棕黄色.检验FeCl2溶液已变质加入 ,溶液中立即出现 现象.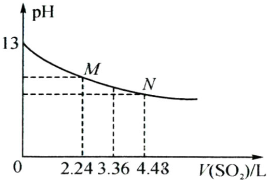
(5)将足量的SO2慢慢通入一定体积某浓度的NaOH溶液中,溶液的pH随SO2体积(已换算成标准状况,不考虑溶液体积变化)的变化曲线如图所示:
①NaOH溶液的物质的量浓度为 mol?L-1;
②n(SO2):n(NaOH)=1:2,反应对应M点的纵坐标 7(填“<”、“=”或“>”);
③N点溶液中含有的阴离子除OH-外,还有 (填化学式).
查看习题详情和答案>>
(1)冶炼铜的反应为:
8CuFeS2+21O2
| ||
若CuFeS2中Cu、Fe的化合价均为+2,反应中被氧化的元素有
(2)上述冶炼过程中产生大量的SO2,下列关于SO2的说法中正确的是
a.可处理后用于消毒杀菌
b.可排放到空气中消灭害虫
c.可处理后用于漂白织物
d.可用KMnO4溶液吸收制浓硫酸
(3)过二硫酸钾(K2S2O8)具有强氧化性,经少量K2S2O8处理过的KI溶液遇淀粉变蓝色,写出K2S2O与KI溶液反应的离子方程式:
(4)用冶炼铜反应的固体产物配制FeCl2溶液,首先用

(5)将足量的SO2慢慢通入一定体积某浓度的NaOH溶液中,溶液的pH随SO2体积(已换算成标准状况,不考虑溶液体积变化)的变化曲线如图所示:
①NaOH溶液的物质的量浓度为
②n(SO2):n(NaOH)=1:2,反应对应M点的纵坐标
③N点溶液中含有的阴离子除OH-外,还有
现有X、Y、Z三种元素.
(1)X的单质可以在Z的单质中燃烧生成XZ,火焰为苍白色.
(2)XZ极易溶于水,其水溶液可使蓝色石蕊试纸变红.
(3)X、Y、Z的单质在常温下为气体.
(4)两分子X的单质可以和Y单质化合生成两分子X2Y(常温下为液体).
(5)Z的单质溶于X2Y中得到溶液具有漂白性,推断:
①X、Y、Z各为何元素(写元素符号)?X
②XZ和X2Y各是什么物质(写化学式)?XZ
(6)Z的单质与铁化学方程式:
(7)化合物XZ与铁化学方程式:
查看习题详情和答案>>
(1)X的单质可以在Z的单质中燃烧生成XZ,火焰为苍白色.
(2)XZ极易溶于水,其水溶液可使蓝色石蕊试纸变红.
(3)X、Y、Z的单质在常温下为气体.
(4)两分子X的单质可以和Y单质化合生成两分子X2Y(常温下为液体).
(5)Z的单质溶于X2Y中得到溶液具有漂白性,推断:
①X、Y、Z各为何元素(写元素符号)?X
H
H
,YO
O
,ZCl
Cl
.②XZ和X2Y各是什么物质(写化学式)?XZ
HCl
HCl
,X2YH2O
H2O
.(6)Z的单质与铁化学方程式:
2Fe+3Cl2
2FeCl3
| ||
2Fe+3Cl2
2FeCl3
.
| ||
(7)化合物XZ与铁化学方程式:
Fe+2HCl═FeCl2+H2↑
Fe+2HCl═FeCl2+H2↑
.