摘要:B 2.C 3.C 4.B 5.C 6.D
网址:http://m.1010jiajiao.com/timu_id_3704735[举报]
A、B、C、D是四种短周期元素,E是过渡元素.A、B、C同周期,C、D同主族,A的原子结构示意图为: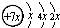 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
(1)写出下列元素的符号:A
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是
(3)用元素符号表示D所在周期(除稀有气体元素外)第一电离能最大的元素是
(4)D的氢化物比C的氢化物的沸点
(5)E元素原子的核电荷数是
(6)A、B、C最高价氧化物的晶体类型是分别是
(7)画出D的核外电子排布图
 ,这样排布遵循了
,这样排布遵循了
查看习题详情和答案>>
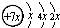 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:(1)写出下列元素的符号:A
Si
Si
BNa
Na
CP
P
DN
N
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是
HNO3
HNO3
,碱性最强的是NaOH
NaOH
.(3)用元素符号表示D所在周期(除稀有气体元素外)第一电离能最大的元素是
F
F
,电负性最大的元素是F
F
.(4)D的氢化物比C的氢化物的沸点
高
高
(填“高“或“低“),原因氨气分子之间含有氢键
氨气分子之间含有氢键
(5)E元素原子的核电荷数是
26
26
,E元素在周期表的第四
四
周期,第Ⅷ
Ⅷ
族,已知元素周期表可按电子排布分为s区、p区等,则E元素在d
d
区.(6)A、B、C最高价氧化物的晶体类型是分别是
原子
原子
晶体、离子
离子
晶体、分子
分子
晶体(7)画出D的核外电子排布图


泡利
泡利
原理和洪特
洪特
规则.A、B、C、D是四种常见单质,其对应元素的原子序数依次增大,其中B、D属于常见金属,其余均为常见化合物,J是一种黑色固体,I的浓溶液具有还原性,从A-I的所有物质之间有如下的转化关系: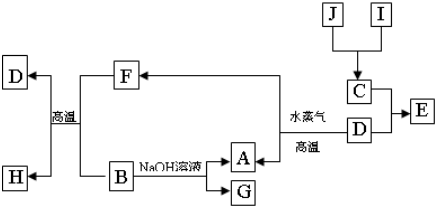
回答下列问题:
(1)写出物质C的构成元素在周期表中的位置
(2)写出B与F反应的化学方程式
(3)由E的饱和溶液可以制得胶体,具体制备方法是:
a.光束通过该液体时形成光亮的“通路”?
b.向液体中逐滴加入足量氢碘酸,先有沉淀产生,后沉淀逐渐溶解,再滴入几滴淀粉溶液,溶液变为蓝色
c.向该液体中加入硝酸银溶液,无沉淀产生?
d.将该液体加热、蒸干、灼烧,得红棕色固体?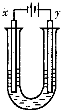
另取少量上述胶体置于U型管中,按如图装置图连接好装置.通电一小段时间后,X极附近的现象是
(4)取少量上述胶体置于试管中,向试管中滴加一定量稀盐酸,边滴边振荡,可以看到溶液颜色逐渐变浅,最终得到黄色的溶液,发生此变化的离子方程式为
(5)G的水溶液显
(6)J在H2O2分解反应中作催化剂.若将适量J加入酸化的H2O2的溶液中,J溶解生成它的+2价离子,该反应的离子方程式是
查看习题详情和答案>>

回答下列问题:
(1)写出物质C的构成元素在周期表中的位置
第三周期、第ⅦA族
第三周期、第ⅦA族
.(2)写出B与F反应的化学方程式
8Al+3Fe3O4
9Fe+4Al2O3
| ||
8Al+3Fe3O4
9Fe+4Al2O3
.
| ||
(3)由E的饱和溶液可以制得胶体,具体制备方法是:
将饱和FeCl3溶液逐滴加入沸水中,继续加热至液体变为红褐色
将饱和FeCl3溶液逐滴加入沸水中,继续加热至液体变为红褐色
,用化学方程式表示该过程的原理:Fe3++3H2O
Fe(OH)3(胶体)+3H+
| ||
Fe3++3H2O
Fe(OH)3(胶体)+3H+
.若要提纯该胶体,采用的操作方法叫
| ||
渗析
渗析
.此液体具有的性质是abd
abd
(填写序号字母)a.光束通过该液体时形成光亮的“通路”?
b.向液体中逐滴加入足量氢碘酸,先有沉淀产生,后沉淀逐渐溶解,再滴入几滴淀粉溶液,溶液变为蓝色
c.向该液体中加入硝酸银溶液,无沉淀产生?
d.将该液体加热、蒸干、灼烧,得红棕色固体?

另取少量上述胶体置于U型管中,按如图装置图连接好装置.通电一小段时间后,X极附近的现象是
红褐色加深
红褐色加深
.(4)取少量上述胶体置于试管中,向试管中滴加一定量稀盐酸,边滴边振荡,可以看到溶液颜色逐渐变浅,最终得到黄色的溶液,发生此变化的离子方程式为
Fe(OH)3+3H+=Fe3++3H2O
Fe(OH)3+3H+=Fe3++3H2O
.(5)G的水溶液显
碱
碱
性(填酸或碱);原因是(用离子方程式表 示)AlO2-+2H2O Al(OH)3+OH-
Al(OH)3+OH-
 Al(OH)3+OH-
Al(OH)3+OH-AlO2-+2H2O Al(OH)3+OH-
Al(OH)3+OH-
. Al(OH)3+OH-
Al(OH)3+OH-(6)J在H2O2分解反应中作催化剂.若将适量J加入酸化的H2O2的溶液中,J溶解生成它的+2价离子,该反应的离子方程式是
MnO2+H2O2+2H+═Mn2++O2↑+2H2O
MnO2+H2O2+2H+═Mn2++O2↑+2H2O
.A、B、C、D为按顺序排列的前四种卤素单质,仔细分析下表中的数据,回答有关问题.
(1)在标准状况下为液体的卤素单质是
(2)A的相对分子质量为
(3)写出B与水反应的化学方程式
(4)卤素单质B、C、D的氧化性由大到小的顺序为
查看习题详情和答案>>
| 卤素单质 | 密度(标准状况下) | 沸点/℃ | 熔点/℃ | 溶解度(标准状况下,100g水中) |
| A | 1.696 g?l-1 | -188.1 | -219.6 | -- |
| B | 3.214 g?l-1 | -34.6 | -101 | 226 cm3 |
| C | 3.119 g?cm-3 | 58.78 | -7.2 | 4.16 g |
| D | 4.93 g?cm-3 | 184.4 | 113.5 | 0.029 g |
C
C
(填字母,下同),为固体的卤素单质是D
D
.(2)A的相对分子质量为
38
38
(保留整数)(3)写出B与水反应的化学方程式
Cl2+H2O═HCl+HClO
Cl2+H2O═HCl+HClO
(4)卤素单质B、C、D的氧化性由大到小的顺序为
Cl2>Br2>I2
Cl2>Br2>I2
(用化学式表示)A、B、C是中学化学中常见的三种短周期元素.已知:①A元素原子最外层电子数是次外层电子数的2倍;②B元素最高正价与最低负价的代数和为2;③C元素有多种化合价,且常温下C元素的单质与某种一元强碱溶液反应,可得到两种含C元素的化合物;④B、C两种元素质子数之和是A元素质子数的4倍.
(1)写出A元素在周期表中的位置
(2)写出C的单质和强碱溶液反应的离子方程式
(3)意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的B4气态分子.B4分子结构与白磷分子结构相似 ,已知断裂1molB-B吸收167kJ的热量,生成1molB≡B放出942kJ热量.试写出由B4气态分子变成B2气态分子的热化学方程式:
,已知断裂1molB-B吸收167kJ的热量,生成1molB≡B放出942kJ热量.试写出由B4气态分子变成B2气态分子的热化学方程式:
(4)由B、C两种元素组成的化合物X,常温下为易挥发的淡黄色液体,X分子为三角锥形分子,且分子里B、C两种原子最外层均达到8个电子的稳定结构.X遇水蒸气可形成一种常见的漂白性物质.则X的结构式为
 ,X与水反应的化学方程式是
,X与水反应的化学方程式是
(5)A、B两种元素可形成一种硬度比金刚石还大的化合物Y.在化合物Y中,A、B原子间以单键相结合,且每个原子的最外层均达到8个电子的稳定结构.则Y的化学式为
(6)B2H4是一种可燃性液体,其水溶液呈弱碱性,是因为溶液中存在平衡:H2B-BH2+H2O?
查看习题详情和答案>>
(1)写出A元素在周期表中的位置
第二周期ⅣA族
第二周期ⅣA族
;(2)写出C的单质和强碱溶液反应的离子方程式
C12+2OH-=ClO-+Cl-+H2O
C12+2OH-=ClO-+Cl-+H2O
;(3)意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的B4气态分子.B4分子结构与白磷分子结构相似
 ,已知断裂1molB-B吸收167kJ的热量,生成1molB≡B放出942kJ热量.试写出由B4气态分子变成B2气态分子的热化学方程式:
,已知断裂1molB-B吸收167kJ的热量,生成1molB≡B放出942kJ热量.试写出由B4气态分子变成B2气态分子的热化学方程式:N4(g)═2N2(g)△H=-882kJ/mol
N4(g)═2N2(g)△H=-882kJ/mol
;(4)由B、C两种元素组成的化合物X,常温下为易挥发的淡黄色液体,X分子为三角锥形分子,且分子里B、C两种原子最外层均达到8个电子的稳定结构.X遇水蒸气可形成一种常见的漂白性物质.则X的结构式为


NCl3+3H2O═NH3+3HClO
NCl3+3H2O═NH3+3HClO
;(5)A、B两种元素可形成一种硬度比金刚石还大的化合物Y.在化合物Y中,A、B原子间以单键相结合,且每个原子的最外层均达到8个电子的稳定结构.则Y的化学式为
C3N4
C3N4
,Y晶体的熔点比金刚石熔点高
高
(填“高”或“低”);(6)B2H4是一种可燃性液体,其水溶液呈弱碱性,是因为溶液中存在平衡:H2B-BH2+H2O?
H2N-NH3++OH-(或N2H5++OH-)
H2N-NH3++OH-(或N2H5++OH-)
.A、B、C三个烧杯中分别盛有相同物质的量浓度的硫酸铜溶液.D为电解池,其中电极材料均为惰性物质,通过导线与直流电源相连.实验开始时,同时在XY两边各滴入几滴酚酞试液,X极附近首先变红.

请回答以下问题:
(1)B中Cu极电极反应式为
(2)A、B、C三个烧杯中Fe的反应速率最快的是
(3)若C中被腐蚀金属的质量是32.5g,则反应中转移的电子的物质的量是
(4)D中直流电源a为
(5)电池D中N极上的电极反应式为:
(6)D中在M、N、X、Y各电极上析出生成物的物质的量之比为
查看习题详情和答案>>

请回答以下问题:
(1)B中Cu极电极反应式为
Cu2++2e-=Cu
Cu2++2e-=Cu
.(2)A、B、C三个烧杯中Fe的反应速率最快的是
B
B
.(3)若C中被腐蚀金属的质量是32.5g,则反应中转移的电子的物质的量是
1mol
1mol
.(4)D中直流电源a为
负
负
极.(5)电池D中N极上的电极反应式为:
2Cl--2e-=Cl2↑
2Cl--2e-=Cl2↑
.(6)D中在M、N、X、Y各电极上析出生成物的物质的量之比为
1:1:1:1
1:1:1:1
.