网址:http://m.1010jiajiao.com/timu_id_3704297[举报]
 (2013?江西模拟)(一)X、Y、Z、L、M五种元素的原子序数依次增大,X的阴离子与Y的内层电子数相等,Y原子的最外层电子数是次外层电子数的两倍,Z、L是空气中含量最多的二种元素,M是地壳中含量最高的金属元素.回答下列问题:
(2013?江西模拟)(一)X、Y、Z、L、M五种元素的原子序数依次增大,X的阴离子与Y的内层电子数相等,Y原子的最外层电子数是次外层电子数的两倍,Z、L是空气中含量最多的二种元素,M是地壳中含量最高的金属元素.回答下列问题:(1)L的元素名称为
(2)Z、X两元素按原子数目比1:3和2:4构成分子A和B,用电子式表示A的形成过程
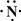 →
→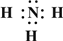
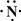 →
→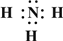


(3)硒(Se)是人体必须的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为
(4)一定条件下,M与TiO2、C(石墨)反应只生成乙和碳化钛(TiC),二者均为某些高温结构陶瓷的主要成分.已知.该反应生成lmol乙时放出536kJ热量,其热化学方程式为
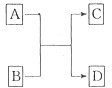
(二)已知A、B、C、D分别是由短周期元素原子组成的四种微粒,它们之间有如图所示的转变关系,且A是种含有18电子的微粒,C是一种含有10电子的微粒.请完成下列各题:
(1)若A、D分别是两种气态单质分子,写出A与B反应的化学方程式
(2)若B、D属同主族的单质分子,写出C的化学式
(3)若B是一种含四核l8电子的分子,如果D是一种气态单质分子,B的结构简式为
(4)若A、B均是含2个原子核的微粒,其中B中含有10个电子,D中含有18个电子,则A、B之间发生的离子反应方程式为
(5)若D是一种含有22电子的分子,则符合如图关系的A的物质有
 已知A、B、C、D四种物质分别是由短周期元素组成的微粒,它们之间有如图所示的转化关系,且A是一种含有18电子的微粒,C是一种含有10电子的微粒.请完成下列各题:
已知A、B、C、D四种物质分别是由短周期元素组成的微粒,它们之间有如图所示的转化关系,且A是一种含有18电子的微粒,C是一种含有10电子的微粒.请完成下列各题:(1)若A、D分别是两种气态单质分子,写出A与B反应的化学方程式:
(2)若B是一种四核含18电子的分子,D是一种气态单质分子,则A的化学式为
(3)若A、B均是含2个原子的微粒,其中B中含有10个电子,D中含有l8个电子,则A、B之间发生反应的离子方程式为
(4)若D是一种含有22个电子的分子,则符合如图所示关系的A的物质有
已知:A、B、C、D分别为中学化学中常见的4种不同微粒,它们之间有如图1-3所示的反应关系:

图1-3
(1)如果A、B、C、D均是10电子微粒,请写出:
A的化学式:_____________;C的电子式:_____________。
(2)如果A和C是18电子的微粒,B和D是10电子微粒,请写出:
A与B在溶液中反应的离子方程式:__________________________________________
查看习题详情和答案>>(10分)下表是元索周期表前四周期的一部分,①〜⑤代表五种元素。
(1)⑤元素形成的一种离子在空气中很不稳定,写出此离子的核外电子排布式:______
(2) 标准状况下,①元素形成的气态氢化物与CO的密度相同,是一种高能燃料。1g该氢化物完全燃烧生成①的最高价氧化物(固态)和液态水放热72.35kJ。请写出该氢化物燃烧的热化学方程式:__________________。
(3) 染料工业排放的废水中含有大量有毒的NO2-,可以在碱性条件下加人③元素形成的单质除去。加热处理后的废水会产生能使湿润的红色石蕊试纸变蓝的气体。请写出相应的离子方程式:________________________。
(4) 分别写出含有④元素的某种18电子的微粒和含有②元素的某种10电子的离子间反应的离子方程式:__________________。
查看习题详情和答案>>
(6分)已知A、B、C、D分别是由短周期元素原子组成的四种微粒,它们之间有如图所示的转变关系,且A是种含有18电子的微粒,C是一种含有10电子的微粒。请完成下列各题:
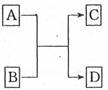
(1)若A、D分别是两种气态单质分子,写出A与B反应的化学方程
式
(2)若B、D属同主族的单质分子,写出C的化学式
(3)若B是一种含四核l8电子的分子,如果D是一种气态单质分子,B的结构简式为 ;
(4)若A、B均是含2个原子核的微粒,其中B中含有10个电子,D中含有18个电子,则A、B之间发生的离子反应方程式为
(5)若D是一种含有22电子的分子,则符合如图关系的A的物质有 (写出物质的化学式,如果是有机物则写相应的结构简式)。
查看习题详情和答案>>