网址:http://m.1010jiajiao.com/timu_id_3702911[举报]
(1)在用KMnO4酸性溶液处理Cu2S和FeS2的混合物时,发生的反应如下:
Ⅰ、MnO4ˉ+Cu2S+H+→Cu2++SO42ˉ+Mn2++H2O(未配平)
Ⅱ、MnO4ˉ+FeS2+H+→Fe3++SO42ˉ+Mn2++H2O(未配平)
①下列关于反应Ⅰ的说法正确的是
A、MnO4ˉ是氧化剂,Cu2S既是氧化剂又是还原剂
B、氧化剂与还原剂的物质的量之比为5:8
C、每生成1mol SO42ˉ,反应转移电子的物质的量为10mol
②若反应Ⅰ和反应Ⅱ中消耗的KMnO4的物质的量相同,则反应Ⅰ和反应Ⅱ中消耗的还原剂的物质的量之比为
(2)KMnO4、双氧水、活性炭常用于饮用水的处理,但三者在联合使用时必须有先后顺序.
①氧化反应:H2O2-2eˉ→2H++O2↑
还原反应:MnO4ˉ+5eˉ+8H+→Mn2++4H2O
写出该氧化还原反应的化学方程式
②在处理饮用水时,活性炭应在高锰酸钾反应结束后投放,否则会发生KMnO4+C+H2O→MnO2+X+K2CO3(未配平),其中X的化学式为
(1)在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
Ⅰ.MnO4-+Cu2S+H+→Cu2++SO2↑+Mn2++H2O(未配平)
Ⅱ.MnO4-+CuS+H+→Cu2++SO2↑+Mn2++H2O(未配平)
请回答下列问题:
①下列关于反应Ⅰ的说法不正确的是
A.被氧化的元素是Cu和S
B.MnO4-是氧化剂,Cu2S既是氧化剂又是还原剂
C.氧化剂与还原剂的物质的量之比为8:5
D.生成2.24L(标况下) SO2,转移电子的物质的量是0.8mol
E.氧化性的强弱关系是:MnO4->Mn2+>Cu2+
②用单线桥表示反应Ⅱ中电子转移的数目和方向:MnO4-+CuS


(2)①在稀硫酸中,MnO4-和H2O2也能发生氧化还原反应:
氧化反应:H2O2-2e-═2H++O2↑
还原反应:MnO4-+5e-+8H+═Mn2++4H2O
写出该氧化还原反应的化学方程式:
反应中若有0.5mol H2O2参加此反应,转移电子的个数为
②实验中发现,当加入的少量KMnO4完全反应后,H2O2仍能发生反应放出气体.其可能的原因是:
I.(1)有下列变化:CO
2- 3 |
2- 4 |
(2)不同条件下高锰酸钾可发生如下反应:MnO4-+5e-+8H+→Mn2++4H2O
MnO4-+3e-+2H2O→MnO2+4OH-
MnO
- 4 |
2- 4 |
由此可知,高锰酸根离子(MnO-4)反应后的产物与
(3)高锰酸钾溶液与硫化亚铁有如下反应:
10FeS+6KMnO4+24H2SO4→3K2SO4+6MnSO4+5Fe2(SO4)3+10S+24H2O
若上述反应前后固体的质量减少了2.8g,则硫元素与KMnO4之间发生电子转移的数目为
Ⅱ.酒后驾车已成为一个社会问题.检测驾驶人员呼气中酒精浓度(BrAC)的方法有多种.
(4)早期是利用检测试剂颜色变化定性判断BrAC,曾用如下反应检测BrAC:
完成并配平上述反应.
(5)受上述方法启发,后来用五氧化二碘的淀粉溶液检测BrAC,乙醇被氧化为乙醛,该反应的化学方程式为
高锰酸钾是一种重要的化学试剂,其溶液不很稳定,在酸性条件下会分解生成二氧化锰和氧气,在中性或弱碱性溶液中分解速度很慢,见光分解速度加快。
(1)酸性条件下高锰酸钾溶液分解的离子方程式 。
(2)请配平高锰酸钾溶液与草酸钠Na2C2O4溶液在酸性条件下反应的离子方程式:
______MnO4— +______C2O42—+______H+=______Mn2++______CO2↑+____________
(3)某学习小组为了探究高锰酸钾溶液和草酸钠溶液的反应过程,将高锰酸钾溶液逐滴地滴入一定体积的酸性草酸钠溶液中(温度相同,并不断振荡时),记录的现象如下表:
滴入高锰酸钾溶液的次序(每滴溶液的体积相同) |
高锰酸钾溶液紫色褪去的时间 |
|
先滴入第1滴 |
1min |
|
褪色后再滴入第2滴 |
15s |
|
褪色后再滴入第3滴 |
3s |
|
褪色后再滴入第4滴 |
1s |
请分析高锰酸钾溶液褪色时间变化的原因 。
(4)该学习小组在获取了上述经验和结论以后,用稳定的物质草酸钠Na2C2O4(相对分子质量134.0)来标定高锰酸钾溶液的浓度。他们准确称取1.340g纯净的草酸钠配成250mL溶液,每次准确量取25.00mL溶液酸化后用KMnO4溶液滴定。
①高锰酸钾溶液应装在 (填下图中的仪器编号)。
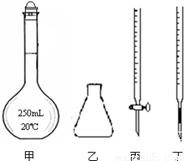
②为了防止高锰酸钾在酸性条件下分解而造成误差,滴定时应注意的是 。
③若在实验过程中存在下列操作,其中会使所测KMnO4浓度偏低的是 。
A.未润洗盛放KMnO4的滴定管
B.滴定前尖嘴部分无气泡,滴定终点时出现气泡
C.定容时,俯视刻度线
D.锥形瓶用水洗之后未用待测液润洗
④当溶液呈微红色且半分钟内不褪色,消耗KMnO4溶液20.00mL(多次测定的平均值),则KMnO4溶液的浓度为 。
查看习题详情和答案>>