摘要:2.Cl2+H2OH++Cl-+HClO平衡移动的应用 向氯水中加入 的物质 浓度变化 平衡移动 的方向 应 用 可溶性氯化物 c(Cl-) ①用饱和食盐水除Cl2中的HCl②用排饱和食盐水法收集Cl2 盐酸 c(H+)和c(Cl-) 次氯酸与浓盐酸反应制Cl2 NaOH c(H+) 用NaOH溶液吸收多余的Cl2 Ca(OH)2 c(H+) 制漂白粉 CaCO3 c(H+) 制高浓度HClO溶液 光照 c 氯水闭光保存或现用现配 [特别提醒]:Cl2+H2OH++Cl-+HClO平衡移动的各种情况均可归结到勒夏特列原理.故掌握知识要“以不变应万变 . [例1](2009届龙岩一中第一学段考试)下列实验现象.与新制氯水中的某些成分没有关系的 ( ) A.将NaHCO3固体加入新制氯水.有无色气泡(H+) B.使红色布条褪色(HCl) C.向FeCl2溶液中滴加氯水.再滴加KSCN溶液.发现呈血红色(Cl2) D.滴加AgNO3溶液生成白色沉淀(Cl-) [解析]氯水中存在H+.与NaHCO3反应产生CO2.与H+相关,氯水使红色布条褪色是因为氯水中存在HClO.而不是因为氯水中存在HCl,氯水中存在Cl2能氧化Fe2+→Fe3+.故滴加KSCN溶液.溶液呈血红色,氯水中存在Cl-能与AgNO3溶液生成白色沉淀. [答案]B [方法技巧]解此题的关键是掌握氯水中含有的各种粒子以及他们对应的性质.强酸性--H+的性质,漂白性--HClO的性质,强氧化性--Cl2.HClO的性质. 考点2 氯气的制法
网址:http://m.1010jiajiao.com/timu_id_3702767[举报]
四种短周期元素A、B、C、D的性质或结构信息如下.
信息①原子半径大小:A>B>C>D
信息②四种元素之间形成的某三种分子的比例模型及部分性质:

请根据上述信息回答下列问题.
(1)①C元素在周期表中的位置
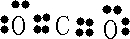 .
.
②A元素的单质与物质甲发生反应的离子方程式
③以Pt为电极,KOH为电解质溶液,两极分别通入乙和C的单质可组成燃料电池,写出电池的电极反应式.负极
(2)A所在周期中,E元素的单质还原性最强,A、E单质反应得到的化合物M是一种重要的化工原料,如图是电解100ml饱和M溶液的装置,X、Y都是惰性电极,实验开始时,同时在两边各滴入几滴酚酞试液,则

①电解池中Y极上的电极反应式
②电解一段时间后,若阴极收集到112ml标准状况下的气体,此时电解液的PH为
查看习题详情和答案>>
信息①原子半径大小:A>B>C>D
信息②四种元素之间形成的某三种分子的比例模型及部分性质:

请根据上述信息回答下列问题.
(1)①C元素在周期表中的位置
第二周期ⅥA族
第二周期ⅥA族
,请写出BC2分子的电子式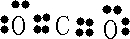
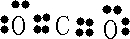
②A元素的单质与物质甲发生反应的离子方程式
Cl2+H2O H++Cl-+HClO
H++Cl-+HClO
 H++Cl-+HClO
H++Cl-+HClOCl2+H2O H++Cl-+HClO
H++Cl-+HClO
. H++Cl-+HClO
H++Cl-+HClO③以Pt为电极,KOH为电解质溶液,两极分别通入乙和C的单质可组成燃料电池,写出电池的电极反应式.负极
CH4-8e-+10OH-=CO32-+7H2O
CH4-8e-+10OH-=CO32-+7H2O
;正极2O2+8e-+4H2O=8OH-
2O2+8e-+4H2O=8OH-
(2)A所在周期中,E元素的单质还原性最强,A、E单质反应得到的化合物M是一种重要的化工原料,如图是电解100ml饱和M溶液的装置,X、Y都是惰性电极,实验开始时,同时在两边各滴入几滴酚酞试液,则

①电解池中Y极上的电极反应式
2Cl-2e-=Cl2↑
2Cl-2e-=Cl2↑
.检验Y电极反应产物的方法是把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色
把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色
.②电解一段时间后,若阴极收集到112ml标准状况下的气体,此时电解液的PH为
13
13
(假设电解液的体积保持不变,常温下)(2011?南关区二模)如图是部分常见元素的单质及其化合物的转化关系图(有关反应的条件及生成的部分产物已略去).
已知:E为红棕色固体,K为浅绿色溶液;反应①、②都是化工生产中的重要反应;B、C、D、H是单质;B、C、D、F、G、H常温下是气态; F、P 和H的水溶液均具有漂白作用,且F是形成酸雨的主要物质之一;N是一种常见的氮肥;化合物G为四原子10电子分子,化合物M由两种元素组成,分子内共有58个电子.
(1)写出F的化学式
 ;
;
(2)在G的水溶液中,阳离子浓度最大的是
(3)写出K与H反应的离子方程式
(4)在实验室中,向饱和H水溶液中加入CaCO3粉末,充分反应后过滤,可制得浓度较大的P的水溶液.用化学平衡移动的原理加以解释
查看习题详情和答案>>

已知:E为红棕色固体,K为浅绿色溶液;反应①、②都是化工生产中的重要反应;B、C、D、H是单质;B、C、D、F、G、H常温下是气态; F、P 和H的水溶液均具有漂白作用,且F是形成酸雨的主要物质之一;N是一种常见的氮肥;化合物G为四原子10电子分子,化合物M由两种元素组成,分子内共有58个电子.
(1)写出F的化学式
SO2
SO2
、P的电子式

(2)在G的水溶液中,阳离子浓度最大的是
NH4+
NH4+
(用离子符号表示)(3)写出K与H反应的离子方程式
2Fe2++Cl2=2Fe3++2Cl-
2Fe2++Cl2=2Fe3++2Cl-
;G与H反应的化学方程式4NH3+3Cl2=NCl3+3NH4Cl
4NH3+3Cl2=NCl3+3NH4Cl
(4)在实验室中,向饱和H水溶液中加入CaCO3粉末,充分反应后过滤,可制得浓度较大的P的水溶液.用化学平衡移动的原理加以解释
饱和H水溶液中存在平衡:Cl2+H2O H++Cl-+HClO,加入的CaCO3粉末与H+反应,平衡正向移动,HClO浓度增大
H++Cl-+HClO,加入的CaCO3粉末与H+反应,平衡正向移动,HClO浓度增大
 H++Cl-+HClO,加入的CaCO3粉末与H+反应,平衡正向移动,HClO浓度增大
H++Cl-+HClO,加入的CaCO3粉末与H+反应,平衡正向移动,HClO浓度增大饱和H水溶液中存在平衡:Cl2+H2O H++Cl-+HClO,加入的CaCO3粉末与H+反应,平衡正向移动,HClO浓度增大
H++Cl-+HClO,加入的CaCO3粉末与H+反应,平衡正向移动,HClO浓度增大
. H++Cl-+HClO,加入的CaCO3粉末与H+反应,平衡正向移动,HClO浓度增大
H++Cl-+HClO,加入的CaCO3粉末与H+反应,平衡正向移动,HClO浓度增大下列反应的离子方程式正确的是
| A.将0.1mol·L-1的NH4Al(SO4)2溶液与0.2mol·L-1的Ba(OH)2溶液等体积混合: Al3++2SO42-+2Ba2++4OH-=AlO2-↓+2BaSO4↓+2H2O |
| B.Ca(HCO3)2溶液与少量的NaOH溶液反应: Ca2+ + 2HCO3- +2OH- = CaCO3↓+ CO32- + 2H2O |
| C.向NaClO溶液中通入过量二氧化碳的离子方程式: 2ClO-+CO2+ H2O  |
D.氯气与水反应:Cl2+H2O H++Cl-+HclO H++Cl-+HclO |
 H++Cl-+HClO
H++Cl-+HClO