摘要:根据元素的价态进行判断: 元素处于最高价只有氧化性.最低价只有还原性.处于中间价态既有氧化又有还原性. 一般来说.同种元素价越高.氧化性越强,价越低还原性越强.如氧化性:Fe3+>Fe2+>Fe, S等.还原性:H2S>S>SO2.但是.氧化性:HClO4< HClO34< HClO24< HClO. 注意:①物质的氧化性.还原性不是一成不变的.同一物质在不同的条件下.其氧化能力或还原能力会有所不同.如:氧化性:HNO3(浓)>HNO3(稀),Cu与浓H2SO4常温下不反应.加热条件下反应,KMnO4在酸性条件下的氧化性比在中性.碱性条件下强. ②原子的氧化性一般都强于分子的氧化性.如:氧化性等. [例2]常温下.在下列溶液中发生如下反应 ①16H++10Z-+2XO4-=2x2++5Z2+8H2O ②2A2+ +B2=2A3++2B- ③2B-+Z2=B2+2Z- 由此判断下列说法错误的是( ) A.反应Z2+2A2+=2A3++2Z-可以进行. B.Z元素在①③反应中均被还原 C.氧化性由强到弱的顺序是XO4-.Z2.B2.A3+ D.还原性由强到弱的顺序是A2+.B-.Z-.X2+ [解析]根据上述规律4可得:氧化性顺序:XO4->Z2>B2>A3+.还原性顺序:A2+>B->Z->X2+. [答案]B 考点三 氧化还原反应方程式的配平方法
网址:http://m.1010jiajiao.com/timu_id_3702725[举报]
下面提供一些氧化还原反应:
①Fe+2HCl=FeCl2+H2↑
②2KMnO4+16HCl=2KCl+2MnCl2+ 5Cl2↑+8H2O
③2AgNO3 2Ag+2NO2↑+O2↑
2Ag+2NO2↑+O2↑
④C+CO2 2CO
2CO
⑤KClO3+6HCl=KCl+3Cl2↑+3H2O
⑥3S+6KOH=2K2S+K2SO3+3H2O
⑦HgS+O2 Hg+SO2
Hg+SO2
⑧2KNO3+3C+S K2S+N2↑+3CO2↑
K2S+N2↑+3CO2↑
⑨NH4NO3 N2O↑+2H2O
N2O↑+2H2O
⑩2KMnO4 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
请从不同的角度对上述氧化还原反应进行分类,把所选化学方程式的序号填在横线上。
(1)根据电子转移的元素种类,可有如下分类:
a.电子转移发生在同价态的同种元素之间的有________;
b.电子转移发生在不同价态的同种元素之间的有_______;
c.电子转移发生在不同种元素之间的有______。
(2)根据电子转移的物质种类,可有如下分类:
a.电子转移发生在不同物质之间的有_________;
b.电子转移发生在同一物质间的有__________。
(3)根据氧化剂和还原剂的种类,可有如下分类:
a.氧化剂和还原剂分别只有一种物质的有_____;
b.氧化剂和还原剂是同一种物质的有_________;
c.氧化剂或还原剂不止一种物质的有_________。 查看习题详情和答案>>
①Fe+2HCl=FeCl2+H2↑
②2KMnO4+16HCl=2KCl+2MnCl2+ 5Cl2↑+8H2O
③2AgNO3
 2Ag+2NO2↑+O2↑
2Ag+2NO2↑+O2↑④C+CO2
 2CO
2CO⑤KClO3+6HCl=KCl+3Cl2↑+3H2O
⑥3S+6KOH=2K2S+K2SO3+3H2O
⑦HgS+O2
 Hg+SO2
Hg+SO2⑧2KNO3+3C+S
 K2S+N2↑+3CO2↑
K2S+N2↑+3CO2↑⑨NH4NO3
 N2O↑+2H2O
N2O↑+2H2O⑩2KMnO4
 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑请从不同的角度对上述氧化还原反应进行分类,把所选化学方程式的序号填在横线上。
(1)根据电子转移的元素种类,可有如下分类:
a.电子转移发生在同价态的同种元素之间的有________;
b.电子转移发生在不同价态的同种元素之间的有_______;
c.电子转移发生在不同种元素之间的有______。
(2)根据电子转移的物质种类,可有如下分类:
a.电子转移发生在不同物质之间的有_________;
b.电子转移发生在同一物质间的有__________。
(3)根据氧化剂和还原剂的种类,可有如下分类:
a.氧化剂和还原剂分别只有一种物质的有_____;
b.氧化剂和还原剂是同一种物质的有_________;
c.氧化剂或还原剂不止一种物质的有_________。 查看习题详情和答案>>
氧化还原反应是一类重要的反应.回答下列问题:
(1)氧化还原反应在工农业生产、日常生活中都有广泛的用途.
①金属冶炼涉及氧化还原反应.许多金属的冶炼过程为:将金属氧化物(如Fe2O3)与具有特殊性质的物质(如CO)在一定条件下反应,从而得到该金属.从氧化还原反应的角度看,金属冶炼过程中,与金属氧化物反应的物质应具有
②钛被誉为21世纪金属.工业中通常用钠与钛的卤化物(TiCl4)共热来得到金属钛.该反应的化学方程式
(2)有些氧化还原反应却有危害.例如钢铁的腐蚀、食物的腐败等等.因此,要想方设法阻碍此类氧化还原反应的发生.
①罐头厂在装食物罐头时,添加一些防腐剂,防止食物被空气中的氧气氧化而变质.从氧化还原反应角度看,防腐剂具有
②在氧化还原反应中,氧化和还原、氧化剂和还原剂总是同时存在的.根据这一知识,如何有效避免有危害的氧化还原反应的发生(可通过实例说明).
答:
查看习题详情和答案>>
(1)氧化还原反应在工农业生产、日常生活中都有广泛的用途.
①金属冶炼涉及氧化还原反应.许多金属的冶炼过程为:将金属氧化物(如Fe2O3)与具有特殊性质的物质(如CO)在一定条件下反应,从而得到该金属.从氧化还原反应的角度看,金属冶炼过程中,与金属氧化物反应的物质应具有
还原性
还原性
(填化学性质).②钛被誉为21世纪金属.工业中通常用钠与钛的卤化物(TiCl4)共热来得到金属钛.该反应的化学方程式
TiCl4+4Na=4NaCl+Ti
TiCl4+4Na=4NaCl+Ti
(2)有些氧化还原反应却有危害.例如钢铁的腐蚀、食物的腐败等等.因此,要想方设法阻碍此类氧化还原反应的发生.
①罐头厂在装食物罐头时,添加一些防腐剂,防止食物被空气中的氧气氧化而变质.从氧化还原反应角度看,防腐剂具有
还原
还原
性.②在氧化还原反应中,氧化和还原、氧化剂和还原剂总是同时存在的.根据这一知识,如何有效避免有危害的氧化还原反应的发生(可通过实例说明).
答:
采用给金属覆盖保护层(如涂油漆、电镀等),真空包装食物等形式,使金属或食物与氧化剂隔离,从而阻止氧化还原反应发生
采用给金属覆盖保护层(如涂油漆、电镀等),真空包装食物等形式,使金属或食物与氧化剂隔离,从而阻止氧化还原反应发生
.硫酸是一种实验室常用的化学试剂.请按要求填空:
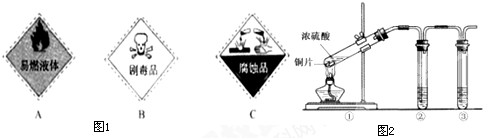
(1)浓硫酸试剂瓶上适合贴上的图标是图1中的 (填写字母标号).
(2)实验室有1.00mol?L-1的硫酸溶液,从中准确量出10.00mL,其物质的量浓度为 mol?L-1.现将准确量出的10.00mL的硫酸溶液配制成0.100mol?L-1的稀硫酸,所需要的玻璃仪器除烧杯、玻璃棒还需 和 .在配制过程中定容时俯视,则所配溶液浓度 (填“偏大”或“偏小”或“无影响”)
(3)用图2所示的实验装置②验证铜与浓硫酸反应生成的气体产物,则装置②、③中试剂依次为下列的 和
A.品红溶液 B.BaCl2溶液 C.NaOH溶液 D.AgNO3溶液
(4)装置①中发生反应的化学方程式为 若装置①中加入铜6.4g和含有0.2molH2SO4的浓硫酸,则产生二氧化硫质量
A.等于6.4克 B.大于6.4克 C.小于6.4克 D.不能确定
(5)若将装置①中的铜片换成木炭,装置②试管内为氢硫酸溶液,装置③试管内为澄清石灰水,则装置①中发生反应的化学方程式为 .装置②中主要反应的氧化剂和还原剂物质的量之比是 .根据装置③观察到有白色沉淀生成的现象 (填“能”或“不能”)判断该白色沉淀一定只有CaCO3.
查看习题详情和答案>>
(1)浓硫酸试剂瓶上适合贴上的图标是图1中的
(2)实验室有1.00mol?L-1的硫酸溶液,从中准确量出10.00mL,其物质的量浓度为
(3)用图2所示的实验装置②验证铜与浓硫酸反应生成的气体产物,则装置②、③中试剂依次为下列的
A.品红溶液 B.BaCl2溶液 C.NaOH溶液 D.AgNO3溶液
(4)装置①中发生反应的化学方程式为
A.等于6.4克 B.大于6.4克 C.小于6.4克 D.不能确定
(5)若将装置①中的铜片换成木炭,装置②试管内为氢硫酸溶液,装置③试管内为澄清石灰水,则装置①中发生反应的化学方程式为

(2011?奉贤区一模)过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等.某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质.
Ⅰ.测定过氧化的含量
请填写下列空白:
(1)移取10.00mL密度为ρ g/mL的过氧化氢溶液至250mL
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关化学式前的系数及化学式填写在横线上.
(3)滴定时,将高锰酸钾标准溶液注入滴定管中,滴定到达终点的现象是
(4)重复滴定二次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为
.
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果
Ⅱ.探究过氧化氢的性质
该化学举小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性.(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾淀粉溶液、饱和硫化氢溶液,实验仪器及用品可自选.)
请将他们的实验方法和实验现象填入下表:(只要完成其中一项探究即可)
查看习题详情和答案>>
Ⅰ.测定过氧化的含量
请填写下列空白:
(1)移取10.00mL密度为ρ g/mL的过氧化氢溶液至250mL
容量瓶
容量瓶
(填仪器名称)中,加水稀释至刻度,摇匀.移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样.(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关化学式前的系数及化学式填写在横线上.
2
2
MnO4-+5
5
H2O2+6
6
H+→2
2
Mn2++8
8
H2O+502
502
(3)滴定时,将高锰酸钾标准溶液注入滴定管中,滴定到达终点的现象是
滴入最后一滴高锰酸钾溶液,溶液呈紫红色,且30秒内不褪色
滴入最后一滴高锰酸钾溶液,溶液呈紫红色,且30秒内不褪色
.(4)重复滴定二次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为
| 0.085cV |
| ρ |
| 0.085cV |
| ρ |
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果
偏高
偏高
(填“偏高”“偏低”“不变”).Ⅱ.探究过氧化氢的性质
该化学举小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性.(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾淀粉溶液、饱和硫化氢溶液,实验仪器及用品可自选.)
请将他们的实验方法和实验现象填入下表:(只要完成其中一项探究即可)
| 实 验 内 容 | 实 验 方 法 | 实 验 现 象 |
| 探究氧化性 | 取适量饱和硫化氢溶液于试管中,滴入 过氧化氢溶液.(取适量碘化钾淀粉溶液于试管中,加入过氧化氢溶液.) 取适量饱和硫化氢溶液于试管中,滴入 过氧化氢溶液.(取适量碘化钾淀粉溶液于试管中,加入过氧化氢溶液.) |
产生淡黄色沉淀或溶液变浑浊.(溶液变蓝色.) 产生淡黄色沉淀或溶液变浑浊.(溶液变蓝色.) |
| 或探究不稳定性 | 取适量过氧化氢溶液于试管中,加热, 用带火星的木条检验.(取适量过氧化氢溶液于试管中,加热,用导气管将得到的气体通入到装有饱和硫化氢溶液的试管中.) 取适量过氧化氢溶液于试管中,加热, 用带火星的木条检验.(取适量过氧化氢溶液于试管中,加热,用导气管将得到的气体通入到装有饱和硫化氢溶液的试管中.) |
产生气泡,木条复燃.(溶液变浑浊或有浅黄色沉淀产生) 产生气泡,木条复燃.(溶液变浑浊或有浅黄色沉淀产生) |
 下列是治疗口腔炎症的药物华素片(西地碘含片)的部分使用说明书:
下列是治疗口腔炎症的药物华素片(西地碘含片)的部分使用说明书:| 使用说明书 | |
| 主要成分 | 活性分子碘含量:1.5mg/片 |
| 贮藏 | 遮光、密闭、在阴凉除保存 |
(1)推断华素片
(2)某同学欲证实该药片中含有碘分子,设计并完成如下实验:
①将药片研碎、溶解、过滤,所得滤液分装于甲、乙两试管中备用.
②向甲试管中加入下列一种试剂,振荡、静置,液体分层,上层液体颜色为
A.苯 B.酒精 C.四氯化碳 D.盐酸
③在乙试管中滴加
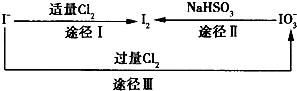
(3)碘在地壳中主要以NaI0的形式存在,在海水中主要以I的形式存在,几种粒子之间有如下所示的转化关系:
①如以海水为原料制取I,加入的Cl要适量.如过量就会发生途径Ⅲ的反应,在该反应的产物中,IO
- 3 |
②如用途径Ⅱ在溶液中制取I,反应后的溶液呈酸性,则反应的离子方程式