网址:http://m.1010jiajiao.com/timu_id_3698241[举报]
工业上用电解饱和食盐水的方法制取氯气,制得的氯气与另一电解产物在一定条件下反应生成两种盐A和B,其物质的量比为5:1,则盐A和B的化学式依次为 ,盐B在酸性条件下可与草酸(H2C2O4)反应制得气体ClO2,写出该反应的离子方程式: ,ClO2是当前对饮用水进行消毒的一种高效消毒剂,物质的量相等的ClO2和Cl2相比较,ClO2的消毒杀菌能力是Cl2的 倍。
查看习题详情和答案>>实验表明,液态时,纯硫酸的电离能力强于纯硝酸,纯硫酸的导电性也强于纯水.又知液态电解质都有能像水那样自身电离而建立电离平衡(即像![]()
![]()
![]() 一样),且在一定温度下都有各自的离子积常数.由此回答:
一样),且在一定温度下都有各自的离子积常数.由此回答:
(1)纯硫酸在液态时自身电离的电离反应是________,它在25℃时的离子积常数![]() 比1×
比1×![]() ________(填大或小,或相等).
________(填大或小,或相等).
(2)在纯硫酸与纯硝酸的液态混合酸中,存在的阴离子主要是________,这是因为混合液中不仅存在两种电离平衡(即![]() 和
和![]() 各自的电离反应)而且还因
各自的电离反应)而且还因![]() 的酸性强于
的酸性强于![]() ,又在无水条件下,混合酸中必发生(写离子反应式)________反应而造成的.故
,又在无水条件下,混合酸中必发生(写离子反应式)________反应而造成的.故![]() 与
与![]() 的无水混合酸中存在的化学平衡为________.
的无水混合酸中存在的化学平衡为________.
(3)由于硫酸(或浓![]() )的强烈吸水性,所以在
)的强烈吸水性,所以在![]() 与
与![]() 混合酸中还存在一种较为简单的含氮的阳离子,它是________.
混合酸中还存在一种较为简单的含氮的阳离子,它是________.
查看习题详情和答案>>
![]() 一样),且在一定温度下都有各自的离子积常数.由此回答:
一样),且在一定温度下都有各自的离子积常数.由此回答:
(1)纯硫酸在液态时自身电离的电离反应是________,它在25℃时的离子积常数![]() 比1×
比1×![]() ________(填大或小,或相等).
________(填大或小,或相等).
(2)在纯硫酸与纯硝酸的液态混合酸中,存在的阴离子主要是________,这是因为混合液中不仅存在两种电离平衡(即![]() 和
和![]() 各自的电离反应)而且还因
各自的电离反应)而且还因![]() 的酸性强于
的酸性强于![]() ,又在无水条件下,混合酸中必发生(写离子反应式)________反应而造成的.故
,又在无水条件下,混合酸中必发生(写离子反应式)________反应而造成的.故![]() 与
与![]() 的无水混合酸中存在的化学平衡为________.
的无水混合酸中存在的化学平衡为________.
(3)由于硫酸(或浓![]() )的强烈吸水性,所以在
)的强烈吸水性,所以在![]() 与
与![]() 混合酸中还存在一种较为简单的含氮的阳离子,它是________.
混合酸中还存在一种较为简单的含氮的阳离子,它是________.
查看习题详情和答案>>

回答下列问题:
(1)若甲、乙是两种常见金属,反应Ⅲ是工业制盐酸的反应.
①反应I中,甲在通常条件下和水剧烈反应,除丙外,还生成一种焰色反应为黄色的物质,则工业上生产甲的一般方法是
A.热分解法 B.热还原法 C.电解法
②反应Ⅱ中,乙与H2O在高温下反应,除丙外,还生成一种有磁性的物质,则反应Ⅱ的化学方程式是
③通过比较反应I、Ⅱ的反应条件,可得出甲的金属性比乙的金属性
(2)若甲、乙是化合物,且反应Ⅲ是工业制漂白粉的反应.
①反应Ⅲ的化学方程式是
②反应I的另一种产物为有机物,则该有机物的电子式是
③在饱和氯水中加块状石灰石,能制得较浓HClO溶液,同时放出一种气体.其反应的离子方程式是
回答下列问题:若甲、乙是两种常见金属,反应Ⅲ是工业制盐酸的反应.
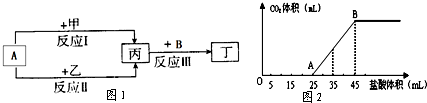
(1)反应I中,甲在通常条件下和A剧烈反应,除丙外,还生成一种焰色反应为黄色的物质,则工业上生产甲的一般方法是
A.热分解法 B.热还原法 C.电解法
(2)反应Ⅱ中,乙与A在高温下反应,除丙外,还生成一种有磁性的物质,则反应Ⅱ的化学方程式是
(3)通过比较反应I、Ⅱ的反应条件,可得出甲的金属性比乙的金属性强弱关系,比较二者金属性强弱的依据还可以是
(4)将3.5g甲的碳酸盐、碳酸氢盐和氢氧化物的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol?L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图2所示.
①写出OA段所发生反应的离子方程式
②当加入35mL盐酸时,产生CO2的体积为
(5)若甲、乙是化合物,反应Ⅲ是工业制漂白液的反应.其中乙为含有非极性键的离子化合物,若向氯化亚铁溶液中加入固体乙,产生红褐色沉淀,但无气体生成,该反应的离子方程式为