网址:http://m.1010jiajiao.com/timu_id_3696177[举报]
不看元素周期表,填写下表:
元素 符号 | 核电荷数 | 基态原子的简 化电子排布式 | 周期表中的位置 | 周期表中的位置与外 围电子层排布的关系 | ||
周期 | 族 | |||||
Na | 11 |
|
|
|
| 周 期 数 等 于 电 子 层 数 |
Ca | 20 |
|
|
| ||
Si | 14 |
|
|
| ||
As | 33 |
|
|
| ||
Cl | 17 |
|
|
| ||
Ti | 22 |
|
|
|
| |
Cr | 24 |
|
|
| ||
Mn | 25 |
|
|
| ||
Cu | 29 |
|
|
|
| |
Zn | 30 |
|
|
| ||
a |
|
|
|
|
|
| b |
|
|
| d | e | f | h |
|
c |
|
| g |
|
| i |
|
(1)“钻石恒久远,一颗永流传。”这句广告词被美国《广告时代》评为20世纪的经典广告之一,说的是上述元素中的_______________(填字母,下同)的一种单质,该广告词能体现的钻石的性质是_____________________。
a.硬度大 b.不能导电 c.化学性质稳定 d.熔点低
(2)钻石晶体中,一个原子位于正四面体的中心,周围四个原子位于四个顶点上,在空间构成连续的、坚固的骨架结构。因此,可以把一块该完美晶体看成一个巨大的“分子”。若有一颗质量为0.6 g的该完美晶体,可以认为它的“相对分子质量”是(阿伏加德罗常数取6.0×1023 mol-1)___________________。
(3)写出一个用金属置换出上表中能形成化合物种数最多的元素的单质的化学反应方程式:________________________________。
(4)2006年7月17日,“发现”号航天飞机出色完成任务后,顺利降落在佛罗里达州肯尼迪航天中心。有同学认为航天飞机内需要有一种化合物来吸收航天员呼出的CO2,同时提供另一种有用的气体,该化合物可能是由上表中的_____________(填字母)元素组成的。可实际上飞船中提供此有用气体的是它的液态单质而不是该化合物,你想这是基于什么考虑?(用文字与方程式简述理由)答:_________________________________________________。
(5)现有另一种元素,其原子获得一个电子所释放出的能量是上表中所列元素中最大的,则X是周期表中第______族元素。
查看习题详情和答案>>(13分)
第四周期过渡元素Fe、Ti可与C、H、N、O形成多种化合物。
(1)①H、C、N、O四种元素的电负性由小到大的顺序为 。
②下列叙述不正确的是 。(填字母)
A.因为HCHO与水分子间能形成氢键,所以CH2O易溶于水
B.HCHO 和CO2分子中的中心原子均采用sp2杂化
C.C6H6分子中含有6个![]() 键和1个大
键和1个大![]() 键,C2H2是非极性分子
键,C2H2是非极性分子
D.CO2晶体的熔点、沸点都比二氧化硅晶体的低
③氰酸(HOCN)是一种链状分子,它与异氰酸(HNCO)互为同分异构体,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式 。
(2) Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物。
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是
②六氰合亚铁离子[Fe(CN)6]4-中不存在__________。
a、共价键 b、非极性键 c、配位键 d、σ键 e、π键
并写出一种与 CN_ 互为等电子体的单质分子式______________________。
③三氯化铁常温下为固体,熔点,沸点
,在
:以上升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁的晶体类型为___________。
(3)①Ti的在周期表中位置______________ 。
根据元素原子的外电子排布的特征,可将元素周期表分成五个区域,其中Ti属于 区。
②Ti的一种氧化物X,其晶胞结构如上图所示,则X的化学式为 。工业上利用X和碳酸钡在熔融状态下制取化合物M(M可看做一种含氧酸盐),制备M的化学反应方程式是________________________________________;
查看习题详情和答案>>
(13分)
第四周期过渡元素Fe、Ti可与C、H、N、O形成多种化合物。
(1)①H、C、N、O四种元素的电负性由小到大的顺序为 。
②下列叙述不正确的是 。(填字母)
A.因为HCHO与水分子间能形成氢键,所以CH2O易溶于水
B.HCHO 和CO2分子中的中心原子均采用sp2杂化
C.C6H6分子中含有6个 键和1个大
键和1个大 键,C2H2是非极性分子
键,C2H2是非极性分子
D.CO2晶体的熔点、沸点都比二氧化硅晶体的低
③氰酸(HOCN) 是一种链状分子,它与异氰酸(HNCO)互为同分异构体
是一种链状分子,它与异氰酸(HNCO)互为同分异构体 ,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式 。
,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式 。
(2) Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物。
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是
②六氰合亚铁离子[Fe(CN)6]4-中不存在__________。
a、共价键 b、非极性键 c、配位键 d、σ键 e、π键
并写出一种与 CN_ 互为等电子体的单质分子式______________________。
③三氯化铁常温下为固体,熔点 ,沸点
,沸点 ,在
,在  :以上升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁的晶体类型为___________。
:以上升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁的晶体类型为___________。
(3)①Ti的在周期表中位置______________ 。
根据元素原子的外电子排布的特征,可将元素周期表分成五个区域,其中Ti属于 区。
②Ti的一种氧化物X,其晶胞结构如上图所示,则X的化学式为 。工业上利用X和碳酸钡在熔融状态下制取化合物M(M可看做一种含氧酸盐),制 备M的化学反应方程式是________________________________________;
备M的化学反应方程式是________________________________________;
(13分)
第四周期过渡元素Fe、Ti可与C、H、N、O形成多种化合物。
(1)①H、C、N、O四种元素的电负性由小到大的顺序为 。
②下列叙述不正确的是 。(填字母)
A.因为HCHO与水分子间能形成氢键,所以CH2O易溶于水
B.HCHO 和CO2分子中的中心原子均采用sp2杂化
C.C6H6分子中含有6个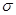 键和1个大
键和1个大 键,C2H2是非极性分子
键,C2H2是非极性分子
D.CO2晶体的熔点、沸点都比二氧化硅晶体的低
③氰酸(HOCN)是一种链状分子,它与异氰酸(HNCO)互为同分异构体,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式 。
(2) Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物。
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是
②六氰合亚铁离子[Fe(CN)6]4-中不存在__________。
a、共价键 b、非极性键 c、配位键 d、σ键 e、π键
并写出一种与 CN_ 互为等电子体的单质分子式______________________。
③三氯化铁常温下为固体,熔点 ,沸点
,沸点 ,在
,在
 :以上升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁的晶体类型为___________。
:以上升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁的晶体类型为___________。
(3)①Ti的在周期表中位置______________ 。
根据元素原子的外电子排布的特征,可将元素周期表分成五个区域,其中Ti属于 区。

②Ti的一种氧化物X,其晶胞结构如上图所示,则X的化学式为 。工业上利用X和碳酸钡在熔融状态下制取化合物M(M可看做一种含氧酸盐),制备M的化学反应方程式是________________________________________;
查看习题详情和答案>>