摘要: 导电类型: . .溶液导电性强弱决定因素:
网址:http://m.1010jiajiao.com/timu_id_3694428[举报]
某固体化合物A不导电,但熔化和溶于水中都能完全电离。下列关于A的说法中,正确的是?
A.A可能是共价化合物?
B.A与金刚石的晶体类型相同?
C.A中不可能有共价键?
D.A溶于水中时一定破坏了A中的离子键
查看习题详情和答案>>根据要求完成下列问题:
(1)分析下列物质的物理性质,判断其晶体类型:
A、固态时能导电,能溶于盐酸;B、能溶于CS2,不溶于水;C、固态、液态时均不导电,熔点3500℃
A、
(2)指出配合物K3[Co(CN)6]中的中心离子、配体及其配位数:
(3)在H2、SiC、CO2、HF中,由极性键组成的非极性分子是
查看习题详情和答案>>
(1)分析下列物质的物理性质,判断其晶体类型:
A、固态时能导电,能溶于盐酸;B、能溶于CS2,不溶于水;C、固态、液态时均不导电,熔点3500℃
A、
金属晶体
金属晶体
B、分子晶体
分子晶体
C、原子晶体
原子晶体
(2)指出配合物K3[Co(CN)6]中的中心离子、配体及其配位数:
Co3+
Co3+
、CN-
CN-
、6
6
.(3)在H2、SiC、CO2、HF中,由极性键组成的非极性分子是
CO2
CO2
,由非极性键形成的非极性分子是H2
H2
,能形成分子晶体的化合物是H2、CO2、HF
H2、CO2、HF
,含有氢键的晶体的化学式HF
HF
,属于原子晶体的是SiC
SiC
,四种物质熔点由高到低的顺序是SiC、HF、CO2、H2
SiC、HF、CO2、H2
.(1)氯酸钾熔化,粒子间克服了
(2)下列六种晶体:①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金刚石,它们的熔点从低到高的顺序为
(3)在H2、(NH4)2SO4、SiC、CO2、HF中,由极性键形成的非极性分子有
(4)A、B、C、D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于CS2,不溶于水
C.固态时不导电,液态时能导电,可溶于水
D.固态、液态时均不导电,熔点为3 500℃
试推断它们的晶体类型:A.
(5)图中A~D是中学化学教科书上常见的几种晶体结构模型,请填写相应物质的名称: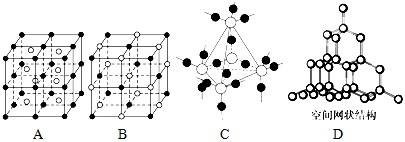
A.
查看习题详情和答案>>
离子键
离子键
的作用力;二氧化硅熔化,粒子间克服了共价键
共价键
的作用力;碘的升华,粒子间克服了分子间
分子间
的作用力.三种晶体的熔点由高到低的顺序是SiO2>KClO3>I2
SiO2>KClO3>I2
.(2)下列六种晶体:①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金刚石,它们的熔点从低到高的顺序为
①⑤③②④⑥
①⑤③②④⑥
(填序号).(3)在H2、(NH4)2SO4、SiC、CO2、HF中,由极性键形成的非极性分子有
CO2
CO2
,由非极性键形成的非极性分子有H2
H2
,能形成分子晶体的物质是H2、CO2、HF
H2、CO2、HF
,含有氢键的晶体的化学式是HF
HF
,属于离子晶体的是(NH4)2SO4
(NH4)2SO4
,属于原子晶体的是SiC
SiC
,五种物质的熔点由高到低的顺序是SiC>(NH4)2SO4>HF>CO2>H2
SiC>(NH4)2SO4>HF>CO2>H2
.(4)A、B、C、D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于CS2,不溶于水
C.固态时不导电,液态时能导电,可溶于水
D.固态、液态时均不导电,熔点为3 500℃
试推断它们的晶体类型:A.
金属晶体
金属晶体
;B.分子晶体
分子晶体
;C.离子晶体
离子晶体
;D.原子晶体
原子晶体
.(5)图中A~D是中学化学教科书上常见的几种晶体结构模型,请填写相应物质的名称:

A.
CsCl
CsCl
;B.NaCl
NaCl
;C.SiO2
SiO2
;D.金刚石
金刚石
.(1)短周期某主族元素M的电离能情况如图A所示.则M元素位于周期表的第

(2)图B是研究部分元素的氢化物的沸点变化规律的图象,折线c可以表达出第
(3)不同同学对某主族元素氢化物的沸点的变化趋势画出了两条折线--折线a和折线b,你认为正确的是:
(4)有三种固态物质,它们的性质如下:
A物质:无色晶体,熔点3550℃,不导电,质硬,难溶于水及有机溶剂.
B物质:无色晶体,溶于水,质硬而脆,熔点800℃,熔化时能导电.
C物质:熔点-56.6℃,微溶于水,硬度小,固态或液态时不导电.
根据上述性质,可推断A和B的晶体类型为:A为
查看习题详情和答案>>
IIIA
IIIA
族.
(2)图B是研究部分元素的氢化物的沸点变化规律的图象,折线c可以表达出第
IVA
IVA
族元素氢化物的沸点的变化规律,①②③中表示为SiH4的是②
②
(3)不同同学对某主族元素氢化物的沸点的变化趋势画出了两条折线--折线a和折线b,你认为正确的是:
b
b
,理由是:A点所示的氢化物是水,由于在水分子间存在氢键,所以其沸点高于氧族元素中的其它氢化物的沸点
A点所示的氢化物是水,由于在水分子间存在氢键,所以其沸点高于氧族元素中的其它氢化物的沸点
.(4)有三种固态物质,它们的性质如下:
A物质:无色晶体,熔点3550℃,不导电,质硬,难溶于水及有机溶剂.
B物质:无色晶体,溶于水,质硬而脆,熔点800℃,熔化时能导电.
C物质:熔点-56.6℃,微溶于水,硬度小,固态或液态时不导电.
根据上述性质,可推断A和B的晶体类型为:A为
原子
原子
晶体,B为离子
离子
晶体.有A、B、C三种晶体,分别由C、H、Na、Cl四种元素中的一种或几种形成,对这三种晶体进行实验,结果见下表.
(1)晶体的化学式分别为:A
(2)晶体的类型分别为:A
(3)晶体中粒子间的作用分别为:A
查看习题详情和答案>>
| 项目 | 熔点/℃ | 硬度 | 水溶性 | 导电性 | 水溶液与Ag+反应 |
| A | 811 | 较大 | 易溶 | 水溶液(或熔融)导电 | 白色沉淀 |
| B | 3 500 | 很大 | 不溶 | 不导电 | 不反应 |
| C | -114.2 | 很小 | 易溶 | 液态不导电 | 白色沉淀 |
NaCl
NaCl
;BC(金刚石)
C(金刚石)
;CHCl
HCl
.(2)晶体的类型分别为:A
离子晶体
离子晶体
;B原子晶体
原子晶体
;C分子晶体
分子晶体
.(3)晶体中粒子间的作用分别为:A
离子键
离子键
;B共价键
共价键
;C分子间作用力
分子间作用力
.