摘要:现有A.B.C.D.E.F六种短周期的元素.它们的原子序数依次增大.其中A与D.C与F分别为同一主族元素,A.D两元素的原子核内的质子数之和是C.F两元素原子核内质子数之和的一半,A的某种同位素原子核内无中子而B的气态氢化物的水溶液遇酚酞变红.请回答下列问题: (1)A.C两元素可形成X.Y两种化合物.其中X在MnO2作用下可以迅速分解得到Y.则X的电子式为 .其分子中含有 键(请用“极性 或“非极性 填空). (2)B.C的氢化物热稳定性顺序为(所涉及物质请用对应的分子式表示) . (3)E是一种金属元素.但也能表现出一定的非金属性.请写出单质E与氧氧化钾溶液反应的离子方程式 . (4)A的单质与C的单质在KOH溶液中可以形成燃料电池.如果M和N均为惰性电极.在电池的M极通入A的单质.N极通入C的单质.则M极的电极反应式为: . (5)请写出D2C2与FC2反应的化学方程式 . [答案](1) , 极性和非极性, (2) NH3<H2O, (3)2Al+2OH-+2H2O=2AlO2-+3H2↑ (4)H2―2e-+2OH- == 2 H2O (5)Na2O2 + SO2 = Na2SO4.
网址:http://m.1010jiajiao.com/timu_id_3691568[举报]
现有A、B、C、D、E、F六种短周期主族元素,其原子序数依次增大,已知A、D位于同一主族,A元素在元素周期表中原子半径最小,C是非金属性最强的元素,B、E原子最外层电子数相等,且B、E原子序数之和是A、D原子序数之和的两倍,F的最高价氧化物对应的水化物酸性最强.
(1)请在如图塔式元素周期表(元素周期表的另一种画法)相应位置中标出B元素的元素符号,同时在图中将过渡元素涂黑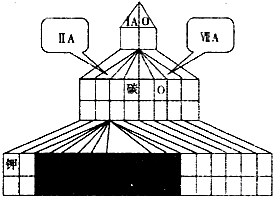
 .
.
(2)D元素的简单离子的离子结构示意图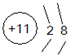
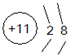
(3)B、E形成的气态氢化物的熔沸点那个高
(4)E与C或F均能形成一些化合物,据有关资料E与C能形成化合物EC6,E能与F能形成化合物E2F2.请回答下面问题:
①甲同学通过分析认为EC6此物质不可能在O2中燃烧,原因是:
②乙同学通过查资料知化合物E2F2中既存在极性键,又存在非极性键,试写出其电子式:
 ;该物质遇水不稳定,生成一种黄色沉淀和无色气体,还得到一种酸性溶液.试写出该过程的反应方程式
;该物质遇水不稳定,生成一种黄色沉淀和无色气体,还得到一种酸性溶液.试写出该过程的反应方程式
查看习题详情和答案>>
(1)请在如图塔式元素周期表(元素周期表的另一种画法)相应位置中标出B元素的元素符号,同时在图中将过渡元素涂黑


(2)D元素的简单离子的离子结构示意图
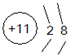
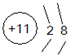
(3)B、E形成的气态氢化物的熔沸点那个高
H2O
H2O
,(用具体的化学式表示).(4)E与C或F均能形成一些化合物,据有关资料E与C能形成化合物EC6,E能与F能形成化合物E2F2.请回答下面问题:
①甲同学通过分析认为EC6此物质不可能在O2中燃烧,原因是:
硫在SF6中显+6价不可再升,O2不可将负一价氟氧化
硫在SF6中显+6价不可再升,O2不可将负一价氟氧化
,②乙同学通过查资料知化合物E2F2中既存在极性键,又存在非极性键,试写出其电子式:


2S2Cl2+2H2O=4HCl+SO2↑+3S↓
2S2Cl2+2H2O=4HCl+SO2↑+3S↓
.现有A、B、C、D、E、F六种短周期元素,原子序数依次增大.已知A与D、C与E分别同主族,D、E、F同周期;A、B的最外层电子数之和与C的最外层电子数相等,A与C形成的化合物常温下均为液态,A分别与E、F形成的气体分子电子总数相等.
请回答下列问题:
(1)元素B在周期表中的位置是
 .
.
(2)A2C比A2E沸点高的原因是
(3)在一定条件下,A、C的单质和A、C、D形成的离子化合物的水溶液可构成电池,该电池正极的电极反应式为
(4)化合物B2A4和B2C4的液体曾被用作火箭推进剂,燃烧反应的生成物是一种气态单质和一种化合物,它们对环境无污染.1mol B2A4与B2C4完全反应生成两种气体时放出热量516.8kJ,则该反应的热化学方程式为
查看习题详情和答案>>
请回答下列问题:
(1)元素B在周期表中的位置是
第二周期第ⅤA族
第二周期第ⅤA族
,元素D的原子结构示意图为

(2)A2C比A2E沸点高的原因是
H2O分子间存在氢键而H2S分子间不能形成氢键
H2O分子间存在氢键而H2S分子间不能形成氢键
.(3)在一定条件下,A、C的单质和A、C、D形成的离子化合物的水溶液可构成电池,该电池正极的电极反应式为
O2+2H2O+4e-═4OH-
O2+2H2O+4e-═4OH-
,负极的电极反应式为2H2+4OH--4e-═4H2O
2H2+4OH--4e-═4H2O
,该电池在放电过程中,电解质溶液的pH将减小
减小
(填“增大”、“减小”或“不变”).(4)化合物B2A4和B2C4的液体曾被用作火箭推进剂,燃烧反应的生成物是一种气态单质和一种化合物,它们对环境无污染.1mol B2A4与B2C4完全反应生成两种气体时放出热量516.8kJ,则该反应的热化学方程式为
2N2H4(l)+N2O4(l)═3N2(g)+4H2O(g)△H=-1033.6kJ?mol-1
2N2H4(l)+N2O4(l)═3N2(g)+4H2O(g)△H=-1033.6kJ?mol-1
.现有A、B、C、D、E、F六种短周期元素,在化学反应中均能形成简单的阴离子或阳离子,且A、B、C、D离子具有相同的电子层结构.已知:
①常温下,F的单质是一种有色气体,常用于杀菌、消毒;
②A的氧化物既能溶于NaOH溶液,又能溶于盐酸;
③C的氢化物分子G是具有10电子的微粒,且可以发生下列转化:G
P
Q
M+P
④E和D是同主族元素,氢化物(H2E)常温下为气态.
⑤B和D可形成微粒个数比为1:1和2:1的离子化合物X和Y.
请回答下列问题:
(1)C元素在周期表的位置
 .
.
(2)A元素的原子结构示意图是
 .化合物X所含化学键类型有
.化合物X所含化学键类型有
(3)G气体的检验方法为
(4)E的非金属性比F
查看习题详情和答案>>
①常温下,F的单质是一种有色气体,常用于杀菌、消毒;
②A的氧化物既能溶于NaOH溶液,又能溶于盐酸;
③C的氢化物分子G是具有10电子的微粒,且可以发生下列转化:G
| D的单质 |
| D的单质 |
| H2O |
④E和D是同主族元素,氢化物(H2E)常温下为气态.
⑤B和D可形成微粒个数比为1:1和2:1的离子化合物X和Y.
请回答下列问题:
(1)C元素在周期表的位置
N元素处于第二周期、ⅤA族
N元素处于第二周期、ⅤA族
;B2E的电子式为

(2)A元素的原子结构示意图是


离子键和共价键
离子键和共价键
.(3)G气体的检验方法为
将湿润的红色石蕊试纸靠近气体,若试纸变蓝,则该气体为NH3(其他合理答案也可)
将湿润的红色石蕊试纸靠近气体,若试纸变蓝,则该气体为NH3(其他合理答案也可)
.(4)E的非金属性比F
弱
弱
(填“强”或“弱”),并用化学事实加以说明(用化学方程式表示)H2S+Cl2=S+2HCl(其他合理答案也可)
H2S+Cl2=S+2HCl(其他合理答案也可)
.现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,A、D同主族,C与E同主族,D、E、F同周期,A、B的最外层电子数之和与C的最外层电子数相等,A能分别与B、C形成电子总数相等的分子,且A与C形成的化合物常温下为液态,A能分别与E、F形成电子总数相等的气体分子.
请回答下列问题:
(1)E、F气态氢化物的稳定性为
(2)E与F可形成E2F2的化合物,其电子式为
 ,其晶体类型为
,其晶体类型为
(3)C、D形成的一种化合物能与D、E形成的化合物在溶液中发生氧化还原反应,其离子方程式为:
(4)A、C、E三种元素形成的一种常见化合物H,其浓溶液在加热条件下可与a g铜反应,则被还原的H的物质的量为
mol
mol.
(5)E的一种常见氧化物为大气污染物,实验室可用足量D的最高价氧化物的水化物来吸收,则吸收生成的盐溶液中离子浓度大小关系为:
(6)b g D单质在纯净的C单质中燃烧放出Q kJ热量,则相关的热化学方程式为:
查看习题详情和答案>>
请回答下列问题:
(1)E、F气态氢化物的稳定性为
HCl
HCl
>H2S
H2S
(用化学式表示).(2)E与F可形成E2F2的化合物,其电子式为


分子晶体
分子晶体
.(3)C、D形成的一种化合物能与D、E形成的化合物在溶液中发生氧化还原反应,其离子方程式为:
Na2O2+S2-+2H2O=S↓+2Na++4OH-
Na2O2+S2-+2H2O=S↓+2Na++4OH-
.(4)A、C、E三种元素形成的一种常见化合物H,其浓溶液在加热条件下可与a g铜反应,则被还原的H的物质的量为
| a |
| 64 |
| a |
| 64 |
(5)E的一种常见氧化物为大气污染物,实验室可用足量D的最高价氧化物的水化物来吸收,则吸收生成的盐溶液中离子浓度大小关系为:
c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+)
c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+)
.(6)b g D单质在纯净的C单质中燃烧放出Q kJ热量,则相关的热化学方程式为:
2Na(s)+O2(g)=Na2O2(s)△H=-
kJ/mol
| 46Q |
| b |
2Na(s)+O2(g)=Na2O2(s)△H=-
kJ/mol
.| 46Q |
| b |
现有A、B、C、D、E、F六种短周期元素,在化学反应中均能形成简单的阴离子或阳离子,且A、B、C、D离子具有相同的电子层结构.已知:
①常温下,F的单质是一种有色气体,常用于杀菌、消毒;
②A的氧化物既能溶于NaOH溶液,又能溶于盐酸;
③C的氢化物分子G是具有10电子的微粒,且可以发生下列转化:G
P
Q
M+P
④E和D是同主族元素,氢化物(H2E)常温下为气态.
⑤B和D可形成微粒个数比为1:1和2:1的离子化合物X和Y.
请回答下列问题:
(1)A元素的原子结构示意图是 ;B2E的电子式为 .
(2)化合物X所含化学键类型有 .
(3)G气体的检验方法为 .
(4)写出F单质与E的氢化物反应的方程式并标明电子转移方向和数目 .
查看习题详情和答案>>
①常温下,F的单质是一种有色气体,常用于杀菌、消毒;
②A的氧化物既能溶于NaOH溶液,又能溶于盐酸;
③C的氢化物分子G是具有10电子的微粒,且可以发生下列转化:G
| D的单质 |
| D的单质 |
| H2O |
④E和D是同主族元素,氢化物(H2E)常温下为气态.
⑤B和D可形成微粒个数比为1:1和2:1的离子化合物X和Y.
请回答下列问题:
(1)A元素的原子结构示意图是
(2)化合物X所含化学键类型有
(3)G气体的检验方法为
(4)写出F单质与E的氢化物反应的方程式并标明电子转移方向和数目