摘要:比较金属性强弱的依据 金属性:金属气态原子失去电子能力的性质, 金属活动性:水溶液中.金属原子失去电子能力的性质. 注:金属性与金属活动性并非同一概念.两者有时表现为不一致.
网址:http://m.1010jiajiao.com/timu_id_3691318[举报]
对碳酸和硅酸的酸性强弱比较,以下几位同学选择的依据不同,得出了不同的结论.
王丽娜:二氧化碳通入硅酸钠溶液中可得到硅酸沉淀,所以,碳酸酸性比硅酸强.
张蕴昊:在高温条件下,将二氧化硅与碳酸钠共熔,得到了二氧化碳与硅酸钠,所以硅酸的酸性比碳酸强.
李莉珊:碳的非金属性比硅强,所以,碳酸酸性比硅酸强.
我的观点:
 已知A、B、C、D两种短周期元素,分别属于不同的主族,其原子序数依次增大,其中A与D、B与C的原子的最外层电子数之和均为9,A原子的最外层与次外层电子数相等,A、B、C、D中只有两种金属元素.试回答下列问题:
已知A、B、C、D两种短周期元素,分别属于不同的主族,其原子序数依次增大,其中A与D、B与C的原子的最外层电子数之和均为9,A原子的最外层与次外层电子数相等,A、B、C、D中只有两种金属元素.试回答下列问题:(1)A的元素符号为
Be
Be
,C的氢化物的化学式为H2S
H2S
.(2)为比较C与D的单质的氧化性强弱,可设计实验以证实,则该实验所依据的反应的化学方程式为
Fe+S
FeS,2Fe+3Cl2
2FeCl3(或H2S+Cl2═S↓+2HCl)
| ||
| ||
Fe+S
FeS,2Fe+3Cl2
2FeCl3(或H2S+Cl2═S↓+2HCl)
.
| ||
| ||
(3)1molC的氢化物与足量C的氧化物反应,转移的电子的物质的量为
2
2
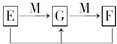
mol.(4)已知E、G、F是均含有B元素的化合物,其有关转化关系如图,请写出E与F反应生成G的离子方程式
Al3++3AlO2-+6H2O═4Al(OH)3
Al3++3AlO2-+6H2O═4Al(OH)3
.
已知A、B、C、D四种短周期元素,分别属于不同的主族,其原子序数依次增大。其中A与D、B与C的原子的最外层电子数之和均为9,A原子的最外层与次外层电子数相等,A、B、C、D中只有两种金属元素。试回答下列各题:
(1)A的元素符号为_______________,C的氢化物的化学式为_______________。
(2)为比较C与D的单质的氧化性强弱,可设计实验以证实,则该实验所依据的化学反应的化学方程式为_____________________________________________。
(3)1 mol C的氢化物与足量C的氧化物反应,转移的电子的物质的量为____________mol。
(4)已知E、G、F是均含有B元素的化合物,其有关转化关系如下:
![]()
请写出E与F生成G的离子方程式_____________________________________________。
查看习题详情和答案>>已知A、B、C、D两种短周期元素,分别属于不同的主族,其原子序数依次增大,其中A与D、B与C的原子的最外层电子数之和均为9,A原子的最外层与次外层电子数相等,A、B、C、D中只有两种金属元素.试回答下列问题:
(1)A的元素符号为________,C的氢化物的化学式为________.
(2)为比较C与D的单质的氧化性强弱,可设计实验以证实,则该实验所依据的反应的化学方程式为______________________________________.
(3)1 molC的氢化物与足量C的氧化物反应,转移的电子的物质的量为________mol.
(4)已知E、G、F是均含有B元素的化合物,其有关转化关系如下:
(1)A的元素符号为________,C的氢化物的化学式为________.
(2)为比较C与D的单质的氧化性强弱,可设计实验以证实,则该实验所依据的反应的化学方程式为______________________________________.
(3)1 molC的氢化物与足量C的氧化物反应,转移的电子的物质的量为________mol.
(4)已知E、G、F是均含有B元素的化合物,其有关转化关系如下:

请写出E与F反应生成G的离子方程式____________________________.
查看习题详情和答案>>
 2FeCl3(或H2S+Cl2═S↓+2HCl)
2FeCl3(或H2S+Cl2═S↓+2HCl)