网址:http://m.1010jiajiao.com/timu_id_3690967[举报]
实验室用NaOH 固体配制1.0mol/L的NaOH溶液500mL,回答下列问题
(1)配制溶液所需仪器为:容量瓶 (规格: )、托盘天平,还需要那些实验仪器才能完成该实验,请写出: 。
(2)在容量瓶的使用方法中,下列操作不正确的是(填编号)_ __。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近标线1~2cm处,用胶头滴管加蒸馏水到刻度线高考资源网
D.配制溶液时,如果试样是液体,用量筒量取试样后,直接倒入容量瓶中,缓慢加入蒸馏水到标线
E.盖好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶反复上下颠倒、摇匀
F.往容量瓶中转移溶液时应用玻璃棒引流
(3)在配制一定物质的量浓度的NaOH溶液时,下列哪个原因会造成所配溶液浓度偏高
A.称量固体NaOH时,有潮解现象 B.定容时俯视容量瓶的刻度线观察液面
C.称量时误用“左码右物”
D.溶解后移液直接转移至容量瓶中,未冷却溶液
E.未洗涤烧杯以及玻璃棒 F.定容时仰视容量瓶的刻度线观察液面
G.定容后,加盖倒转摇匀后,发现液面低于刻度线,又加水至刻度
H.容量瓶中原有少量蒸馏水。
查看习题详情和答案>>短周期元素X、Y、Z的原高考资源网子序数依次增大,X和Y同主族,Y和Z同周期,Y与Z能形成离子个数比为1︰1的离子化合物A,X与Z能形成原子个数比为1︰1的共价化合物B,它们之间能实现如下图所示转化(部分产物已略去):
(1)Y在周期表的位置是______________________;Z2的结构式是________。
(2)反应①的离子方程式____________________________________________。
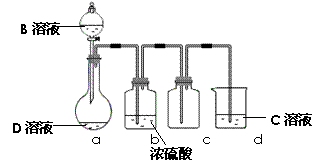 (3)D是很多漂白剂中含有的有效成分,这些产品不能与洁厕灵(含有有机酸和无机酸)一起使用,其原因就是在常温时能发生与反应②相似的反应。某校的学生在实验室利用反应②的原理来制备纯净、干燥的Z2,仪器装置如右图所示(夹持固定装置的仪器已略去)。
(3)D是很多漂白剂中含有的有效成分,这些产品不能与洁厕灵(含有有机酸和无机酸)一起使用,其原因就是在常温时能发生与反应②相似的反应。某校的学生在实验室利用反应②的原理来制备纯净、干燥的Z2,仪器装置如右图所示(夹持固定装置的仪器已略去)。
I、写出反应②的离子方程式_____________________
II、上述实验装置不够完善,改进方法是
Ⅲ、足量Z2 通入FeBr2溶液中发生反应的离子方程式是 。
查看习题详情和答案>>某氯化铁样品含有少量FeCl2杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行:

请根据上面流程,回答以下问题:
(1)操作I所用到的玻璃仪器除烧杯.玻璃棒.量筒外,还必须有____________ (填仪器名称),操作II必须用到的仪器是____________(填编号)。
A.50mL烧杯 B.50mL量筒
C.25mL碱式滴定管 D.25mL酸式滴定管
(2)洗涤是洗去附着在沉淀上的____________。(写离子符号)
(3)检验沉淀是否已经洗涤干净的操作是________________________。
(4)将沉淀物加热,并置高考资源网于干燥器中冷却至室温,用天平称量其质量为b1g,再次加热并冷却至室温称量其质量为b2g,若b1-b2=0.3g,则接下来还应进行的操作是_________。
(5)若蒸发皿质量是W1g,蒸发皿与加热后固体总质量是W2g,则样品中铁元素的质量分数是____________。
(6)有同学认为:上述流程中若不加入氯水,其它步骤不变,仍可达到目的。他的理由是________________________。(用化学方程式表示)
查看习题详情和答案>>某氯化铁样品含有少量FeCl2杂质.现要测定其中铁元素的质量分数,实验按以下步骤进行:
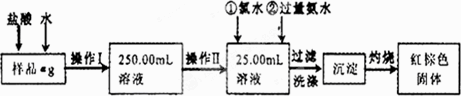
请根据上面流程,回答以下问题:
(1)操作Ⅰ所用到的玻璃仪器除烧杯.玻璃棒.量筒外,还必须有________ (填仪器名称),操作Ⅱ必须用到的仪器是________(填编号).
A.50 mL烧杯
B.50 mL量筒
C.25 mL碱式滴定管
D.25 mL酸式滴定管
(2)洗涤是洗去附着在沉淀上的________.(写离子符号)
(3)检验沉淀是否已经洗涤干净的操作是________.
(4)将沉淀物加热,并置高考资源网于干燥器中冷却至室温,用天平称量其质量为b1g,再次加热并冷却至室温称量其质量为b2 g,若b1-b2=0.3 g,则接下来还应进行的操作是________.
(5)若蒸发皿质量是W1 g,蒸发皿与加热后固体总质量是W2 g,则样品中铁元素的质量分数是________.
(6)有同学认为:上述流程中若不加入氯水,其它步骤不变,仍可达到目的.他的理由是________.(用化学方程式表示)