摘要:14.下列所列各物质的用途中.不正确的是-------.-------( ) A.分子筛:吸附剂.催化剂 B.硅胶:干燥剂.吸附剂.催化剂载体 C.碳化硅:砂纸.砂轮 D.硅酸:粘合剂.耐火材料
网址:http://m.1010jiajiao.com/timu_id_3685999[举报]
铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂。
(1)Cu位于元素周期表第I B族。Cu2+的核外电子排布式为 ▲ 。
(2)右图是铜的某种氧化物的晶胞结构示意图,可确定该晶胞中阴离子的个数为 ▲ 。
(3)胆矾CuSO4·5H2O可写成[Cu(H2O)4]SO4 ·H2O,其结构示意图如下:

下列说法正确的是 ▲ (填字母)。
A.在上述结构示意图中,所有氧原子都采用sp3杂化
B.在上述结构示意图中,存在配位键、共价键和离子键
C.胆矾是分子晶体,分子间存在氢键
D.胆矾中的水在不同温度下会分步失去
(4)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是 ▲ 。
酞菁也是常见的配位体,结构如右图。该分子中氮原子杂化方式为 ▲ 。 写出与硫酸根离子互为等电子体的分子和离子各一种 ▲ 、 ▲ 。

(5)Cu2O的熔点比Cu2S的 ▲ (填“高”或“低”),
请解释原因 ▲ 。
查看习题详情和答案>>合成氨生产技术的创立开辟了人工固氮的途径,对化学工业技术也产生了重大影响.合成氨反应的化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ?mol-1.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷或焦炭与水蒸气反应制得.
(1)在一容积固定的密闭容器中注入N2和H2两种气体,发生上述反应.在某温度下达到平衡时,各物质的浓度分别是:c(H2)=9.00mol?L-1,c(N2)=3.00mol?L-1,c(NH3)=4.00mol?L-1,此温度下该反应的平衡常数K=
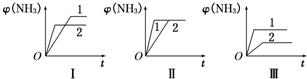
(2)在三个相同容器中各充入1mol N2和3mol H2,在不同条件下反应并达到平衡,氨的体积分数随时间变化的曲线如图所示.下列说法中正确的是
A.图Ⅰ可能是不同压强对反应的影响,且p2>p1
B.图Ⅱ可能是不同压强对反应的影响,且p1>p2
C.图Ⅲ可能是不同温度对反应的影响,且T1>T2
D.图Ⅱ可能是同温同压下不同催化剂对反应的影响,且催化剂性能1>2
(3)乙醇可通过淀粉等生物质原料发酵制得,属于可再生资源,通过乙醇制取氢气
具有良好的应用前景.已知通过乙醇制取氢气有如下两条路线:
a、CH3CH2OH(g)+H2O(g)?4H2(g)+2CO(g)△H=+255.58kJ/mol
b、CH3CH2OH(g)+1/2O2(g)?3H2(g)+2CO(g)△H=+13.76kJ/mol
下列说法错误的是:
A.从原料消耗的角度来看,a路线制氢更有价值
B.从能量消耗的角度来看,b路线制氢更加有利
C.a路线制氢由于要消耗很多能量,所以在实际生产中意义不大
D.降低温度,可提高b路线中乙醇的转化率.
查看习题详情和答案>>

(1)在一容积固定的密闭容器中注入N2和H2两种气体,发生上述反应.在某温度下达到平衡时,各物质的浓度分别是:c(H2)=9.00mol?L-1,c(N2)=3.00mol?L-1,c(NH3)=4.00mol?L-1,此温度下该反应的平衡常数K=
7.32×10-3
7.32×10-3
.(2)在三个相同容器中各充入1mol N2和3mol H2,在不同条件下反应并达到平衡,氨的体积分数随时间变化的曲线如图所示.下列说法中正确的是
D
D
(填字母,下同).A.图Ⅰ可能是不同压强对反应的影响,且p2>p1
B.图Ⅱ可能是不同压强对反应的影响,且p1>p2
C.图Ⅲ可能是不同温度对反应的影响,且T1>T2
D.图Ⅱ可能是同温同压下不同催化剂对反应的影响,且催化剂性能1>2
(3)乙醇可通过淀粉等生物质原料发酵制得,属于可再生资源,通过乙醇制取氢气
具有良好的应用前景.已知通过乙醇制取氢气有如下两条路线:
a、CH3CH2OH(g)+H2O(g)?4H2(g)+2CO(g)△H=+255.58kJ/mol
b、CH3CH2OH(g)+1/2O2(g)?3H2(g)+2CO(g)△H=+13.76kJ/mol
下列说法错误的是:
D
D
A.从原料消耗的角度来看,a路线制氢更有价值
B.从能量消耗的角度来看,b路线制氢更加有利
C.a路线制氢由于要消耗很多能量,所以在实际生产中意义不大
D.降低温度,可提高b路线中乙醇的转化率.