摘要:双水解反应: (1)构成盐的阴阳离子均能发生水解的反应为双水解反应.双水解反应相互促进.水解程度较大.有的甚至水解完全.其促进过程以NH4Ac为例解释如下: NH4Ac == NH4+ + Ac- NH4+ + H2ONH3·H2O + H+ Ac- + H2OHAc + OH- 两个水解反应生成的H+和OH-反应生成水而使两个水解反应的生成物浓度均减少.平衡均右移. (2)常见的双水解反应完全的为:Fe3+.Al3+与AlO2-.CO32-(HCO3-).S2-(HS-).SO32-(HSO3-),其特点是相互水解成沉淀或气体.双水解完全的方程式写“== 并标“↑↓ .其离子方程式配平依据是两边电荷平衡.如:2Al3+ + 3S2- + 6H2O == 2Al(OH)3↓+ 3H2S↑
网址:http://m.1010jiajiao.com/timu_id_3685397[举报]
用 表示阿伏加德罗常数的值,判断下列说法的正误:
表示阿伏加德罗常数的值,判断下列说法的正误:
(1)![]() 。?
。?
(2)在室温常压下,1 mol氖气含有的原子数为![]() 。?
。?
(3)1 mol白磷分子中所含共价键数为4![]() 。
。
(4)常温常压下,![]() 个CH4分子的体积大于
个CH4分子的体积大于
(5)标准状况下,![]() 。?
。?
(6)只有在熔化时,1 mol NaCl中才含有![]() 个Cl-。
个Cl-。
(7)1 mol金刚石和1 mol二氧化硅中所含C—C键、Si—O键数目均为2![]() 。?
。?
(8)在电解食盐水的实验中,测得电解后溶液的pH为14,又知电解后溶液总体积为![]() 。?
。?
(9)在常温常压下,![]() 。?
。?
(10)1 mol苯分子中含有的碳碳双键数为3![]() 。?
。?
(11)常温常压下,1 mol NO2气体与水在无氧条件下反应生成![]() 个NO
个NO![]() 。?
。?
(12)1 mol·L-1的醋酸钠溶液中含CH3COOH、CH3COO-共![]() 个。?
个。?
(13)![]() 。?
。?
(14)![]() 个阳离子。?
个阳离子。?
(15)![]() 。?
。?
(16)电解精炼铜时转移0.1![]() 个电子时阳极溶解
个电子时阳极溶解
(17)![]() 个图3-1所示的结构单元。
个图3-1所示的结构单元。

图3-1
???????
查看习题详情和答案>>已知:E为常见金属单质,C、D、F、I均为常见气体,其中C、D为单质,F、I为化合物,且组成元素相同,D、F有毒,I为直线型非极性分子,它们有如下框图关系: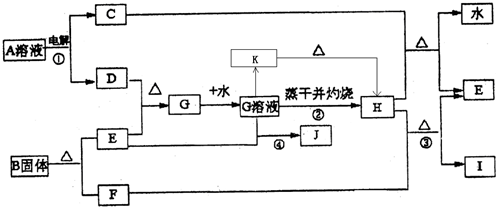
(1)反应①阳极的电极反应式
(2)反应③的化学方程式
(3)反应④的离子方程式为
(4)K是一种难溶于水的固体,K受热分解可生成H.实现由G溶液到K的转化时可以加入的试剂是(填写选项字母)
A.NaOH溶液 B.氨水 C.Na2CO3溶液 D.NaHCO3溶液
(5)将G的饱和溶液加入到沸水中,继续加热可得红褐色液体,写出反应的离子方程式:
(6)若E中含有合金元素,会导致G不纯.测定G的质量分数通常可用碘量法测定:称取mg无水G样品,溶于稀盐酸,再转移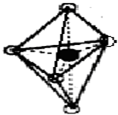 到
到
100mL容量瓶,用蒸馏水定容;取出10.00mL,加入稍过量的KI溶液,充分反应后,用淀粉作指示剂并用cmol?L-1Na2S2O3溶液滴定(I2+2S2O32-=2I-+S4O62-),共用去VmL.(杂质不参与反应)则样品中G的质量分数为:
×%
×%.
(7)B的结构为三角双锥(如图所示),图中○代表F分子,●代表E原子.则B的化学式为
查看习题详情和答案>>

(1)反应①阳极的电极反应式
2Cl--2e-=Cl2↑
2Cl--2e-=Cl2↑
.(2)反应③的化学方程式
Fe2O3+3CO
2Fe+3CO2
| ||
Fe2O3+3CO
2Fe+3CO2
.
| ||
(3)反应④的离子方程式为
2Fe3++Fe=3Fe2+
2Fe3++Fe=3Fe2+
.(4)K是一种难溶于水的固体,K受热分解可生成H.实现由G溶液到K的转化时可以加入的试剂是(填写选项字母)
ABCD
ABCD
A.NaOH溶液 B.氨水 C.Na2CO3溶液 D.NaHCO3溶液
(5)将G的饱和溶液加入到沸水中,继续加热可得红褐色液体,写出反应的离子方程式:
FeCl3+3H2O(沸水)=Fe(OH)3(胶体)+3HCl
FeCl3+3H2O(沸水)=Fe(OH)3(胶体)+3HCl
,该液体接通直流电后阴
阴
极附近颜色加深,这种过程叫做电泳
电泳
.(6)若E中含有合金元素,会导致G不纯.测定G的质量分数通常可用碘量法测定:称取mg无水G样品,溶于稀盐酸,再转移
 到
到100mL容量瓶,用蒸馏水定容;取出10.00mL,加入稍过量的KI溶液,充分反应后,用淀粉作指示剂并用cmol?L-1Na2S2O3溶液滴定(I2+2S2O32-=2I-+S4O62-),共用去VmL.(杂质不参与反应)则样品中G的质量分数为:
| 162.5Vc |
| m |
| 162.5Vc |
| m |
(7)B的结构为三角双锥(如图所示),图中○代表F分子,●代表E原子.则B的化学式为
Fe(CO)5或者FeC5O5
Fe(CO)5或者FeC5O5
.