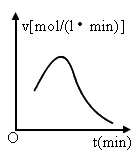摘要:已知氯酸钾和亚硫酸氢钠发生氧化还原反应.生成-1价的氯和+6价的硫的化合物.反应速率v和反应时间t的关系如图所示. 已知这个反应速率随溶液中氢离子浓度增大而加快.试解释: (1)反应开始时.反应速率加快的原因是 . (2)反应后期.反应速率下降的原因是 . 解析:由题意可知.该反应的速率随着c(H+)的增大而加快.因此必须把反应过程中c(H+)的变化及反应物浓度的变化结合考虑.才能得出该题的正确答案.该反应的化学方程式是:2KClO3+6NaHSO3=3Na2SO4+2KCl+3H2SO4.开始时.随着反应的进行.不断有强酸H2SO4生成.c(H+)不断增大.反应速率也随之增大.随着时间的延长.KClO3和NaHSO3被消耗而愈来愈少.浓度愈来愈小.因此反应速率下降. 答案:(1)开始时.随着反应的进行.不断有强酸H2SO4生成. ClO3-+3HSO3-=3SO42-+Cl-+3H+.c(H+)不断增大.反应速率也随之增大. (2)随着时间的延长.KClO3和NaHSO3被消耗而愈来愈少.H++ HSO3-=SO2↑+H2O.c(H+)浓度愈来愈小.因此反应速率下降. 知能训练
网址:http://m.1010jiajiao.com/timu_id_3685124[举报]
已知氯酸钾和亚硫酸氢钠发生氧化还原反应生成Cl-和含S6+粒子的速率如图2-4所示。已知这个反应速率随着溶液中C(H+)的增大而加快。

图2-4
(1)为什么反应开始一段时间内速率逐渐加快?
(2)为什么后期反应速率逐渐减慢?
查看习题详情和答案>>已知氯酸钾和亚硫酸氢钠发生氧化还原反应,生成-1价的氯和+6价的硫的化合物,反应速率(v)与时间(t)的关系如下图所示。
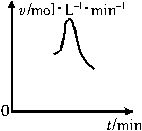
已知该反应的反应速率随溶液中氢离子浓度的增大而加快,试解释:
(1)反应开始时,反应速率加快的原因是__________________________________。
(2)反应后期,反应速率下降的原因是_____________________________________。
已知氯酸钾和亚硫酸氢钠发生氧化还原反应时,生成-1价的氯和+6价的硫的化合物,反应速v和反应时间,t的关系如图所示.

已知这个反应的反应速率随溶液中氢离子浓度增大而加快,试解释:
(1)反应开始后,反应速率加快的原因是_______________________.
(2)反应后期,反应速率下降的原因是_________________________.
查看习题详情和答案>>