摘要:压强对化学反应速率的影响 思考1:2L密闭容器中,投入5molN2,8molH2,在催化剂存在的条件下发生反应,2min 时,测得容器内生成NH34mol,若将容器的体积减小为原来的一半,其他条件不变,同样生成4molNH3所花费的时间 2min,为什么? 思考2:在室温条件,通过什么途径可以改变容器体积? 结论:有气体参与的反应,压强增大,化学反应速率 思考3:参加反应的物质是固体,液体或溶液时,压强对反应速率 影响? 例3.NO和CO都是汽车尾气中的有害物质.它们能缓慢地起反应.生成N2和CO2.对此反应的下列叙述中正确的是( ) A. 使用催化剂不能加快反应速率 B. 降低压强能加快反应速率 C. 升高温度能加快反应速率 D. 改变压强对化学反应速率无影响 解析:根据外界条件对反应速率影响的分析:使用催化剂一般能加快反应速率,对气体反应来说.压强的改变对反应速率有影响.增大压强会加快反应速率.减小压强会减慢反应速率,升高温度会加快反应速率.降低温度会减慢反应速率.据此可判断A.B.D说法错误.选项C说法正确. 探讨:N2 + 3H22NH3反应在密闭容器中进行
网址:http://m.1010jiajiao.com/timu_id_3685119[举报]
在某密闭容器中发生如下反应:A(g)+2B(g) xC(g);△H=a kJ·mol-1。某课外活动小组研究其它条件不变时,改变某一条件对上述反应的影响,满足下图关系[横坐标为时间t,纵坐标为C的体积分数φ(C)]。下列叙述不正确的是( )
xC(g);△H=a kJ·mol-1。某课外活动小组研究其它条件不变时,改变某一条件对上述反应的影响,满足下图关系[横坐标为时间t,纵坐标为C的体积分数φ(C)]。下列叙述不正确的是( )

A.研究压强对化学反应速率的影响时,甲的压强较大
B.研究压强对化学平衡的影响时,x>3
C.研究温度对化学反应速率的影响时,乙的温度较高
D.研究温度对化学平衡的影响时,a<0
查看习题详情和答案>>下列关于压强对化学反应速率的影响的说法中正确的是
[ ]
A.对于任何化学反应,增大压强都可加快它们的反应速率
B.对于气体反应,增大压强相当于增加反应物浓度,所以反应速率加快
C.对于固态或非固态反应物,由于压强对它们的体积改变很小,可以认为压强与它们的反应速率无关
D.增大压强可以加快合成氨的反应速率
查看习题详情和答案>>下列关于压强对化学反应速率的影响的说法中正确的是
[ ]
A.对于任何化学反应,增大压强都可加快它们的反应速率
B.对于气体反应,增大压强相当于增加反应物浓度,所以反应速率加快
C.对于固态或非固态反应物,由于压强对它们的体积改变很小,可以认为压强与它们的反应速率无关
D.增大压强可以加快合成氨的反应速率
查看习题详情和答案>>下列关于压强对化学反应速率的影响的说法中正确的是
- A.对于任何化学反应,增大压强都可加快它们的反应速率
- B.对于气体反应,增大压强相当于增加反应物浓度,所以反应速率加快
- C.对于固态或非固态反应物,由于压强对它们的体积改变很小,可以认为压强与它们的反应速率无关
- D.增大压强可以加快合成氨的反应速率
随着环保意识增强,清洁能源越来越受到人们关注.
(1)甲烷是一种理想的洁净燃料.已知:
CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-802.3kJ?mol-1
H2O(1)=H2O(g)△H=+44.0kJ?mol-1
则4.8g甲烷气体完全燃烧生成液态水,放出热量为
(2)利用甲烷与水反应制备氢气,因原料廉价,具有推广价值.
该反应为CH4(g)+H2O(g)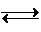 CO(g)+3H2(g)△H=+206.1kJ?mol-1.
CO(g)+3H2(g)△H=+206.1kJ?mol-1.
①若800℃时,反应的化学平衡常数K=l.0,某时刻测得该温度下密闭容器中各物质的物质的量浓度如下表.
则此时正、逆反应速率的关系是
A.v(正)>v(逆) B.v(正)<v(逆)C.v(正)=v(逆)D.无法判断
②为了探究温度、压强对上述化学反应速率的影响,张山同学设计了以下三组对比实验(温度为360℃或480℃、压强为101kPa或303kPa,其余实验条件见下表).
表中t=
设计实验2、3的目的是
实验l、2、3中反应的化学平衡常数的大小关系是
(3)利用催化剂,通过两步反应可将水分解制得氢气,若第一步反应为:MnFe2O4
MnFe2O4-x+
□↑,则框内物质为
第二步反应的化学方程式为
查看习题详情和答案>>
(1)甲烷是一种理想的洁净燃料.已知:
CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-802.3kJ?mol-1
H2O(1)=H2O(g)△H=+44.0kJ?mol-1
则4.8g甲烷气体完全燃烧生成液态水,放出热量为
267.1kJ
267.1kJ
.(2)利用甲烷与水反应制备氢气,因原料廉价,具有推广价值.
该反应为CH4(g)+H2O(g)
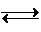 CO(g)+3H2(g)△H=+206.1kJ?mol-1.
CO(g)+3H2(g)△H=+206.1kJ?mol-1.①若800℃时,反应的化学平衡常数K=l.0,某时刻测得该温度下密闭容器中各物质的物质的量浓度如下表.
| CH4 | H2O | CO | H2 |
| 3.0mol?L-1 | 8.5mol?L-1 | 2.0mol?L-1 | 2.0mol?L-1 |
A
A
.(填下列相关选项的字母符号)A.v(正)>v(逆) B.v(正)<v(逆)C.v(正)=v(逆)D.无法判断
②为了探究温度、压强对上述化学反应速率的影响,张山同学设计了以下三组对比实验(温度为360℃或480℃、压强为101kPa或303kPa,其余实验条件见下表).
| 实验序号 | 温度/℃ | 压强/kPa | CH4初始浓度/mol?L-1 | H2O初始浓度/mol?L-1 | K |
| 1 | 360 | P | 2.00 | 6.80 | K1 |
| 2 | t | 101 | 2.00 | 6.80 | K2 |
| 3 | 360 | 101 | 2.00 | 6.80 | K3 |
480
480
,P=303
303
;设计实验2、3的目的是
探究温度对化学反应速率的影响
探究温度对化学反应速率的影响
;实验l、2、3中反应的化学平衡常数的大小关系是
K2>K1=K3
K2>K1=K3
(用K1、K2、K3表示).(3)利用催化剂,通过两步反应可将水分解制得氢气,若第一步反应为:MnFe2O4
| ||
| x |
| 2 |
O2
O2
;第二步反应的化学方程式为
xH2O+MnFe2O4-x=MnFe2O4+xH2↑
xH2O+MnFe2O4-x=MnFe2O4+xH2↑
(可不写反应条件).