摘要:温度对化学反应速率的影响:温度升高,化学反应速率 . 例2. 设C+CO22CO.反应速率为V1,N2+3H22NH3.反应速率为V2.对于上述反应.当温度升高时.V1和V2的变化情况为 A 同时增大 B 同时减小 C V1增大.V2减小 D V1减小.V2增大 解析:当温度升高时.无论正反应是吸热还是放热.化学反应速率都将增大.只不过增大的程度一个小一些.一个大些.本题易误解为:升高温度.C+CO22CO反应速率减小.原因是“正反应为吸热反应 .选 (A). 反思:一个化学反应的反应速率固然跟它的放热.吸热有关.但升高温度都将使化学反应速率增大.
网址:http://m.1010jiajiao.com/timu_id_3685118[举报]
(8分)化学反应的快慢和限度对人类生产生活有重要的意义。
(1)请将影响表中“实例”反应速率的“条件”仿照示例填在空格横线上。
| 实例 | 影响条件 |
| ①食物放在冰箱里能延长保质期 | 温度(示例) |
| ②实验室将块状药品研细,再进行反应 | ____________ |
| ③用H2O2分解制O2时,加入MnO2 | ____________ |
| ④工业制硫酸催化氧化SO2制取SO3时,通入过量的空气 | ____________ |

①写出该反应的化学方程式__________。
②从反应开始到10 s,用Z表示的反应速率为__________mol/(L·s)。
③该反应的化学平衡常数为__________(结果保留整数)。
④当反应进行到15 s时,向密闭容器中通入氩气,此时用Z表示的反应速率__________(填“小于”或“等于”或“大于”)10 s时用Z表示的反应速率。 查看习题详情和答案>>
某化学反应:3A(s)+B(g) 2C(g)+D(g) △H=xkJ/mol。恒温条件下,在一体积为2L的密闭容器中充入一定量A和B进行该反应,测得4s时反应放热225.6 kJ,并测得不同时间B的物质的量如下表所示
2C(g)+D(g) △H=xkJ/mol。恒温条件下,在一体积为2L的密闭容器中充入一定量A和B进行该反应,测得4s时反应放热225.6 kJ,并测得不同时间B的物质的量如下表所示
 2C(g)+D(g) △H=xkJ/mol。恒温条件下,在一体积为2L的密闭容器中充入一定量A和B进行该反应,测得4s时反应放热225.6 kJ,并测得不同时间B的物质的量如下表所示
2C(g)+D(g) △H=xkJ/mol。恒温条件下,在一体积为2L的密闭容器中充入一定量A和B进行该反应,测得4s时反应放热225.6 kJ,并测得不同时间B的物质的量如下表所示
请回答下列问题:
(1)x=__________。
(2)第2s时,a<__________。
(3)该温度下,该反应的平衡常数K=___________。
(4)平衡后下列措施既可提高正反应速率,又可降低B的转化率的是_________(填写序号)。
①使用催化剂
②升高反应体系的温度
③增大反应体系的压强
④扩大容器的体积
(5)为了探究温度、固体反应物的表面积对化学反应速率的影响,某同学在一体积为2L的密闭容器中加入一定量A和B,设计了三组实验,部分实验条件已经填写在下面的实验设计表中。
(1)x=__________。
(2)第2s时,a<__________。
(3)该温度下,该反应的平衡常数K=___________。
(4)平衡后下列措施既可提高正反应速率,又可降低B的转化率的是_________(填写序号)。
①使用催化剂
②升高反应体系的温度
③增大反应体系的压强
④扩大容器的体积
(5)为了探究温度、固体反应物的表面积对化学反应速率的影响,某同学在一体积为2L的密闭容器中加入一定量A和B,设计了三组实验,部分实验条件已经填写在下面的实验设计表中。

①请将上述实验设计表填写完整。
②请在如图坐标中画出上述三个实验条件下B的浓度随时间变化的曲线,并标明每条曲线的实验编号。
②请在如图坐标中画出上述三个实验条件下B的浓度随时间变化的曲线,并标明每条曲线的实验编号。
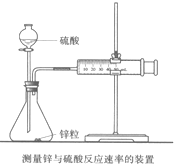
 影响化学反应速率的因素很多,某同学设计了以下实验研究不同浓度的硫酸对反应速率的影响.药品:Cu、Fe、Na和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L);装置如图.
影响化学反应速率的因素很多,某同学设计了以下实验研究不同浓度的硫酸对反应速率的影响.药品:Cu、Fe、Na和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L);装置如图.(1)用此装置进行定量实验,应选用上述的实验药品是:
Fe、0.5mol/L硫酸、2mol/L硫酸
Fe、0.5mol/L硫酸、2mol/L硫酸
;(2)应该测定的实验数据是
测定一定时间产生的体积(或者测定一定体积的气体所需的时间)
测定一定时间产生的体积(或者测定一定体积的气体所需的时间)
;(3)此实验忽视了影响反应速率的其他因素是(假设金属颗粒是均匀的):
温度对反应速率的影响
温度对反应速率的影响
. 影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究.
影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究.实验药品:铜、铁、镁、0.5mol/LH2SO4、2mol/LH2SO4、18.4mol/LH2SO4
甲同学研究的实验报告如下表:
| 实验步骤 | 现象 | 结论 |
| ①分别取等体积的2mol/L的硫酸于试管中 ② 分别投入大小、形状相同的铜、铁、镁 分别投入大小、形状相同的铜、铁、镁 |
反应速率镁>铁,铜不反应 | 金属的性质越活泼,反应速率越快 |
分别投入大小、形状相同的铜、铁、镁
分别投入大小、形状相同的铜、铁、镁
;(2)甲同学的实验目的是
研究金属本身的性质与反应速率的关系
研究金属本身的性质与反应速率的关系
;要得出正确的实验结论,还需要控制的实验条件是:温度相同
温度相同
;乙同学为了更精确的研究浓度对反应速率的影响,利用下图所示装置进行实验,(3)乙同学在实验中应该测定的数据是
一定时间内产生气体的体积(或产生一定体积的气体所需的时间)
一定时间内产生气体的体积(或产生一定体积的气体所需的时间)
;(4)乙同学完成该实验的应选用的实验药品
镁(或铁)和0.5mol/LH2SO4、2mol/LH2SO4
镁(或铁)和0.5mol/LH2SO4、2mol/LH2SO4
;该实验中不选用某浓度的硫酸,理由是常温下,镁与18.4mol/LH2SO4反应产生SO2,使对比实验的反应原理不同.18.4mol/LH2SO4使铁钝化
常温下,镁与18.4mol/LH2SO4反应产生SO2,使对比实验的反应原理不同.18.4mol/LH2SO4使铁钝化
.