摘要:Fe3+→Fe2+需要较强的还原剂.如Fe.Zn.H2S(S2-).KI(I-).Na2SO3(SO32-)等.Cu虽不是强的还原剂.但因Fe3+具有较强的氧化性.可被Cu还原成Fe2+. Cu+2FeCl3=CuCl2+2FeCl2,H2S+2FeCl3=2FeCl2+S↓+2HCl 2KI+2FeCl3=FeCl2+I2+2KCl
网址:http://m.1010jiajiao.com/timu_id_3684997[举报]
B.《实验化学》粗CuO是将工业废铜、废电线及废铜合金高温焙烧而成的,杂质主要是铁的氧化物及泥沙.以粗CuO为原料制备CuSO4?5H2O的主要步骤如下图所示:
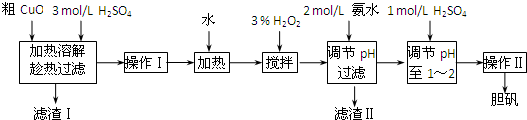
Fe3+、Fe2+、Cu2+转化为相应氢氧化物时,开始沉淀和沉淀完全时的pH如下表:
(1)加入3% H2O2之前需将热溶液冷却,其目的是 ,H2O2的作用是 .
(2)加入2mol/L氨水后,溶液的pH应在 范围内.
(3)经操作Ⅰ得到粗胆矾,经操作Ⅱ得到精制胆矾.两步操作相同,都包括 、抽滤、洗涤、干燥等步骤.某同学装配的抽滤装置如下图所示,该装置中的错误之处是 .
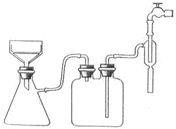
(4)调节溶液的pH常选用稀酸或稀碱,而不用浓酸、浓碱,理由是 .
查看习题详情和答案>>

Fe3+、Fe2+、Cu2+转化为相应氢氧化物时,开始沉淀和沉淀完全时的pH如下表:
| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物沉淀完全时的pH | 3.2 | 9.0 | 6.7 |
(2)加入2mol/L氨水后,溶液的pH应在
(3)经操作Ⅰ得到粗胆矾,经操作Ⅱ得到精制胆矾.两步操作相同,都包括

(4)调节溶液的pH常选用稀酸或稀碱,而不用浓酸、浓碱,理由是
(2012?湖南模拟)2011年8月12日,网传云南曲靖市越州镇约5000余吨的重毒化工废料铬渣非法丢放,毒水被直接排放到南盘江中.被污染的水中主要含有Cr3+,同时还含有少量的Cu2+、Fe2+、Fe3+和Al3+等,且酸性较强.
Ⅰ.污泥中Cr+回收与再利用工艺如下(硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+、Mg2+):
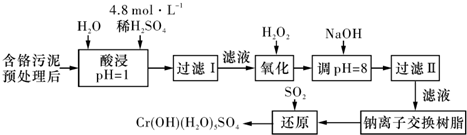
部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
(1)实验室用18.4mol?L-1的浓硫酸配制250mL 4.8mol?L-1的硫酸溶液,所用的玻璃仪器除烧杯、玻璃棒和吸量管(一种能精确量取一定体积液体的仪器)外,还需
(2)加入H2O2的作用是
(3)还原过程发生以下反应,请配平:
Na2SO4
Ⅱ.工业废水中常含有一定量的Cr2
和Cr
,它们会对人类及生态系统产生很大损害,必须进行处理.其中一种处理方法为电解法,该法用Fe做电极,电解含Cr2
的酸性废水,随着电解进行,阴极附近溶液pH升高,产生Cr(OH)3沉淀.
阳极的电极反应式为
电解时能否用Cu电极来代替Fe电极?
查看习题详情和答案>>
Ⅰ.污泥中Cr+回收与再利用工艺如下(硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+、Mg2+):

部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
| 开始沉淀时的pH | 1.9 | 7.0 | - | _ | 4.7 | - |
| 沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9(>9溶解) |
250mL容量瓶、胶头滴管.
250mL容量瓶、胶头滴管.
(2)加入H2O2的作用是
将滤液Ⅰ中的Cr3+转化为Cr2O72-,以便于与杂质离子分离
将滤液Ⅰ中的Cr3+转化为Cr2O72-,以便于与杂质离子分离
.调节溶液的pH=8是为了除去Fe3+、Al3+
Fe3+、Al3+
离子.(3)还原过程发生以下反应,请配平:
1
1
Na2Cr2O7+3
3
SO2+11
11
H2O
H2O
═2
2
Cr(OH)(H2O)5 SO4+Na2SO4
Na2SO4
Na2SO4
Ⅱ.工业废水中常含有一定量的Cr2
| O | 2- 7 |
| O | 2- 4 |
| O | 2- 7 |
阳极的电极反应式为
Fe-2e-═Fe2+
Fe-2e-═Fe2+
.电解时能否用Cu电极来代替Fe电极?
不能
不能
(填“能”或“不能”),理由是因阳极产生的Cu2+不能使Cr2O72-还原到低价态
因阳极产生的Cu2+不能使Cr2O72-还原到低价态
.