网址:http://m.1010jiajiao.com/timu_id_3684517[举报]
卤素单质的性质活泼,卤素的化合物应用广泛,运用化学反应原理研究卤族元素的有关性质具有重要意义。
(1)下列关于氯水的叙述正确的是_______(填写序号)。
A.氯水中存在两种电离平衡????????????????????
B.向氯水中通入SO2,其漂白性增强
C.向氯水中通入氯气,c( H+)/c(ClO-)减小???????
D.加水稀释氯水,溶液中的所有离子浓度均减小
E.加水稀释氯水,水的电离平衡向正反应方向移动
F.向氯水中加少量固体NaOH,可能有c(Na+)=c(Cl- )+c(ClO-)
(2)工业上通过氯碱工业生产氯气,其反应的离子方程式为______。
(3)常温下,已知25℃时有关弱酸的电离平衡常数:

写出84消毒液(主要成分为NaClO)露置在空气中发生反应的有关化学方程式________。若将84消毒液与洁厕剂(含有浓盐酸)混合使用可能会导致中毒,请用离子方程式解释有关原因___________。
(4)碘钨灯具有比白炽灯寿命长且环保节能的;特点。一定温度下,灯泡内封存的少量碘与使用过程中沉积在管壁上的钨可以发生反应:  。为模拟上述反应,准确称取0. 508g碘、0.736g金属钨置于50. 0mL的密闭容器中,加热使其反应。如图是 WI2(g)的物质的量随时间变化关系图象,其中曲线I(0~t2时间段)的反应温度为T1,曲线II(从t2开始)的反应温度为T2,且T2>T1。则
。为模拟上述反应,准确称取0. 508g碘、0.736g金属钨置于50. 0mL的密闭容器中,加热使其反应。如图是 WI2(g)的物质的量随时间变化关系图象,其中曲线I(0~t2时间段)的反应温度为T1,曲线II(从t2开始)的反应温度为T2,且T2>T1。则

①该反应的△H_______0(填“>。、=或“<”)
②从反应开始到t1时间内的平均反应速率v(I2)=_________。
③下列说法中不正确的是_________(填序号),
A.利用该反应原理可以提纯钨
B.该反应的平衡常数表达式是K=
C.灯丝附近温度越高,灯丝附近区域WI2越易变为W而重新沉积到灯丝上
(5)25℃时,向5mL含有KCI和KI浓度均为0.1mol/L的混合液中,滴加6mL0.1mol/L的AgNO3溶液,先生成的沉淀是_________,溶液中离子浓度由大到小的顺序是_______ [不考虑H+和OH-。25℃时
 ]。
]。
查看习题详情和答案>>
卤素单质的性质活泼,卤素的化合物应用广泛,运用化学反应原理研究卤族元素的有关性质具有重要意义。
(1)下列关于氯水的叙述正确的是_______(填写序号)。
A.氯水中存在两种电离平衡
B.向氯水中通入SO2,其漂白性增强
C.向氯水中通入氯气,c( H+)/c(ClO-)减小
D.加水稀释氯水,溶液中的所有离子浓度均减小
E.加水稀释氯水,水的电离平衡向正反应方向移动
F.向氯水中加少量固体NaOH,可能有c(Na+)=c(Cl- )+c(ClO-)
(2)工业上通过氯碱工业生产氯气,其反应的离子方程式为______。
(3)常温下,已知25℃时有关弱酸的电离平衡常数:
写出84消毒液(主要成分为NaClO)露置在空气中发生反应的有关化学方程式________。若将84消毒液与洁厕剂(含有浓盐酸)混合使用可能会导致中毒,请用离子方程式解释有关原因___________。
(4)碘钨灯具有比白炽灯寿命长且环保节能的;特点。一定温度下,灯泡内封存的少量碘与使用过程中沉积在管壁上的钨可以发生反应:  。为模拟上述反应,准确称取0. 508g碘、0.736g金属钨置于50. 0mL的密闭容器中,加热使其反应。如图是 WI2(g)的物质的量随时间变化关系图象,其中曲线I(0~t2时间段)的反应温度为T1,曲线II(从t2开始)的反应温度为T2,且T2>T1。则
。为模拟上述反应,准确称取0. 508g碘、0.736g金属钨置于50. 0mL的密闭容器中,加热使其反应。如图是 WI2(g)的物质的量随时间变化关系图象,其中曲线I(0~t2时间段)的反应温度为T1,曲线II(从t2开始)的反应温度为T2,且T2>T1。则
①该反应的△H_______0(填“>。、=或“<”)
②从反应开始到t1时间内的平均反应速率v(I2)=_________。
③下列说法中不正确的是_________(填序号),
A.利用该反应原理可以提纯钨
B.该反应的平衡常数表达式是K=
C.灯丝附近温度越高,灯丝附近区域WI2越易变为W而重新沉积到灯丝上
(5)25℃时,向5mL含有KCI和KI浓度均为0.1mol/L的混合液中,滴加6mL0.1mol/L的AgNO3溶液,先生成的沉淀是_________,溶液中离子浓度由大到小的顺序是_______ [不考虑H+和OH-。25℃时
 ]。
]。
B.苯和甲苯分别在浓硫酸条件下与浓硝酸反应,通过产物对比可以探究基团间的相互影响:该实验的结论是甲基对苯环产生了影响
C.乙醚是一种重要的有机溶剂,在苯酚和乙醇性质比较实验中,将等量的两者分别溶于乙醚,再投入金属钠,从而可以比较出羟基氢的活性
D.物质的分离提纯方法之一为“筛分”:如胶体—渗析法分离提纯;浊液—过滤分离,本质上就是依据所分离粒子的直径大小选择具有合适孔径的“筛子”
下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
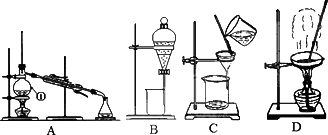
(1)从氯化钠溶液中得到氯化钠固体,选择装置________(填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置________;从碘水中分离出I2,选择装置________,该分离方法的名称为________.
(2)装置A中①的名称是________,进冷却水的方向是________.
装置B在分液时为使液体顺利下滴,应进行的具体操作是________.
(3)实验室中制取的Fe(OH)3胶体中常常含有杂质Cl-离子.可用________的方法除去Fe(OH)3胶体中混有的杂质Cl-离子.
某研究性学习小组探究溴的制备及提纯
●资料收集
| 溴 | 物理性质 | 暗红色液体,刺激性气味。室温下易挥发。熔点-7.2℃,沸点59.1℃。密度2.928g?cm-3。稍溶于冷水。 |
| 化学性质 | 溶于水生成次溴酸 |
●溴的制备
现只有下列试剂:溴化钾、MnO2、浓盐酸、稀硫酸、浓硫酸
(1)写出制取溴的化学方程式: 。
现只有下列仪器:(石棉网、导管、铁架台、塞子等略去)

(2)根据反应原理,制备和收集溴应该选择的仪器有: (填字母序号)。
●溴的提纯
实验室用蒸馏法提纯液溴,装置如图所示。

(3)蒸馏装置都用磨口玻璃器具,而不用橡胶管和橡胶塞连接,是因为
。
(4)装置4的作用是 。
(5)要想除去液溴中少量Cl2,可在液溴中加入 (填序号)后再分液分离即可。
①48%的氢溴酸 ②浓NaOH溶液 ③饱和KI溶液
查看习题详情和答案>>