摘要:离子化合物.共价化合物的导电性 离子化合物--阴.阳离子间通过离子键形成的化合物.固态不导电.溶于水或受热熔化时能导电. 共价化合物--不同的原子间通过共用电子对形成的化合物.液态都不导电.只有部分共价化合物溶于水时能导电.如能证明氯化氢是共价化合物的事实只能是:液态氯化氢不导电.
网址:http://m.1010jiajiao.com/timu_id_3684414[举报]
某无机化合物的二聚分子结构如图,该分子中A、B两种元素都是第三周期的元素,分子中所有原子最外层都达到8电子稳定结构。下列关于该化合物的说法不正确的是

[ ]
A.化学式是Al2Cl6
B.不存在离子键和非极性共价键
C.在固态时所形成的晶体是分子晶体
D.是离子化合物,在熔融状态下能导电
查看习题详情和答案>>
B.不存在离子键和非极性共价键
C.在固态时所形成的晶体是分子晶体
D.是离子化合物,在熔融状态下能导电
某无机化合物的二聚分子结构如图,该分子中A、B两种元素都是第三周期的元素,分
子中所有原子最外层都达到8电子稳定结构。下列关于该化合物的说法不正确的是( )
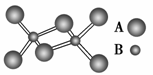
A.化学式是Al2Cl6
B.不存在离子键和非极性共价键
C.在固态时所形成的晶体是分子晶体
D.是离子化合物,在熔融状态下能导电
查看习题详情和答案>>
【化学—物质结构与性质】
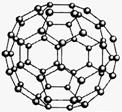 C60(结构模型如下图所示)的发现是化学界的大事之一。C60与金属钾化合生成K3C60。K3C60具有超导性。k.s.5.u
C60(结构模型如下图所示)的发现是化学界的大事之一。C60与金属钾化合生成K3C60。K3C60具有超导性。k.s.5.u
(1)碳原子的价电子排布式为 。
(2)C60分子中的杂化轨道介于石墨和金刚石的杂化轨道之间,则石墨和金刚石中碳原子的杂化方式分别是 、 。
(3)K3C60属于离子晶体,其中阴阳离子个数比为1∶3,则该晶体的构成微粒为 。(用化学式表示)
(4)已知C60晶体内相邻C60球体间的距离是304pm,与石墨平面层间距离(335pm)相比较,说明C60晶体中C60和C60间作用力属于 (填“离子键”、“共价键”或“分子间作用力”),两者数据存在差异的原因是 。
查看习题详情和答案>>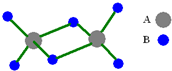 如图是某无机化合物的二聚分子,该分子中A、B两种元素都是第三周期的元素,分子中所有原子的最外层电子都达到8个电子的稳定结构.下列说法不正确的是( )
如图是某无机化合物的二聚分子,该分子中A、B两种元素都是第三周期的元素,分子中所有原子的最外层电子都达到8个电子的稳定结构.下列说法不正确的是( )