摘要:HCl 抑制水解平衡MgCl2+H2O Mg(OH)Cl+HCl正向进行
网址:http://m.1010jiajiao.com/timu_id_3684378[举报]
(2012?石家庄一模)目前高铁酸钠(Na2FeO4)被广泛应用于水处理,具有高效、无毒的优点.
(1)将Fe(OH)3与NaClO溶液混合,可制得Na2FeO4,完成并配平下列离子方程式
(2)某地海水样品经Na2FeO4处理后,所含离子及其浓度如下表所示(H+和0H-未列出):
常温下,取一定量经Na2FeO4处理过的海水为原料制备精制食盐水和MgCl2?7H20,过程如下:
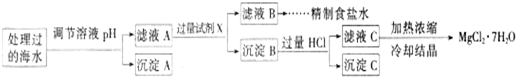
注:离子的浓度小于1.0×10-5mol/L,可认为该离子不存在;Ksp[Fe(OH)3]=1.0×10-38 Ksp[Mg(OH)2]=5.0×10-12;操作过程中溶液体积变化忽略不计.
①表格中的a
②沉淀A的组成为
③加入的过量试剂X为
④加入过量HCl的作用为
查看习题详情和答案>>
(1)将Fe(OH)3与NaClO溶液混合,可制得Na2FeO4,完成并配平下列离子方程式
2
2
Fe(OH)3+3
3
ClO-+4OH-
4OH-
=2
2
FeO42-+3
3
Cl-+5H2O
5H2O
(2)某地海水样品经Na2FeO4处理后,所含离子及其浓度如下表所示(H+和0H-未列出):
| 离子 | SO42- | Mg2+ | Fe3+ | Na+ | Cl- |
| 浓度(mol/L) | a | 0.05 | 0.10 | 0.50 | 0.58 |

注:离子的浓度小于1.0×10-5mol/L,可认为该离子不存在;Ksp[Fe(OH)3]=1.0×10-38 Ksp[Mg(OH)2]=5.0×10-12;操作过程中溶液体积变化忽略不计.
①表格中的a
>
>
0.16 (填“<”、“>”或“=”).②沉淀A的组成为
Fe(OH)3
Fe(OH)3
(填化学式)③加入的过量试剂X为
Ba(OH)2
Ba(OH)2
(填化学式)④加入过量HCl的作用为
使Mg(OH)2全部溶解转化为MgCl2;在加热浓缩滤液C时抑制Mg2+水解
使Mg(OH)2全部溶解转化为MgCl2;在加热浓缩滤液C时抑制Mg2+水解
.