摘要: 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑
网址:http://m.1010jiajiao.com/timu_id_3679923[举报]
|
下列反应的离子方程式不正确的是 | |
| [ ] | |
A. |
镁和稀硫酸 Mg+2H+ |
B. |
碳酸氢铵和足量烧碱溶液 HCO3-+OH- |
C. |
铜和浓硝酸 Cu+4H++2NO3- |
D. |
氯化铝溶液中加入足量的氨水 Al3++3NH3·H2O |
已知SiO2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定的相似性.
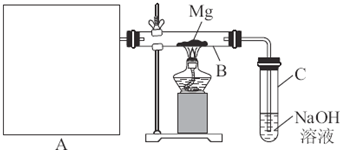
Ⅰ.用如图所示装置进行Mg和SO2的实验,其中A是制备SO2的发生装置.
(1)选择制取SO2的合适试剂
①10%的H2SO4溶液 ②80%的H2SO4溶液 ③Na2SO3固体 ④CaSO3固体
(2)写出装置B中发生的主要反应的化学方程式:
装置C中NaOH溶液的作用是
(3)请在图中画出制备SO2的发生装置并注明主要仪器的名称,固定仪器省略不画
 .
.
(4)你认为该装置的不足之处是
Ⅱ.某研究性学习小组进行了“实验室制Si”的研究,他们以课本为基础,查阅资料得到以下可供参考的信息:
①工业上在高温时用C还原SiO2可制得Si
②Mg在点燃的条件下即可与SiO2反应
③金属硅化物与稀H2SO4反应生成硫酸盐与SiH4
④Si和SiO2均不与稀H2SO4反应
⑤SiH4在空气中自燃
他们在研究报告中记载着:“…选用合适的物质在适宜的条件下充分反应,再用足量稀硫酸溶解固体产物;然后过滤、洗涤、干燥,最后称量…在用稀硫酸溶解固体产物时,发现有爆鸣声和火花,其产率也只有预期值的63%左右.”
(5)该小组“实验室制Si”的化学方程式是
(6)你估计“用稀硫酸溶解固体产物时,发现有爆鸣声和火花”的原因是
查看习题详情和答案>>
Ⅰ.用如图所示装置进行Mg和SO2的实验,其中A是制备SO2的发生装置.

(1)选择制取SO2的合适试剂
②③
②③
(填序号).①10%的H2SO4溶液 ②80%的H2SO4溶液 ③Na2SO3固体 ④CaSO3固体
(2)写出装置B中发生的主要反应的化学方程式:
3Mg+SO2
2MgO+MgS(或2Mg+SO2
2MgO+S,Mg+S
MgS)
| ||
| ||
| ||
3Mg+SO2
2MgO+MgS(或2Mg+SO2
2MgO+S,Mg+S
MgS)
.
| ||
| ||
| ||
装置C中NaOH溶液的作用是
吸收多余的SO2,防止污染环境
吸收多余的SO2,防止污染环境
.(3)请在图中画出制备SO2的发生装置并注明主要仪器的名称,固定仪器省略不画


(4)你认为该装置的不足之处是
在A和B之间没有连接一个干燥装置;C装置未与大气相通;在镁下方未垫一个不锈钢片,镁与玻璃管反应;未设计一个防倒吸装置
在A和B之间没有连接一个干燥装置;C装置未与大气相通;在镁下方未垫一个不锈钢片,镁与玻璃管反应;未设计一个防倒吸装置
.Ⅱ.某研究性学习小组进行了“实验室制Si”的研究,他们以课本为基础,查阅资料得到以下可供参考的信息:
①工业上在高温时用C还原SiO2可制得Si
②Mg在点燃的条件下即可与SiO2反应
③金属硅化物与稀H2SO4反应生成硫酸盐与SiH4
④Si和SiO2均不与稀H2SO4反应
⑤SiH4在空气中自燃
他们在研究报告中记载着:“…选用合适的物质在适宜的条件下充分反应,再用足量稀硫酸溶解固体产物;然后过滤、洗涤、干燥,最后称量…在用稀硫酸溶解固体产物时,发现有爆鸣声和火花,其产率也只有预期值的63%左右.”
(5)该小组“实验室制Si”的化学方程式是
2Mg+SiO2
2MgO+Si
| ||
2Mg+SiO2
2MgO+Si
.
| ||
(6)你估计“用稀硫酸溶解固体产物时,发现有爆鸣声和火花”的原因是
金属镁与生成的硅继续反应生成硅化镁,硅化镁与稀硫酸反应生成的SiH4可自燃
金属镁与生成的硅继续反应生成硅化镁,硅化镁与稀硫酸反应生成的SiH4可自燃
.某混合金属粉末,除Mg外,还含有Al、Zn中的一种或两种,含量都在10%以上.某研究小组设计实验探究该混合金属粉末中铝、锌元素的存在.
所用试剂:样品、pH试纸、稀H2SO4、NaOH溶液、稀NH3?H2O.
探究过程:
●查阅资料:
所用试剂:样品、pH试纸、稀H2SO4、NaOH溶液、稀NH3?H2O.
探究过程:
●查阅资料:
| ①镁、铝、锌都是银白色的金属 ②锌(Zn)可以与NaOH溶液反应生成H2 ③Zn(OH)2为白色固体,难溶于水,可溶于强碱及NH3?H2O ④Zn2+易形成络合物如[Zn(NH3)4]2+,该络合物遇强酸转化变成Zn2+、NH4+●提出假设: (1)假设①:该混合金属粉末中除镁外还含有 假设②:该混合金属粉末中除镁外还含有 假设③:该混合金属粉末中除镁外还含有铝、锌. ●实验探究: 甲同学基于假设③设计实验方案: 操作Ⅰ是在滤液中逐滴加入稀硫酸,直至生成的沉淀刚好溶解,再加足量的稀氨水,请回答:  乙同学基于假设③设计另一方案:  (2)沉淀A、B、D的化学式:A (3)甲同学用样品和稀硫酸反应所得溶液含有较多H+、Mg2+、Al3+、SO42-,向其中滴入NaOH溶液,生成沉淀的量与加入NaOH溶液体积关系可能正确的是  (4)乙同学方案的操作②中,铝与NaOH溶液反应的化学方程式为 操作②与操作③中都加了NaOH溶液,但其用量差别是 (5)丙同学通过分析对比,认为乙的方案比甲同学的好,其理由可能是 |