网址:http://m.1010jiajiao.com/timu_id_3674301[举报]
医用氯化钙可用于补钙、抗过敏和消炎等,以工业碳酸钙(含少量Na+、Al3+、Fe3+等杂质)生产医用二水合氯化钙(CaCl2·2H2O的质量分数为97.3-103.0%),工艺流程为:

(1)CaCO3与
盐酸反应的离子方程式________.(2)
除杂操作是加入氢氧化钙,调节溶液的pH为8.0~8.5,以除去溶液中少量的Al3+、Fe3+.检验Fe(OH)3是否沉淀完全的实验操作是________.(3)过滤时需用的玻璃仪器除烧杯、玻璃棒外还有________.滤渣主要成分的化学式________.
(4)酸化时加盐酸的目的为:①________,②防止Ca2+在蒸发时发生水解.
(5)为什么蒸发结晶要保持在160℃:________.
(6)为测定样品中CaCl2·2H2O的含量,称取0.75 g样品并配成250 mL溶液,各取该溶液25.00 mL,分别置于三个锥形瓶中,用0.04 mol/L AgNO3溶液进行三次滴定,消耗AgNO3溶液的平均体积为20.00 mL.
①通过计算,样品中含CaCl2·2H2O的质量分数为________.
②若所测样品CaCl2·2H2O的质量分数偏高(忽略其它实验误差),可能的原因之一为________.
A.《化学与生活》
(1)材料是人类赖以生存和发展的重要物质基础.
①生产水泥的主要原料是黏土和
②有机玻璃(聚甲基丙烯酸甲酯)实际上不是硅酸盐材料,而是一种
③上海世博会中国馆用到一种涂料-氟碳涂层聚酯(FEP),它的单体为CF3-CF=CF2,这种涂料具有
④玻璃钢具有耐腐蚀、质量轻、强度高的性能,它属于
(2)人体健康与食品、药物等关系密切.
①有些学生从小偏食,不爱吃水果、蔬菜,结果营养缺乏、发育不良,这主要是由于摄取
②生活中应合理地摄取人体必需的元素,体内
③糖类、油脂、蛋白质都是人体必需的营养物质.其中蛋白质被摄入人体后,在酶的作用下水解为
④小苏打可用来治疗胃酸过多,请写出该反应的离子方程式
⑤可以帮助流感病人解热镇痛的药物是
(3)洁净安全的生存环境更是健康的保障.
①为确保上海世博会期间城市空气质量优良率达到95%以上,世博会期间的空气质量状况监测中,不需要监测的指标是
a.可吸入颗粒物(PM10) b.NO2浓度 c.SO2浓度 d.CO2浓度
②自来水可利用漂白粉来杀菌消毒,其能杀菌消毒的原因(用化学反应方程式表示)是
③垃圾的无害化处理常用的方法包括卫生填埋和
④人们为追求时尚而把头发染成各种各样的颜色,常见的染发剂有植物染发剂、无机染发剂和
B.(1)具有明显现象的官能团特征反应常被用来鉴定化合物.
①欲区分CH2=CH2和CH3CH3,应选用
a.NaOH溶液 b.溴水 c.银氨溶液
②欲区分HCHO和HCOOH,应选用
a.KMnO4溶液 b.银氨溶液 c.Na2CO3溶液
③欲区分
 和
和 ,应选用
,应选用a.FeCl3溶液 b.NaOH溶液 c.AgNO3溶液
(2)在有机化学中,同分异构是普遍存在现象.分子式为C4H9OH的有机物共有
种.其中,一种有机物通过消去反应可转变为2-丁烯,请写出该消去反应的化学方程式
| ||
| △ |
| ||
| △ |


(3)A是石油裂解气的成分之一,A的某一同系物E的产量通常用来衡量一个国家的石油化工水平.现以A为主要原料合成C6H12O2,其合成路线如图所示:

回答下列问题:
①A的结构简式为:
②B、D分子中的官能团名称分别为
③写出B的同类别的同分异构体的结构简式:


④写出B→C的化学方程式:
| ||
| △ |
| ||
| △ |
(1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为
(2)漂白粉的有效成分是(填化学式)
(3)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为
(4)据报道,在全国各地发生了不当使用洁污剂发生氯气中毒的事件.“84消毒液”中含有NaClO,当它和呈酸性的家用“洁厕净”(主要成分为工业盐酸)等混合时,就会发生反应生成氯气,从而导致中毒,写出发生反应生成氯气的化学方程式
Ⅰ.电石
| 水 |
| 自然风干 |
①电石与水反应的化学方程式是
②残渣中主要成分是Ca(OH)2和
Ⅱ.将Ⅰ中的部分灰浆配成浊液,通入Cl2,得到Ca(ClO3)2与CaCl2物质的量之比为1:5的溶液,反应的化学方程式是
Ⅲ.向Ⅱ所得溶液中加入KCl,发生复分解反应,经蒸发浓缩,冷却结晶,过滤得KClO3 晶体.你认为能得到KClO3 晶体的原因是
Ⅳ.将Ⅰ中的残渣溶于NH4Cl溶液,加热,收集挥发出的气体再利用.向所得CaCl2溶液中依次通入NH3、CO2,便可获得超细CaCO3,过程如下:

①根据沉淀溶解平衡原理,解释残渣中难溶盐的溶解原因
②CaCl2溶液中通入两种气体后,生成超细CaCO3的化学方程式是
③图示的溶液A可循环使用,其主要成分的化学式是
(12 分)
KClO3在农业上用作除草剂,超细CaCO3泛用于消光纸、无炭复写纸等。某同学在实验室模拟工业过程,利用制乙炔产生的残渣制备上述两种物质,过程如下:
①电石与水反应的化学方程式是__________。
②残渣中主要成分是Ca(OH)2和________。
II.将I中的部分灰浆配成池液,通人Cl2,得到Ca(Clo3)2与Cacl2物质的量之比为1:5的溶液,反应的化学方程式是________________
III.向II所得溶液中加人KCl,发生复分解反应,经蒸发浓缩,冷却结晶,过滤得KClO3晶体。你认为能得到KClO3晶体的原因是________________。
IV.将I中的残渣溶于NH4Cl溶液,加热,收集挥发出的气体再利用。向所得CaCl2溶液中依次通入NH3、C02,便可获得超细CaCO3,过程如下:
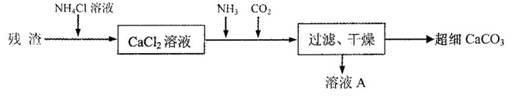
①根据沉淀溶解平衡原理,解释残渣中难溶盐的溶解原因________。
②CaCl2溶液中通入两种气体后,生成超细CaCO3的化学方程式是________。
③图示的溶液A可循环使用,其主要成分的化学式是________
查看习题详情和答案>>
