摘要: ⑴.⑹.2.B [针对训练]
网址:http://m.1010jiajiao.com/timu_id_3672762[举报]
工业上可以从电解铜的阳极泥中提取很多重要物质,其工艺流程如下:
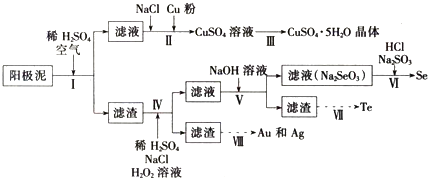
已知:①阳极泥的主要化学成分,如表所示
②温度和硫酸浓度对阳极泥中各组分浸出率的影响,如表所示
(1)步骤I的主要目的为浸出铜,此过程中发生的主要反应的化学方程式为 ,分析表2数据,可知步骤I最适合的条件为 .
(2)步骤Ⅱ中,加入Cu粉的目的是除去滤液中含碲的离子,加入NaCl的目的为 .
(3)步骤Ⅲ的操作方法为 .
(4)步骤Ⅳ中,反应温度为75℃.加入H2O2溶液的作用为 ;此过程中H2O2溶液的添加量要远远高于理沧值,原因为 .
(5)步骤Ⅵ中所发生反应的化学方程式为 .
(6)步骤Ⅶ中,Te的获得可以通过碱性环境下电解Na2TeO3溶液实现,其阴极的电极反应式为 .
(7)步骤Ⅷ中得到的Au和Ag混合物可以用 进行分离(填选项字母).
A.稀硝酸 B.浓盐酸 C.浓氢氡化钠溶液 D.王水. 查看习题详情和答案>>

已知:①阳极泥的主要化学成分,如表所示
| 主要成分 | Cu | Ag | Au | Se | Te |
| 百分含量/% | 23.4 | 12.1 | 0.9 | 6.7 | 3.1 |
| 固定浸出温度 | 固定H2SO4浓度 | |||||||||||
| H2SO4浓度/mol?L-1 | 浸出率/% | 浸出温度/℃ | 浸出率/% | |||||||||
| Cu | Ag | Au | Se | Te | Cu | Ag | Au | Se | Te | |||
| 4 | 95.1 | 4.67 | <0.2 | 0.83 | 8.93 | 30 | 87.1 | 4.58 | <0.2 | 0.08 | 6.83 | |
| 3 | 94.5 | 4.65 | <0.2 | 0.28 | 6.90 | 40 | 94.5 | 4.65 | <0.2 | 0.28 | 6.90 | |
| 2 | 78.1 | 2.65 | <0.2 | 0.05 | 2.85 | 50 | 96.1 | 5.90 | <0.2 | 0.64 | 8.73 | |
(2)步骤Ⅱ中,加入Cu粉的目的是除去滤液中含碲的离子,加入NaCl的目的为
(3)步骤Ⅲ的操作方法为
(4)步骤Ⅳ中,反应温度为75℃.加入H2O2溶液的作用为
(5)步骤Ⅵ中所发生反应的化学方程式为
(6)步骤Ⅶ中,Te的获得可以通过碱性环境下电解Na2TeO3溶液实现,其阴极的电极反应式为
(7)步骤Ⅷ中得到的Au和Ag混合物可以用
A.稀硝酸 B.浓盐酸 C.浓氢氡化钠溶液 D.王水. 查看习题详情和答案>>
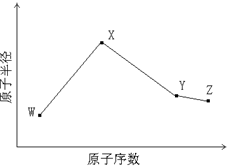 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为14,中子数为7;X的离子与NH4+具有相同的质子、电子数目; W与Y的氧化物均能导致酸雨的形成;Z的非金属性在同周期主族元素中最强.
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为14,中子数为7;X的离子与NH4+具有相同的质子、电子数目; W与Y的氧化物均能导致酸雨的形成;Z的非金属性在同周期主族元素中最强.(1)Y在周期表中的位置是
(2)用电子式解释X与W能形成化合物X3W的原因
(3)X3W遇水可释放出使酚酞溶液变红的气体A,化学方程式是
(4)用惰性电极电解化合物XZ溶液从阴极释放出气体B,反应的离子方程式是
(5)已知W的单质与气体B在一定条件下可形成气体A,即:W2(g)+3B (g)?2A(g)△H=-92.4kJ?mol-1
在某温度时,一个容积固定的密闭容器中,发生上述反应.在不同时间测定的容器内各物质的浓度如下表:
| 时间 | 浓度(mol/L) | ||
| c(W2) | c(B) | c(A) | |
| 第0min | 4.0 | 9.0 | 0 |
| 第10min | 3.8 | 8.4 | 0.4 |
| 第20min | 3.4 | 7.2 | 1.2 |
| 第30min | 3.4 | 7.2 | 1.2 |
| 第40min | 3.6 | 7.8 | 0.8 |
②反应在第10min改变了反应条件,改变的条件可能是
a.更新了催化剂 b.升高温度 c.增大压强 d.增加B的浓度
③若反应从第30min末又发生了一次条件改变,改变的反应条件可能是
a.更新了催化剂 b.升高温度 c.增大压强 d.减小A的浓度.
下表中元素均为中学化学中常见短周期元素,根据表中信息,下列说法不正确的是( )
|
查看习题详情和答案>>
(2012?唐山二模)【化学-选修化学与技术】
某科研小组设计出利用工业废酸(10% H2SO4)来堆浸某废弃的氧化铜锌矿的方案实现废物综合利用,方案如图所示.

已知各离子开始沉淀及完全沉淀时的pH如下表所示.
请回答下列问题:
(1)焙烧Zn2(OH)2CO3的化学反应方程式是
(2)堆浸后加入Fe粉发生的反应的离子方程式有
(3)加入A物质的目的是
A.KMnO4 B. HNO3 C.H2O2 D.Cl2
(4)除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在
(5)物质B可直接用作氮肥,则B的化学式是
查看习题详情和答案>>
某科研小组设计出利用工业废酸(10% H2SO4)来堆浸某废弃的氧化铜锌矿的方案实现废物综合利用,方案如图所示.

已知各离子开始沉淀及完全沉淀时的pH如下表所示.
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.34 | 9.7 |
| Fe3+ | 1.48 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
(1)焙烧Zn2(OH)2CO3的化学反应方程式是
Zn2(OH)2CO3
2ZnO+H2O+CO2↑
| ||
Zn2(OH)2CO3
2ZnO+H2O+CO2↑
.
| ||
(2)堆浸后加入Fe粉发生的反应的离子方程式有
Fe+2H+═Fe2++H2↑,Fe+Cu2+═Fe2++Cu
Fe+2H+═Fe2++H2↑,Fe+Cu2+═Fe2++Cu
.(3)加入A物质的目的是
将Fe2+氧化成Fe3+,以便除去
将Fe2+氧化成Fe3+,以便除去
,下列物质作为物质A使用较好的是C
C
.(填字母)A.KMnO4 B. HNO3 C.H2O2 D.Cl2
(4)除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在
3.2~6.2
3.2~6.2
范围之间.(5)物质B可直接用作氮肥,则B的化学式是
(NH4)2SO4
(NH4)2SO4
.