网址:http://m.1010jiajiao.com/timu_id_3671963[举报]
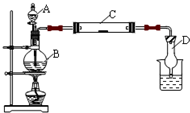 (2011?松江区模拟)为了制得氯气并探究氯气的一些化学性质,某学生用如图所示装置进行有关实验,打开A的玻璃塞,将A中浓盐酸溶液逐滴加入装有二氧化锰的B中.试回答:
(2011?松江区模拟)为了制得氯气并探究氯气的一些化学性质,某学生用如图所示装置进行有关实验,打开A的玻璃塞,将A中浓盐酸溶液逐滴加入装有二氧化锰的B中.试回答:(1)怎样检验装置的气密性
(2)若C中为淀粉KI试纸,实验片刻后C中可以观察到的实验现象为
B中发生反应的离子方程式
| ||
| ||
(3)若C中的淀粉KI试纸实验一段时间后又变为无色,原因是
(4)D的作用是
(5)若实验室暂时无二氧化锰,仍用此装置制取氯气,选用
某校化学实验兴趣小组进行实验室制取氯气,并验证氯气的某些化学性质实验,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略),按要求回答问题。

(1)下列方法中,可制得氯气的正确组合是 。
① MnO2和浓盐酸混合共热;② NaCl固体和浓硫酸混合共热;
③ 次氯酸钠和稀盐酸混合; ④ K2Cr2O7和浓盐酸混合;
⑤ KClO3和浓盐酸混合; ⑥ KMnO4和浓盐酸混合。
A.①②⑥ B.②④⑥ C.①③⑥ D.①④⑤⑥
(2)制取氯气时在烧瓶中加入一定量的MnO2,通过 (填仪器名称)向烧瓶中加入适量的浓盐酸,该反应的离子方程式: ;实验时为了除去氯气中的氯化氢气体,最好在A、B之间安装盛有 试剂的净化装置。
(3) 若用含有0.2 mol HCl的浓盐酸与足量的MnO2反应制Cl2,制得Cl2的体积(标准状况下)
总是小于1.12 L的原因是
(4)①装置B中盛有 试剂(填序号)a.浓硫酸 b.碱石灰 c.五氧化二磷 d.无水氯化钙。其作用是
②装置C中的现象是 ;D中下层液体的现象是
③装置E中发生反应的离子方程式为
(5)乙同学认为甲同学的实验有缺陷,提出在 位置后(填字母)增加一个装置,该装置中应放入 试剂,其作用是
查看习题详情和答案>>方法一:________________________________________。
方法二:________________________________________。
方法三:________________________________________。
方法四:________________________________________。
若制得相同质量的氧气,上述各反应中电子转移数目之比依次比为______________。
查看习题详情和答案>>(20分)某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明Cl2的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题:
(1)下列方法中,可制得的正确组合是__________。
①MnO2和浓盐酸混合共热; ②MnO2、NaCl和浓硫酸混合共热:
③NaClO和浓盐酸混合; ④K2Cr2O7和浓盐酸混合:
⑤KClO3和浓盐酸混合共热; ⑥KMnO4和浓盐酸混合。
A.①②⑥B.②④⑥C.①④⑥ D.全部可以
(2)写出实验室制取Cl2的离子方程式____________。
(3)若用含有0.2 mol HCl的浓盐酸与足量的MnO2反应制得Cl2的体积(标况下)总是小于1.12L的原因是_________________________________________。
(4)①装置B的作用是__________________________________。
②装置C和D出现的不同现象说明的问题是________________________。
③装置E的作用是_____________________。
(5)乙同学认为甲同学的实验有缺陷,不能确像最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液中的气体只有一种,乙同学提出应该在装置__________与________之间(填装置字母序号)增加一个装置,增加装置里面的试剂可为____________。
A.湿润的淀粉KI试纸B.氢氧化钠溶液
C.湿润的红色布条 D.饱和的食盐水
(1)若用溶有7.3g HCl的浓盐酸与足量的MnO2加热反应制得的Cl2在标准状况下体积总是小于1.12L,除盐酸挥发外,还因为
(2)下列方法中,也可制得Cl2的正确组合是
①MnO2、NaCl和浓硫酸混合共热;②浓盐酸与浓硝酸混合;③NaClO和浓盐酸混合;④PbO2和浓盐酸混合;⑤KClO3和浓盐酸混合共热;⑥KMnO4和浓盐酸混合.
A.①④⑤B.①②④⑤C.①③④⑤⑥D.全部可以
(3)某学习小组利用漂白粉与浓硫酸加热也得到了Cl2,他们用此反应原理设计了如下图所示装置制取氯气并探究其性质.
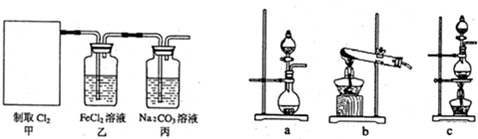
①甲部分的装置是
②证明乙装置中FeCl2发生了氧化反应的实验方法是
③丙装置中通入少量Cl2,可制得某种生活中常用的漂白、消毒的物质.已知相同条件下HClO的电离程度大于HCO3-,则丙中反应的化学方程式是
④该实验存在明显的缺陷,改进的方法是
(4)为测定漂白粉中Ca(ClO)2的质量分数,该小组将2.0g漂白粉配制成250mL溶液,取出25mL并向其中依次加入过量稀H2SO4、过量KI溶液,完全反应后,再滴入0.1mol?L-1 Na2S2O3溶液:2Na2S2O3+I2═Na2S4O6+2NaI,共消耗20mL Na2S2O3溶液,则漂白粉中Ca(ClO)2的质量分数为