摘要:14.S2- (3)非金属元素
网址:http://m.1010jiajiao.com/timu_id_3659234[举报]
23、某元素A的原子结构示意图为 该元素原子的核电荷数为
该元素原子的核电荷数为
查看习题详情和答案>>
 该元素原子的核电荷数为
该元素原子的核电荷数为16
,原子的最外层电子数是6
,A属非金属
元素.(填金属、非金属或稀有气体),A原子通过得失电子而形成的离子的符号是S2-
.24、下表是元素周期表中1~18号元素原子核外电子排布,我对它进行研究:

(1)原子序数为16的元素名称
(2)通过对元素周期表的分析,我能得出的一条信息是
(3)研究表明:在同一周期中,从左到右,原子失去电子的能力逐渐减弱,得到电子的能力逐渐增强.由此推断:第二周期中得电子能力最强的的是
查看习题详情和答案>>

(1)原子序数为16的元素名称
硫元素
是非金属元素
,在化学反应中,该元素的原子容易得
(填“得”或“失”)电子,成为阴
(填“阴”或“阳”)离子,离子符号为S2-
,原子序数为13的元素属于金属
(填“金属”或“非金属”).(2)通过对元素周期表的分析,我能得出的一条信息是
从左到右,元素原子的原子序数依次增加
.(3)研究表明:在同一周期中,从左到右,原子失去电子的能力逐渐减弱,得到电子的能力逐渐增强.由此推断:第二周期中得电子能力最强的的是
F
原子,具有稳定结构的是Ne
原子.元素周期表是学习化学的重要工具.下面是元素周期表中1~18号元素原子核外电子排布,我们对它进行研究:
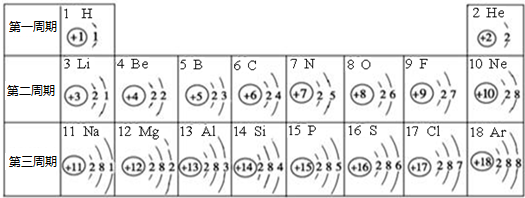
(1)第16号元素属于
(2)元素的化学性质与原子结构中的
(3)在同一族中各元素的原子结构呈现的规律有
(4)研究表明:第二周期从3~9号元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的吸引力逐渐增大,故原子半径逐渐减小.我分析第三周期从11~17号元素原子半径变化规律是
查看习题详情和答案>>

(1)第16号元素属于
非
非
金属元素(填“金属”或“非金属”),它在化学反应中容易得
得
失(填“得”或“失”)电子,所形成的微粒的符号:S2-
S2-
Mg2+(2)元素的化学性质与原子结构中的
原子核外
原子核外
最外层电子数关系密切.(3)在同一族中各元素的原子结构呈现的规律有
最外层电子数相同
最外层电子数相同
(任写一点)(4)研究表明:第二周期从3~9号元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的吸引力逐渐增大,故原子半径逐渐减小.我分析第三周期从11~17号元素原子半径变化规律是
原子半径逐渐减小
原子半径逐渐减小
. 17、 某元素A的原子结构示意图为:则该元素原子的核电荷数为
17、 某元素A的原子结构示意图为:则该元素原子的核电荷数为 14、右图为硫原子的结构示意图.
14、右图为硫原子的结构示意图.