摘要:2% 用相应的化学用语填空 ①5个氢气分子 , ②一个铜原子 , ③2个碳酸根离子 , ④铁元素的化合价为+3价 . (2)化学就在我们身边.它能改善我们的生活.请从“ A.氧气 B.氮气 C.生石灰 D.熟石灰 E.明矾 F. 尿素 中选择适当的物质填空 ①抢救危重病人常用的物质是 ,②用于农作物肥料的物质是 , ③常用作袋装食品干燥剂的是 ,④净化水时可作絮凝剂是 .
网址:http://m.1010jiajiao.com/timu_id_3659121[举报]
(2010?成都)木炭作为还原剂用于金属冶炼已有几千年历史.教材用如图I实验介绍这一知识.

(1)木炭与氧化铜反应的化学方程式是
(2)木炭呈块状,实验时要先将木炭研细,再与CuO粉末混合均匀后使用.这样处理的目的是
(3)酒精灯火焰处加有铁丝网罩,其作用时
(4)为了提高成功率,某研究小组设计如图Ⅱ方案进行实验.
【装置改进】
稳定的高温时本实验成果的关键因素之一,实验装置也会影响加热的效率.图Ⅱ装置将卧式装置改为直立式装置.实验时,将反应混合物夯实于试管底部,调节酒精灯是外焰完全包围试管的下部.你认为该设计是否更好?
【实验研究】
分别称取2g木炭与CuO的混合物,按每种比例重复实验3次.实验记录如下表:
由实验数据分析,影响实验的另一因素是
【讨论交流】
由于试管中有空气,实验时应注意:
①混合物需进行预热,除了使试管受热均匀外,目的是
②不能把石灰水浑浊作为木炭跟CuO反应的充分证据.因为试管中还可能发生反应:
【提出问题】关于影响该实验的因素,你认为还可进一步探究的问题
查看习题详情和答案>>

(1)木炭与氧化铜反应的化学方程式是
C+2CuO
2Cu+CO2↑
| ||
C+2CuO
2Cu+CO2↑
.
| ||
(2)木炭呈块状,实验时要先将木炭研细,再与CuO粉末混合均匀后使用.这样处理的目的是
增大反应物的接触面积,使反应更充分
增大反应物的接触面积,使反应更充分
.(3)酒精灯火焰处加有铁丝网罩,其作用时
使火焰更集中,提升温度
使火焰更集中,提升温度
.(4)为了提高成功率,某研究小组设计如图Ⅱ方案进行实验.
【装置改进】
稳定的高温时本实验成果的关键因素之一,实验装置也会影响加热的效率.图Ⅱ装置将卧式装置改为直立式装置.实验时,将反应混合物夯实于试管底部,调节酒精灯是外焰完全包围试管的下部.你认为该设计是否更好?
是
是
(填“是”或“否”);理由是铁丝网形成一个类似烟囱的空腔,使空气的对流加快,从而使燃烧更充分,火焰更稳定.
铁丝网形成一个类似烟囱的空腔,使空气的对流加快,从而使燃烧更充分,火焰更稳定.
.【实验研究】
分别称取2g木炭与CuO的混合物,按每种比例重复实验3次.实验记录如下表:
| 总质量相同(2g)但木炭与CuO比例不同的实验对比表 | |||||||
| 比例 | 1:6 | 1:7 | 1:8 | 1:9 | 1:10~1:11 | 1:12 | 1:13 |
| 加热时间 | 1′51″ | 1′43″ | 1′57″ | 1′51″ | 1′51″ | 1′53″ | 4′ |
| 实验现象 | 红热,产生大量气泡,石灰水变浑浊 | 偶尔红热,气泡较少 | |||||
| 实验结果 | 表层铜珠较大,出现未完全反应的黑色木炭粉末,且木炭含量越高黑色粉末越多 | 反应较完全,生成亮红色网状铜块 | 部分生成Cu2O | 主要产物是Cu2O | |||
反应物的比例
反应物的比例
;从产物分析,该反应混合物的最佳比例范围是1:10~1:11
1:10~1:11
.【讨论交流】
由于试管中有空气,实验时应注意:
①混合物需进行预热,除了使试管受热均匀外,目的是
减少试管内剩余空气的量,降低氧气对实验的影响
减少试管内剩余空气的量,降低氧气对实验的影响
;②不能把石灰水浑浊作为木炭跟CuO反应的充分证据.因为试管中还可能发生反应:
C+O2
CO2
| ||
C+O2
CO2
(写化学方程式);
| ||
【提出问题】关于影响该实验的因素,你认为还可进一步探究的问题
反应物的形状(或反应温度)
反应物的形状(或反应温度)
.
追踪科学家的足迹
材料1:纯碱的产量是衡量一个国家化学工业发展水平的重要指标.下面是实验室摸拟侯氏制碱法生产原理的主要过程:
(1)20℃时,向浓氨水中通入足量的二氧化碳得到NH4HCO3饱和溶液;
②向NH4HCO3饱和溶液中加入食盐细粒,并不断搅拌,直到NaHCO3结晶析出完毕;
③将析出的晶体过滤,得到晶体和滤液,洗涤晶体,然后将晶体放在试管中充分加热,得到Na2CO3;
④向③的滤液中加入食盐细粒,析出NH4CI晶体,过滤,得到NH4CI.
材料2:四种盐在不同温度下的溶解度表.
试回答下列问题:
(1)在实验室中,你选择的制备C02反应的化学方程式为 .在工业生产中,要获得生产纯碱的原料CO2你认为最经济实用的方法是以 为原料,该反应的化学方程式为 .
(2)有人认为侯氏制碱法有以下优点,你认为其中正确的是 .
A.生产过程中部分反应产物可作为原料循环使用
B.副产品是一种氮肥
C.反应都不需要加热,可节约能源
(3)检验③中的白色粉末中是否含有氯化钠的方法是 .
(4)在②中,随着食盐的逐渐加入,溶液变成了NH4HCO3和NaCl的混合溶液,析出晶体之前,混合溶液中存在的离子有(用离子符号表示,下同.) .在③中,将析出的晶体过滤后,溶液中数量减少的离子有 ;滤液中仍然存在的离子有 .②中反应的化学方程式为 .
(5)在20℃时,向含NH4HC0321g的饱和溶液中加入足量食盆.试通过计算说明,随着食盐的逐渐加入,为什么会有NaHC03晶体析出,而没有NH4Cl. 查看习题详情和答案>>
材料1:纯碱的产量是衡量一个国家化学工业发展水平的重要指标.下面是实验室摸拟侯氏制碱法生产原理的主要过程:
(1)20℃时,向浓氨水中通入足量的二氧化碳得到NH4HCO3饱和溶液;
②向NH4HCO3饱和溶液中加入食盐细粒,并不断搅拌,直到NaHCO3结晶析出完毕;
③将析出的晶体过滤,得到晶体和滤液,洗涤晶体,然后将晶体放在试管中充分加热,得到Na2CO3;
④向③的滤液中加入食盐细粒,析出NH4CI晶体,过滤,得到NH4CI.
材料2:四种盐在不同温度下的溶解度表.
| 温度 盐 溶解度 |
10℃ | 20℃ | 30℃ | 40℃ | 50℃ |
| NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| NH4HCO3 | 15.8 | 21.0 | 27.0 | ------ | ------ |
| NaHCO3 | 8.1 | 9.6 | 11.1 | 12.7 | ---- |
| NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
(1)在实验室中,你选择的制备C02反应的化学方程式为
(2)有人认为侯氏制碱法有以下优点,你认为其中正确的是
A.生产过程中部分反应产物可作为原料循环使用
B.副产品是一种氮肥
C.反应都不需要加热,可节约能源
(3)检验③中的白色粉末中是否含有氯化钠的方法是
(4)在②中,随着食盐的逐渐加入,溶液变成了NH4HCO3和NaCl的混合溶液,析出晶体之前,混合溶液中存在的离子有(用离子符号表示,下同.)
(5)在20℃时,向含NH4HC0321g的饱和溶液中加入足量食盆.试通过计算说明,随着食盐的逐渐加入,为什么会有NaHC03晶体析出,而没有NH4Cl. 查看习题详情和答案>>
追踪科学家的足迹
材料1:纯碱的产量是衡量一个国家化学工业发展水平的重要指标.下面是实验室摸拟侯氏制碱法生产原理的主要过程:
(1)20℃时,向浓氨水中通入足量的二氧化碳得到NH4HCO3饱和溶液;
②向NH4HCO3饱和溶液中加入食盐细粒,并不断搅拌,直到NaHCO3结晶析出完毕;
③将析出的晶体过滤,得到晶体和滤液,洗涤晶体,然后将晶体放在试管中充分加热,得到Na2CO3;
④向③的滤液中加入食盐细粒,析出NH4Cl晶体,过滤,得到NH4Cl.
材料2:四种盐在不同温度下的溶解度表.
试回答下列问题:
(1)在实验室中,你选择的制备C02反应的化学方程式为 .在工业生产中,要获得生产纯碱的原料CO2你认为最经济实用的方法是以 为原料,该反应的化学方程式为 .
(2)有人认为侯氏制碱法有以下优点,你认为其中正确的是 .
A.生产过程中部分反应产物可作为原料循环使用
B.副产品是一种氮肥
C.反应都不需要加热,可节约能源
(3)检验③中的白色粉末中是否含有氯化钠的方法是 .
(4)在②中,随着食盐的逐渐加入,溶液变成了NH4HCO3和NaCl的混合溶液,析出晶体之前,混合溶液中存在的离子有(用离子符号表示,下同.) .在③中,将析出的晶体过滤后,溶液中数量减少的离子有 ;滤液中仍然存在的离子有 .②中反应的化学方程式为 .
(5)在20℃时,向含NH4HC03 21g的饱和溶液中加入足量食盆.试通过计算说明,随着食盐的逐渐加入,为什么会有NaHC03晶体析出,而没有NH4CI晶休析出?理论上能析出多少克NaHCO3?(友情提示:本小题没有计算过程不得分.可能用到的相对分子质量:NH4HC03:79; NaCl:58.5; NaHC03:84,NH4CI:53.5). 查看习题详情和答案>>
材料1:纯碱的产量是衡量一个国家化学工业发展水平的重要指标.下面是实验室摸拟侯氏制碱法生产原理的主要过程:
(1)20℃时,向浓氨水中通入足量的二氧化碳得到NH4HCO3饱和溶液;
②向NH4HCO3饱和溶液中加入食盐细粒,并不断搅拌,直到NaHCO3结晶析出完毕;
③将析出的晶体过滤,得到晶体和滤液,洗涤晶体,然后将晶体放在试管中充分加热,得到Na2CO3;
④向③的滤液中加入食盐细粒,析出NH4Cl晶体,过滤,得到NH4Cl.
材料2:四种盐在不同温度下的溶解度表.
| 温度 盐 溶解度 |
10℃ | 20℃ | 30℃ | 40℃ | 50℃ |
| NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| NH4HCO3 | 15.8 | 21.0 | 27.0 | ------ | ------ |
| NaHCO3 | 8.1 | 9.6 | 11.1 | 12.7 | ---- |
| NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
(1)在实验室中,你选择的制备C02反应的化学方程式为
(2)有人认为侯氏制碱法有以下优点,你认为其中正确的是
A.生产过程中部分反应产物可作为原料循环使用
B.副产品是一种氮肥
C.反应都不需要加热,可节约能源
(3)检验③中的白色粉末中是否含有氯化钠的方法是
(4)在②中,随着食盐的逐渐加入,溶液变成了NH4HCO3和NaCl的混合溶液,析出晶体之前,混合溶液中存在的离子有(用离子符号表示,下同.)
(5)在20℃时,向含NH4HC03 21g的饱和溶液中加入足量食盆.试通过计算说明,随着食盐的逐渐加入,为什么会有NaHC03晶体析出,而没有NH4CI晶休析出?理论上能析出多少克NaHCO3?(友情提示:本小题没有计算过程不得分.可能用到的相对分子质量:NH4HC03:79; NaCl:58.5; NaHC03:84,NH4CI:53.5). 查看习题详情和答案>>
木炭作为还原剂用于金属冶炼已有几千年历史.教材用如图I实验介绍这一知识.

(1)木炭与氧化铜反应的化学方程式是 .
(2)木炭呈块状,实验时要先将木炭研细,再与CuO粉末混合均匀后使用.这样处理的目的是 .
(3)图Ⅱ酒精灯火焰处加有铁丝网罩,其作用时 .
(4)为了提高成功率,某研究小组设计如图Ⅱ方案进行实验.
装置改进:
稳定的高温是本实验成功的关键因素之一,实验装置也会影响加热的效率.图Ⅱ装置将卧式装置改为直立式装置.实验时,将反应混合物夯实于试管底部,调节酒精灯使外焰完全包围试管的下部.你认为该设计是否更好? (填“是”或“否”);理由是 ;
实验研究:
分别称取2g木炭与CuO的混合物,按每种比例重复实验3次.实验记录如下表:
总质量相同(2g)但木炭与CuO比例不同的实验对比表
由实验数据分析,影响实验的另一因素是 ;从产物分析,该反应混合物的最佳比例范围是 .
反思交流:
交流中小敏认为装置图Ⅰ存在一定的问题,请你指出它的主要问题是 ,改进的方法是 .
提出问题:关于影响该实验的因素,你认为还可进一步探究的问题 .
查看习题详情和答案>>

(1)木炭与氧化铜反应的化学方程式是
(2)木炭呈块状,实验时要先将木炭研细,再与CuO粉末混合均匀后使用.这样处理的目的是
(3)图Ⅱ酒精灯火焰处加有铁丝网罩,其作用时
(4)为了提高成功率,某研究小组设计如图Ⅱ方案进行实验.
装置改进:
稳定的高温是本实验成功的关键因素之一,实验装置也会影响加热的效率.图Ⅱ装置将卧式装置改为直立式装置.实验时,将反应混合物夯实于试管底部,调节酒精灯使外焰完全包围试管的下部.你认为该设计是否更好?
实验研究:
分别称取2g木炭与CuO的混合物,按每种比例重复实验3次.实验记录如下表:
总质量相同(2g)但木炭与CuO比例不同的实验对比表
| 比例 | 1:6 | 1:7 | 1:8 | 1:9 | 1:10~1:11 | 1:12 | 1:13 |
| 加热时间 | 1′51″ | 1′43″ | 1′57″ | 1′51″ | 1′51″ | 1′53″ | 4′ |
| 实验现象 | 红热,产生大量气泡,石灰水变浑浊 | 偶尔红热,气泡较少 | |||||
| 实验结果 | 表层铜珠较大,出现未完全反应的黑色木炭粉末,且木炭含量越高黑色粉末越多 | 反应较完全,生成亮红色网状铜块 | 部分生成Cu2O | 主要产物是Cu2O | |||
反思交流:
交流中小敏认为装置图Ⅰ存在一定的问题,请你指出它的主要问题是
提出问题:关于影响该实验的因素,你认为还可进一步探究的问题
木炭作为还原剂用于金属冶炼已有几千年历史.教材用如图Ⅰ实验介绍这一知识.
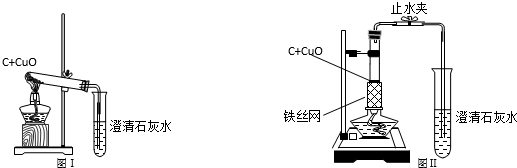
(1)木炭与氧化铜反应的化学方程式是 ;
(2)如图Ⅰ实验中试管口向下倾斜的目的是 ;
(3)木炭呈块状,实验时要先将木炭研细,再与CuO粉末混合均匀后使用,这样处理的目的是 ;
(4)酒精灯火焰处加油铁丝网罩,作用是 ;
(5)为提高成功率,某研究小组设计如图Ⅱ方案实验.
【装置改进】
稳定的高温是本实验成功的关键因素之一,实验装置也会影响加热的效率.图Ⅱ装置将卧式装置改为立式装置.实验时,将反应混合物夯实于试管底部,调节酒精灯外焰完全包围试管的下部.你认为设计是否更好? (填“是”或“否”);理由是 ;
【实验研究】
分别称取2g木炭和氧化铜的混合物,按每种比例重复实验3次.实验记录如表:
总质量相同(2g)的木炭与CuO比例不同的实验对比表
由实验数据分析,影响实验的另一因素是 ;
从产物分析,该混合物的最佳比例范围是 .
【讨论交流】
由于试管中有空气,实验时应该注意:
①混合物需进行预热,除了使试管均匀受热外,目的 ;
②不能把石灰水浑浊作为木炭跟CuO反应的充分证据,因为试管中还可能发生反应:
(写化学方程式).
【提出问题】关于影响实验的因素,你认为还可以进一步探究的问题: .
查看习题详情和答案>>

(1)木炭与氧化铜反应的化学方程式是
(2)如图Ⅰ实验中试管口向下倾斜的目的是
(3)木炭呈块状,实验时要先将木炭研细,再与CuO粉末混合均匀后使用,这样处理的目的是
(4)酒精灯火焰处加油铁丝网罩,作用是
(5)为提高成功率,某研究小组设计如图Ⅱ方案实验.
【装置改进】
稳定的高温是本实验成功的关键因素之一,实验装置也会影响加热的效率.图Ⅱ装置将卧式装置改为立式装置.实验时,将反应混合物夯实于试管底部,调节酒精灯外焰完全包围试管的下部.你认为设计是否更好?
【实验研究】
分别称取2g木炭和氧化铜的混合物,按每种比例重复实验3次.实验记录如表:
总质量相同(2g)的木炭与CuO比例不同的实验对比表
| 比例 | 1:6 | 1:7 | 1:8 | 1:9 | 1:10~1:11 | 1:12 | 1:13 |
| 时间 | 1'51〃 | 1'43〃 | 1'57〃 | 1'51〃 | 1'51〃 | 1'53〃 | 4' |
| 实验现象 | 红热,产生大量气泡,澄清石灰水变浑浊 | 偶尔红热,气泡较少 | |||||
| 实验结果 | 表层铜珠较大,出现未完全反应的黑色木炭粉末,且木炭含量越高黑色粉末越多 | 反应较完全,生成亮红色网状铜块 | 部分生成Cu2O | 主要产物是Cu2O | |||
从产物分析,该混合物的最佳比例范围是
【讨论交流】
由于试管中有空气,实验时应该注意:
①混合物需进行预热,除了使试管均匀受热外,目的
②不能把石灰水浑浊作为木炭跟CuO反应的充分证据,因为试管中还可能发生反应:
【提出问题】关于影响实验的因素,你认为还可以进一步探究的问题: