网址:http://m.1010jiajiao.com/timu_id_3657765[举报]
(1)将浓度均为0.1mol/L的BaCl2溶液与Na2SO4溶液等体积混合,充分搅拌后过滤,滤液中c(Ba2+)=______mol/L.取100mL滤液与100mL2mol/LNa2SO4的溶液混合,混合液中c(Ba2+)=______mol/L.
(2)医学上进行消化系统的X射线透视时,常使用BaSO4作内服造影剂.胃酸很强(pH约为1),但服用大量BaSO4仍然是安全的,BaSO4不溶于酸的原因是(用溶解平衡原理解)______.
万一误服了少量BaCO3,应尽快用大量0.5mol/LNa2SO4溶液给患者洗胃,如果忽略洗胃过程中Na2SO4溶液浓度的变化,残留在胃液中的Ba2+浓度仅为______mol/L.
(3)长期使用的锅炉需要定期除水垢,否则会降低燃料的利用率.水垢中含有的CaSO4,可先用Na2CO3溶液处理,使之转化为疏松、易溶于酸的CaCO3,而后用酸除去.
①CaSO4 转化为CaCO3的离子方程式为______
②请分析CaSO4 转化为CaCO3的原理______.
查看习题详情和答案>>
科学家利用淡水与海水之间含盐量的差别发明了一种新型电池——水电池。
(1)用二氧化锰纳米棒作电池正极可提高发电效率,这是利用纳米材料的 特性,使之能与钠离子充分接触。
(2)水电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,该电池的负极反应式为 。水电池工作时,Na+不断向 极方向移动。
(3)水电池生成1 mol Na2Mn5O10转移电子的物质的量为 。
(4)某温度下,Fe(OH)3(s)、Mg(OH)2(s)分别在溶液中达到沉淀溶解平衡后,溶液中金属阳离子的浓度与溶液pH的关系如右图。请据右图分析:

①该温度下,溶度积常数的关系为:KSP[Fe(OH)3] KSP[Mg(OH)2](填“>”、“=”或“<”);
②如果在新生成的Mg(OH)2浊液中滴入足量的FeCl3溶液,振荡后,白色沉淀会全部转化为红褐色沉淀,原因是 。
查看习题详情和答案>>
科学家利用淡水与海水之间含盐量的差别发明了一种新型电池——水电池。
(1)用二氧化锰纳米棒作电池正极可提高发电效率,这是利用纳米材料的 特性,使之能与钠离子充分接触。
(2)水电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,该电池的负极反应式为 。水电池工作时,Na+不断向 极方向移动。
(3)水电池生成1 mol Na2Mn5O10转移电子的物质的量为 。
(4)某温度下,Fe(OH)3(s)、Mg(OH)2(s)分别在溶液中达到沉淀溶解平衡后,溶液中金属阳离子的浓度与溶液pH的关系如右图。请据右图分析: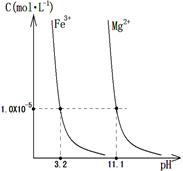
①该温度下,溶度积常数的关系为:KSP[Fe(OH)3] KSP[Mg(OH)2](填“>”、“=”或“<”);
②如果在新生成的Mg(OH)2浊液中滴入足量的FeCl3溶液,振荡后,白色沉淀会全部转化为红褐色沉淀,原因是 。
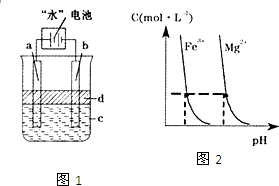 “水”电池是利用淡水与海水之间含盐量的差别进行发电的一种新型电池.(1)研究表明,电池用二氧化锰纳米棒为正极材料可提高发电效率,这是利用纳米材料具有
“水”电池是利用淡水与海水之间含盐量的差别进行发电的一种新型电池.(1)研究表明,电池用二氧化锰纳米棒为正极材料可提高发电效率,这是利用纳米材料具有(3)利用电解实验可以制得纯净的Fe(OH)2白色沉淀,如图1,已知两电极的材料分别为石墨和铁.
①若图中的电池为“水”电池,则其与a极相连的电极是由下列物质中的
A.MnO2 B.Ag C.NaCl D.Na2Mn5O10 E.AgCl
②a极的电极反应式为
③电解液c可以是
A.纯水 B.NaCl溶液 C.H2SO4溶液 D.CuCl2溶液
④当生成1mol Fe(OH)2白色沉淀时将消耗MnO2
(4)某温度下,Fe(OH)3(s)、Mg(OH)2(s)分别在溶液中达到沉淀溶解平衡后,溶液中金属阳离子的浓度与溶液pH的关系如图2.请据图2分析:①该温度下,溶度积常数的关系为:KSP[Fe(OH)3]
KSP[Mg(OH)2](填“>”、“=”或“<”);
②如果在新生成的Mg(OH)2浊液中滴入足量的Fe3+,振荡后,白色沉淀会全部转化为红褐色沉淀,原因是
“水”电池是利用淡水与海水之间含盐量的差别进行发电的一种新型电池.
(1)研究表明,电池用二氧化锰纳米棒为正极材料可提高发电效率,这是利用纳米材料具有________特性,使之能与钠离子充分接触.
(2)“水”电池总反应可表示为:5MnO2+2Ag+2NaCl![]() Na2Mn5O10+2AgCl,该电池的负极反应式为________.
Na2Mn5O10+2AgCl,该电池的负极反应式为________.
(3)利用电解实验可以制得纯净的Fe(OH)2白色沉淀,如下图所示,已知两电极的材料分别为石墨和铁.

①若图中的电池为“水”电池,则其与a极相连的电极是由下列物质中的________制成(填编号,下同).
A.MnO2
B.Ag
C.NaCl
D.Na2Mn5O10
E.AgCl
②a极的电极反应式为________.
③电解液c可以是________.
A.纯水
B.NaCl溶液
C.H2SO4溶液
D.CuCl2溶液
④当生成1 mol Fe(OH)2白色沉淀时将消耗MnO2________mol.
(4)某温度下,Fe(OH)3(s)、Mg(OH)2(s)分别在溶液中达到沉淀溶解平衡后,溶液中金属阳离子的浓度与溶液pH的关系如下图.请据图分析:

①该温度下,溶度积常数的关系为:KSP[Fe(OH)3]________KSP[Mg(OH)2](填“>”、“=”或“<”);
②如果在新生成的Mg(OH)2浊液中滴入足量的Fe3+,振荡后,白色沉淀会全部转化为红褐色沉淀,原因是________.