摘要:33.(1)CO2+Ca(OH)2=CaCO3↓+H2O (2)①氢氧化钠溶液与CO2发生反应.使容器内气压降低 ②CO2能溶于水.也能使容器内气压降低 将氢氧化钠溶液换成等体积的水 ③稀盐酸 有气泡产生(或加氯化钙溶液 有沉淀生成 其他合理答案均可) ④A 氢氧化钠有腐蚀性.易伤到手
网址:http://m.1010jiajiao.com/timu_id_3656631[举报]
 (2013?建邺区一模)氢氧化钠俗名苛性钠,是一种重要的化工原料.下列研究从其结构、制备方法、性质以及变化规律等角度进行,请根据要求回答相应问题.
(2013?建邺区一模)氢氧化钠俗名苛性钠,是一种重要的化工原料.下列研究从其结构、制备方法、性质以及变化规律等角度进行,请根据要求回答相应问题.Ⅰ.结构:
NaOH含有钠元素,钠在元素周期表中处于第三周期的
开头
开头
(填“开头”、“中间”或“结尾”).NaOH属于碱,碱在溶液中都可以电离出相同的离子,该离子是
OH-
OH-
(填离子符号).Ⅱ.制备:
实验室用纯碱制备烧碱的化学反应方程式为
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
.Ⅲ.性质及变化:
(1)氢氧化钠固体曝露在空气中容易
吸水潮解
吸水潮解
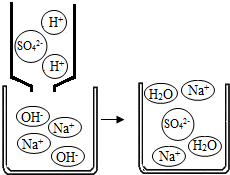
,因此它与生石灰一起用作某些气体的干燥剂(2)如右图所示,NaOH溶液可与稀酸反应的方程式为
2NaOH+H2SO4=Na2SO4+2H2O
2NaOH+H2SO4=Na2SO4+2H2O
.该反应没有明显的现象,为了说明该反应确实能够发生,下列哪种物质肯定无法帮助你达到目的
d
d
.a.镁条 b.酚酞 c.CuSO4 d.Ba(NO3)2
Ⅳ.保存:
张老师整理药品时,意外发现实验桌上有瓶敞口放置的NaOH固体,他让同学们对这瓶NaOH固体进行探究.
【提出猜想】
猜想I:没有变质
猜想Ⅱ:部分变质为Na2CO3,依据是
2NaOH+CO2=Na2CO3+H2O
2NaOH+CO2=Na2CO3+H2O
(用方程式表示);猜想Ⅲ:全部变质
【实验设计、现象和推断】
| 实验步骤 | 实验现象 |
| ①取少量白色固体于试管中,加水振荡后,至全部溶解 | 无色溶液 |
| ②向试管的溶液中滴加适量物质X的溶液 | 现象A |
| ③再向试管中滴加几滴酚酞试液. | 现象B |
稀盐酸
稀盐酸
,说明猜想I
I
可排除.(2)若X是Ca(OH)2溶液,现象A有白色沉淀,现象B为无色变红色,该实验
不能
不能
(填“能”或“不能”)说明猜想Ⅱ成立.(3)若X是CaCl2溶液,则猜想Ⅱ成立的实验现象是
现象A有白色沉淀产生,现象B溶液变成红色
现象A有白色沉淀产生,现象B溶液变成红色
.(4)定量研究:根据上述实验,可通过测定
产生气体的质量或产生白色沉淀的质量
产生气体的质量或产生白色沉淀的质量
,再通过计算得到氢氧化钠的变质情况.(2009?东丽区模拟)氢氧化钠固体必须密封保存,这是因为氢氧化钠既
查看习题详情和答案>>
易潮解
易潮解
又与空气中的二氧化碳反应
与空气中的二氧化碳反应
的缘故;欲证明氢氧化钠溶液露置于空气中而发生的变质,可加入稀盐酸
稀盐酸
溶液,有关反应的化学方程式为Na2CO3+2HCl=2NaCl+H2O+CO2↑
Na2CO3+2HCl=2NaCl+H2O+CO2↑
;若要除去因变质而带来的杂质,应加入氢氧化钙
氢氧化钙
溶液,其化学反应方程式为Na2CO3+Ca(OH)2=2NaOH+CaCO3↓.
Na2CO3+Ca(OH)2=2NaOH+CaCO3↓.
. 干燥剂“碱石灰”是氧化钙和氢氧化钠的混合物,在空气中容易变质.某研究小组对一只干燥管里的“碱石灰”样品的成分进行实验探究.
干燥剂“碱石灰”是氧化钙和氢氧化钠的混合物,在空气中容易变质.某研究小组对一只干燥管里的“碱石灰”样品的成分进行实验探究.[提出猜想]
猜想Ⅰ:没有变质,只含有氧化钙和氢氧化钠.
猜想Ⅱ:部分变质,含有…
猜想Ⅲ:完全变质,只含有碳酸钙、碳酸钠.
[实验探究]
| 操作 | 现象 | 结论 |
① |
试管外壁发烫,得到浑浊的液体 | 推测样品中含有 氧化钙和氢氧化钠至少有一个 氧化钙和氢氧化钠至少有一个 |
②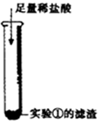 |
滤渣溶解,产生大量气泡 | 写出产生大量气泡的化学方程式 CaCO3+2HCl=CaCl2+H2O+CO2↑ CaCO3+2HCl=CaCl2+H2O+CO2↑ |
③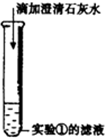 |
产生白色沉淀 | 写出产生白色沉淀的化学方程式 Ca(OH)2+Na2CO3=CaCO3↓+2NaOH Ca(OH)2+Na2CO3=CaCO3↓+2NaOH |
(1)从上述实验现象推断:猜想
II
II
成立.(2)“碱石灰”样品里是否一定含有碳酸钙?
不一定
不一定
(填“一定”或“不一定”),请说明理由.若碱石灰中同时有Ca(OH)2和Na2CO3加水后也会得到碳酸钙
若碱石灰中同时有Ca(OH)2和Na2CO3加水后也会得到碳酸钙
.(3)能用碱石灰干燥的气体是
DE
DE
.A.HCl B.CO2 C.SO2 D.NH3 E.O2.
同学们在实验室进行“二氧化碳的性质与制取”实验.请结合如图所示回答问题.
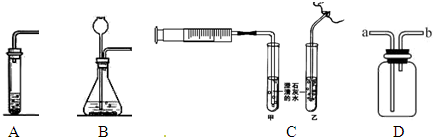
(1)制取二氧化碳:
①反应物应选择
②发生装置选择:
③经检查装置气密性良好后,装入药品开始实验.二氧化碳可用
(2)如图C所示,在甲、乙两支试管中分别装有相同质量相同浓度的澄清石灰水,用针管不断向甲试管石灰水中注入空气,通过导管向乙试管石灰水中不断吹气.实验发现,乙试管内的澄清石灰水先变浑浊.该实验能否说明人呼出的气体中二氧化碳浓度大于空气中的二氧化碳浓度?为什么
(3)实验室用无水醋酸钠和碱石灰两种固体混合共热制取甲烷气体,用硫化亚铁固体与稀硫酸制取硫化氢气体.以上两种气体可使用如图B所示发生装置的是
查看习题详情和答案>>

(1)制取二氧化碳:
①反应物应选择
石灰石
石灰石
和稀盐酸
稀盐酸
(均填物质名称),反应原理的符号表达式写为CaCO3+2HCl═CaCl2+H2O+CO2↑
CaCO3+2HCl═CaCl2+H2O+CO2↑
.②发生装置选择:
B
B
(填序号),理由反应物是固体和液体不需要加热,长颈漏斗可以随时添加液体药品
反应物是固体和液体不需要加热,长颈漏斗可以随时添加液体药品
.检查这套装置气密性的方法是(写明简单操作、现象及结论)从长颈漏斗口加入水,当液面没过长颈漏斗末端,再将导管一端浸入水中,用两手掌紧握锥形瓶外壁,如果导管口有气泡冒出,说明气密性良好
从长颈漏斗口加入水,当液面没过长颈漏斗末端,再将导管一端浸入水中,用两手掌紧握锥形瓶外壁,如果导管口有气泡冒出,说明气密性良好
.③经检查装置气密性良好后,装入药品开始实验.二氧化碳可用
向上排空气
向上排空气
法或排水法收集,能用排水法收集二氧化碳的原因是产生二氧化碳的速度远大于二氧化碳溶解或与水反应的速度
产生二氧化碳的速度远大于二氧化碳溶解或与水反应的速度
.排水法收集二氧化碳的最佳时机是有气泡连续均匀冒出
有气泡连续均匀冒出
.实验中发现有的组反应器内有大量气泡产生,却长时间收集不到二氧化碳气体,可能的原因有装入固体药品后未旋紧橡皮塞,装置漏气
装入固体药品后未旋紧橡皮塞,装置漏气
.还可用如图D所示装置以排空法收集二氧化碳,使用时,二氧化碳从a
a
管通入.(2)如图C所示,在甲、乙两支试管中分别装有相同质量相同浓度的澄清石灰水,用针管不断向甲试管石灰水中注入空气,通过导管向乙试管石灰水中不断吹气.实验发现,乙试管内的澄清石灰水先变浑浊.该实验能否说明人呼出的气体中二氧化碳浓度大于空气中的二氧化碳浓度?为什么
不能,未控制单位时间内注入气体的量相同
不能,未控制单位时间内注入气体的量相同
.二氧化碳使澄清石灰水变浑浊的反应符号表达式写为Ca(OH)2+CO2═CaCO3↓+H2O
Ca(OH)2+CO2═CaCO3↓+H2O
.(3)实验室用无水醋酸钠和碱石灰两种固体混合共热制取甲烷气体,用硫化亚铁固体与稀硫酸制取硫化氢气体.以上两种气体可使用如图B所示发生装置的是
硫化氢
硫化氢
. (2010?重庆)干燥剂“碱石灰”是氧化钙和氢氧化钠的混合物,在空气中容易变质.某研究小组对一只干燥管里的“碱石灰”样品的成分进行实验探究.
(2010?重庆)干燥剂“碱石灰”是氧化钙和氢氧化钠的混合物,在空气中容易变质.某研究小组对一只干燥管里的“碱石灰”样品的成分进行实验探究.【提出猜想】
猜想Ⅰ:没有变质,只含有氧化钙和氢氧化钠.
猜想Ⅱ:部分变质,含有…
猜想Ⅲ:完全变质,只含有碳酸钙、碳酸钠.
【实验探究】
| 操作 | 现象 | 结论 |
 | 试管外壁发烫,得到浑浊的液体. | 推测样品中含有 氢氧化钠(氧化钙和氢氧化钠至少有一个即可)、碳酸钙 氢氧化钠(氧化钙和氢氧化钠至少有一个即可)、碳酸钙 |
 | 滤渣溶解,产生大量气泡. | 写出产生大量气泡的化学方程式: CaCO3+2HCl=CaCl2+H2O+CO2↑ CaCO3+2HCl=CaCl2+H2O+CO2↑ |
 | 产生白色沉淀. | 写出产生白色沉淀的化学方程式: Ca(OH)2+Na2CO3=CaCO3↓+2NaOH Ca(OH)2+Na2CO3=CaCO3↓+2NaOH |
(1)从上述实验现象推断:猜想
II
II
成立.(2)“碱石灰”样品里是否一定含有碳酸钙?请说明理由.
不一定,若碱石灰中同时有Ca(OH)2和Na2CO3加水后也会得浑浊液体
不一定,若碱石灰中同时有Ca(OH)2和Na2CO3加水后也会得浑浊液体
.