网址:http://m.1010jiajiao.com/timu_id_3650535[举报]
水是地球上最重要的一种物质,试回答下列问题:
Ⅰ.饮用水的安全事关人民的健康,在饮用水的处理过程中,经常要用到消毒剂,其中以“84”消毒液、漂白粉等较为常见。除了上述消毒剂以外,ClO2由于处理水时不产生致癌的有机氯化物,因此已经逐渐地取代氯气等成为饮用水处理中常用的消毒剂。
(1)漂白粉的商品名又叫漂白精,其中包装袋上注明保存时要密封,启用后需要立即使用,切忌长时间放置,请用化学方程式表示其原因:______________________________________。
(2)生产ClO2常用的方法是在酸性条件下还原NaClO3,例如:
①2ClO![]() +4H++2Cl-===2ClO2↑+Cl2↑+2H2O
+4H++2Cl-===2ClO2↑+Cl2↑+2H2O
②2ClO![]() +SO
+SO![]() +2H+===2ClO2↑+SO
+2H+===2ClO2↑+SO![]() +H2O
+H2O
比较两种方法,你认为__________比较好,优点是________________________________________________。
Ⅱ.海水中含有大量的宝贵资源,工业上从海洋中制溴的方法是:先把盐卤(海水中氯化钠被分离后剩下的母液)加热到363 K后控制pH为3.5,通入氧气把溴置换出来,再用一种气体X把溴吹出并用碳酸钠溶液吸收,这时溴就歧化生成溴离子和溴酸根离子,最后用硫酸酸化,单质溴就从溶液中析出。根据上述信息回答下列问题:
(1)把溴吹出的气体X,工业上最适宜选用________。
A.NH3 B.空气 C.氩气 D.CO2
(2)用Na2CO3溶液吸收溴,再用硫酸酸化,析出溴,是工业上获取溴的方法之一。用离子方程式表示该反应过程:
①____________________________________;
②____________________________________。
查看习题详情和答案>>.(16分)化学实验是科学探究的基础。请回答有关实验问题:
(1)下面的四个实验装置有三个都存在明显缺陷,其中完全正确的是 :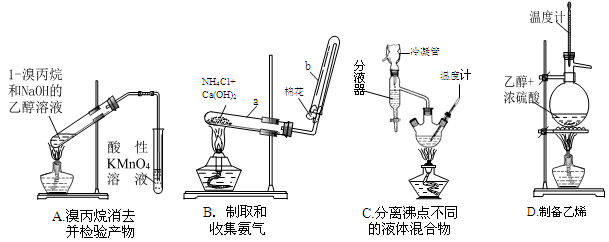
(2)要检验上面B装置氨气已集满的操作是 则试管已集满。
(3)ClO2是一种安全、高效、广谱、强力杀菌剂,其性质如右表:
①由下表可以看出:保存液态ClO2的条件是密封、 ;ClO2与碱反应的离子方程式 ;观察下“图A”,要从NaClO2溶液制得不含结晶水的晶体,操作是蒸发结晶,控制条件是 ;应控制析出晶体的温度范围是 。
| 色态 | 溶于碱 | 超过1Kpa、受热或遇光 | |
| 常温气体 | -59-11℃ 红黄色液体 | 生成亚氯酸盐和氯酸盐 | 爆炸 |
②工业用潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得。某学生拟用下图B所示装置模拟工业制法制取并收集液态ClO2,请模仿下图B的装置图和图例,在答题卡的相应图中补充完善装置图,并作必要的标注。
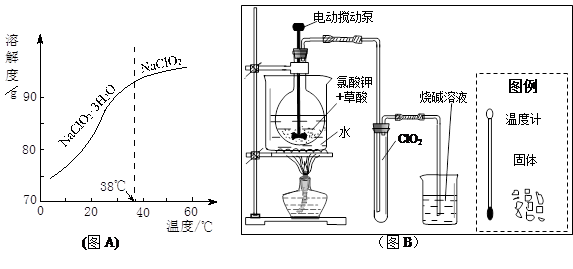 查看习题详情和答案>>
查看习题详情和答案>>
(16分)化学实验是科学探究的基础。请回答有关实验问题:
(1)下面的四个实验装置有三个都存在明显缺陷,其中完全正确的是 :
(2)要检验上面B装置氨气已集满的操作是 则试管已集满。
(3)ClO2是一种安全、高效、广谱、强力杀菌剂,其性质如右表:
| 色态 | 溶于碱 | 超过1Kpa、受热或遇光 | |
| 常温气体 | -59-11℃红黄色液体 | 生成亚氯酸盐和氯酸盐 | 爆炸 |
②工业用潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得。某学生拟用下图B所示装置模拟工业制法制取并收集液态ClO2,请模仿下图B的装置图和图例,在答题卡的相应图中补充完善装置图,并作必要的标注。
 查看习题详情和答案>>
查看习题详情和答案>>