摘要:用电子式表示物质的形成过程: HCl ,Na2O2 , H2O ,CaCl2 , [典型例题] 例1.下列离子中.电子数大于质子数且质子数大于中子数的是 A.D3O+ B.Li+ C.OD¯ D.OH¯ 例2.下列原子或离子核外电子排布不属于基态排布的是 A.N: 1s22s22p3 B.S2-: 1s22s22p63s23p6 C.Na: 1s22s22p53s2 D.Si: 1s22s22p63s23p2 例3.下列化学式中.能真实表示物质的分子组成的是 A.CuSO4 B.CS2 C.Ar D.CsCl 例4.有关苯分子中的化学键描述正确的是 A.每个碳原子的sp2杂化轨道中的其中一个形成大π键 B.每个碳原子的未参加杂化的2p轨道形成大π键 C.碳原子的三个sp2杂化轨道形成三个σ键 D.碳原子的未参加杂化的2p轨道形成σ键 例5.下列各组分子中.都属于含极性键的非极性分子的是 A. CO2 H2S B. C2H4 CH4 C. C60 C2H4 D.NH3 HCl [针对性练习]
网址:http://m.1010jiajiao.com/timu_id_3649052[举报]
【化学--选修3:物质结构与性质】
现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
(1)G位于 族 区,价电子排布式为 .
(2)B基态原子中能量最高的电子,其电子云在空间有 个方向,原子轨道呈
形.
(3)画出C原子的电子排布图 .
(4)已知BA5为离子化合物,写出其电子式 .
(5)DE3中心原子的杂化方式为 ,用价层电子对互斥理论推测其空间构型为 .
(6)用电子式表示F元素与E元素形成化合物的形成过程 .
查看习题详情和答案>>
现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(2)B基态原子中能量最高的电子,其电子云在空间有
形.
(3)画出C原子的电子排布图
(4)已知BA5为离子化合物,写出其电子式
(5)DE3中心原子的杂化方式为
(6)用电子式表示F元素与E元素形成化合物的形成过程
化学学习中有很多形如“A+B→C+D”的反应,请根据不同的情况回答下列问题:
(1)如果上式中A、B、C、D均为多核10电子微粒,其中A为阳离子,B为阴离子,C、D均为分子,且C的相对分子质量比D大1.
则:①A+B→C+D表示的离子方程式为 .
②标准状况下,若2.24L的D被100mL 2mol/L盐酸吸收,则所得溶液中各离子浓度从大到小的顺序为 .
(2)如果上式中A、C为生活中常见的金属单质,B、D为两种氧化物且它们的摩尔质量比为12:17,其中D能与NaOH溶液反应.
则:①A+B→C+D表示的化学方程式为 .
②D与NaOH溶液反应的化学方程式为 .
③工业上,将B、D按一定的量溶于盐酸后,继续通入气体Z,再加入NaOH溶液调节pH可得高效净水剂[化学式为CA(OH)nCl6-n],则气体Z的作用是 ,B、D的最佳物质的量之比是 .
④工业上,通常第一步先用C与过量稀硫酸作用得溶液X:第二步再往溶液X中加入亚硝酸钠来制备C(OH)SO4,同时有气体NO生成,写出第二步反应的化学方程式为 .
查看习题详情和答案>>
(1)如果上式中A、B、C、D均为多核10电子微粒,其中A为阳离子,B为阴离子,C、D均为分子,且C的相对分子质量比D大1.
则:①A+B→C+D表示的离子方程式为
②标准状况下,若2.24L的D被100mL 2mol/L盐酸吸收,则所得溶液中各离子浓度从大到小的顺序为
(2)如果上式中A、C为生活中常见的金属单质,B、D为两种氧化物且它们的摩尔质量比为12:17,其中D能与NaOH溶液反应.
则:①A+B→C+D表示的化学方程式为
②D与NaOH溶液反应的化学方程式为
③工业上,将B、D按一定的量溶于盐酸后,继续通入气体Z,再加入NaOH溶液调节pH可得高效净水剂[化学式为CA(OH)nCl6-n],则气体Z的作用是
④工业上,通常第一步先用C与过量稀硫酸作用得溶液X:第二步再往溶液X中加入亚硝酸钠来制备C(OH)SO4,同时有气体NO生成,写出第二步反应的化学方程式为
 (2012?长春三模)[化学-选修 物质结构与性质]A、B、C、D、E、F为原子序数依次增大的六种元素.已知:A是周期表中原子半径最小的元素,B的基态原子核外电子有7种运动状态,B、C、E三种元素原子中未成对电子数之比为3:2:1,D原子核外有4个能级且均充满电子,D与E可形成DE2形化合物,F原子核外最外层只有1个电子,其余各层均充满电子.
(2012?长春三模)[化学-选修 物质结构与性质]A、B、C、D、E、F为原子序数依次增大的六种元素.已知:A是周期表中原子半径最小的元素,B的基态原子核外电子有7种运动状态,B、C、E三种元素原子中未成对电子数之比为3:2:1,D原子核外有4个能级且均充满电子,D与E可形成DE2形化合物,F原子核外最外层只有1个电子,其余各层均充满电子.回答下列问题:
(1)B、C、D三种元素的第一电离能由大到小的顺序为
N>O>Mg
N>O>Mg
.(用元素符号表示)(2)F在周期表中位于
ds
ds
区,其价电子排布式为3d104s1
3d104s1
,与F同周期且未成对电子数最多的元素为Cr
Cr
(填写元素符号).(3)B、E二种元素中可形成XY3形化合物的化学式为
NCl3
NCl3
,其中心原子杂化方式为sp3
sp3
,分子的空间构型为三角锥形
三角锥形
.(4)A与B形成的化合物易溶解在A与C形成的化合物中,其原因是
两分子间易形成氢键
两分子间易形成氢键
.(5)DC化合物熔点高于DE2的熔点,其原因是
MgO的晶格能高于MgCl2
MgO的晶格能高于MgCl2
.(6)F2+与NH3形成配离子[F(NH3)4]2+,在[F(NH3)4]2+中,F2+位于正四面体中心,NH3位于正四面体的顶点,试在图中表示[F(NH3)4]2+中F2+与N之间的化学键
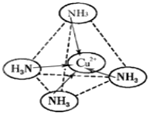

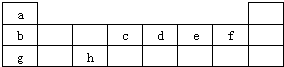 (2010?普陀区二模)如图是元素周期表的前三周期.请用相应的化学用语回答下列问题:
(2010?普陀区二模)如图是元素周期表的前三周期.请用相应的化学用语回答下列问题:(1)写出由e形成的两种阴离子的符号,它们带有相同的电荷数:
O2-
O2-
、O22-
O22-
;(2)h的单质能与g元素的最高价氧化物对应水化物的溶液反应,请写出该反应的化学方程式
2NaOH+2Al+2H2O=2NaAlO2+3H2↑
2NaOH+2Al+2H2O=2NaAlO2+3H2↑
(3)图1表示的是b、c、d、e、f的氢化物的沸点(℃).序列“5”的氢化物是由
极性
极性
键构成的非极性
非极性
分子(均填写“极性”或“非极性”).由c和 e 组成的可灭火的物质的电子式是

(4)图2是表示第三周期8种元素单质的熔点(℃)柱形图,已知柱形“1”代表Ar,则柱形“8”熔点最高的原因是
晶体硅是原子晶体,熔点最高
晶体硅是原子晶体,熔点最高
.
【化学-选修物质结构与性质】
X、Y、Z、Q、E、F六种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在第二周期主族元素中电负性最大的元素.
请回答下列问题:
(1)XZ2与YZ2分子的立体结构分别是
(2)Q的元素符号是
(3)用氢键表示式写出E的氢化物溶液中存在的所有氢键
(4)F的氢化物是一种碱性气体,F还可与氢形成离子化合物FH5, 其电子式为
其电子式为
 ;其晶体的最小结构单元如图所示经实验测得CA5晶体的密度为dg/cm3,阿伏加德罗常数用NA表示,则该晶体中阴离子与阳离子之间的最短距离为
;其晶体的最小结构单元如图所示经实验测得CA5晶体的密度为dg/cm3,阿伏加德罗常数用NA表示,则该晶体中阴离子与阳离子之间的最短距离为
cm.
查看习题详情和答案>>
X、Y、Z、Q、E、F六种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在第二周期主族元素中电负性最大的元素.
请回答下列问题:
(1)XZ2与YZ2分子的立体结构分别是
V形
V形
和直线形
直线形
,相同条件下两者在水中的溶解度较大的是SO2
SO2
(写分子式),理由是因为CO2是非极性分子,SO2和H2O都是极性分子,根据“相似相溶”原理,SO2在H2O中的溶解度较大
因为CO2是非极性分子,SO2和H2O都是极性分子,根据“相似相溶”原理,SO2在H2O中的溶解度较大
;(2)Q的元素符号是
Cr
Cr
,它的核外电子排布式为1s22s22p63s23p63d54s1
1s22s22p63s23p63d54s1
,在形成化合物时它的最高化合价为+6
+6
;(3)用氢键表示式写出E的氢化物溶液中存在的所有氢键
F-H…FF-H…O O-H…F O-H…O
F-H…FF-H…O O-H…F O-H…O
.(4)F的氢化物是一种碱性气体,F还可与氢形成离子化合物FH5,
 其电子式为
其电子式为

| ||
| 2 |
| 3 |
| ||
| ||
| 2 |
| 3 |
| ||